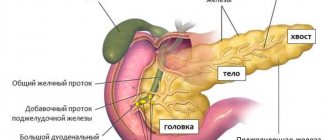
Ферменты поджелудочной железы играют важнейшую роль в процессе переваривания в тонкой кишке поступившей из желудка пищи. Биокарбонат, являющийся основным компонентом панкреатического сока, создает щелочную среду, нейтрализует кислотность пищевой массы с желудочным соком в двенадцатиперстной кишке, создавая необходимый для панкреатических ферментов диапазон рН. Участие в пищеварении и регуляции обмена – основные функции поджелудочной железы, которая является одновременно как экзокринным (секретирующим), так и эндокринным (инкретирующим) органом.
Экзокринная функция поджелудочной железы
Секретирующая функция поджелудочной железы подразделяется на два вида:
- • Экболическая функция — заключается в синтезе её клетками более двадцати ферментов и проферментов и выделении их в двенадцатиперстную кишку. Пищеварительные ферменты составляют более 90% белков поджелудочного сока и участвуют в расщеплении пищи в кишечнике.
- • Гидрокинетическая функция — состоит в выработке воды, бикарбонатов и других электролитов. Данная функция влияет на нейтрализацию содержимого желудка, создавая в кишечнике щелочную среду, благоприятную для деятельности панкреатических и кишечных ферментов.
Ферменты поджелудочной железы
Существует несколько видов панкреатических ферментов:
- • Амилолитические ферменты (амилазы) расщепляют сложные углеводы до декстринов, мальтозы, мальтоолигосахаридов и глюкозы.
- • Липолитические ферменты (липазы) расщепляют жиры до жирных кислот и моноглицеридов, проходящих через мембрану энтероцита.
- • Протеолитические ферменты (протеазы) расщепляют белки, разрывая внутренние связи в середине аминокислотных цепей и синтезируя пептиды.
- • Нуклеолитические ферменты (нуклеазы) расщепляют нуклеиновые кислоты. Фосфодиэстеразы, присутствующие в панкреатическом соке, подразделяются на две группы: рибонуклеаза расщепляет рибонуклеиновую кислоту, а дезоксирибонуклеаза гидролизирует дезоксирибонуклеиновую кислоту.
Секреция поджелудочной железы
Количество и качественный состав употребленной пищи прямо пропорциональны количеству выделяемого панкреатического сока и его ферментативной активности. Увеличение секреции поджелудочного сока вызывает большой объем пищи, которая стимулирует повышение кислотности в желудке. Прием жидкой пищи вызывает более быструю секрецию поджелудочной железы, чем медленно эвакуируемая из желудка твердая, жирная пища. Продукция панкреатического сока увеличивается спустя 2-3 минуты после попадания пищи в желудок, продолжительность её составляет от 6 до 14 часов. Наибольший секреторный ответ вызывает смешанная пища. Сильными стимуляторами, воздействующими на секреторные ферменты поджелудочной железы, являются нейтральные жиры, продукты их переваривания и белки. Аминокислоты, поступающие в кишечный тракт (особенно фенилаланин, холин, метионин), влияют на резкое увеличение в крови уровня холецистокинина – гормона, отвечающего за местную стимуляцию деятельности ацинарных клеток, обладающих функцией синтеза ферментов. Преобладание в рационе питания углеводов облегчает деятельность поджелудочной железы, поэтому данная группа продуктов особенно рекомендована в диетах для пациентов, страдающих обострением хронического панкреатита. Продукты и напитки, возбуждающие аппетит (фрукты, молочные продукты, продукты, содержащие специи и пряности, маринады, соки и алкоголь), увеличивают продукцию желудочного сока, соляной кислоты, которая, в свою очередь, стимулирует начало внешней секреции поджелудочной железы.
Журнал «Здоровье ребенка» 8 (43) 2012
Поджелудочная железа, как известно, — крупнейшая и важнейшая железа пищеварительной системы и одновременно важнейшая железа внутренней секреции, принимающая участие в регуляции углеводного обмена. Она секретирует в кровь (эндокринная функция) гормоны — инсулин, глюкагон, гастрин, соматостатин, панкреатический полипептид, амилин. При этом инсулин, вырабатываемый только в этом органе, является эссенциальным для жизни вследствие его роли в обеспечении нормального обмена. С другой стороны, поджелудочная железа продуцирует секрет (экзокринная функция), важный в работе пищеварительного тракта. Содержащиеся в секрете ферменты участвуют в гидролизе всех питательных веществ. Заболевания поджелудочной железы могут приводить как к нарушениям пищеварения (изменение желудочнокишечной секреции, абсорбции, моторики), так и к метаболическим изменениям в организме.
Поджелудочная железа человека вырабатывает каждые сутки от 50 до 1500 мл сока (в зависимости от возраста), содержащего ферменты, которые играют ключевую роль в переваривании питательных веществ. Доля дигестивных ферментов из слюнных желез (амилаза), желудка (пепсин), кишечного эпителия (протеазы) сравнительно мала. Панкреатические ферменты расщепляют белки, жиры, углеводы до мелких молекул, которые в дальнейшем либо расщепляются интестинальными мембранными ферментами на отдельные молекулы, либо могут проникать через кишечную слизистую оболочку (дипептиды, моноглицериды). Бикарбонаты, которыми богат панкреатический сок, обеспечивают реакцию среды, необходимую для активации энзимов и оптимума их действия [1, 5].
Преобладающая часть секрета (водноэлектролитная) образуется в центроацинарных клетках, эпителии вставочных протоков и ходов, меньшая часть (ферментная) — в ацинарных клетках. При всех условиях панкреатический секрет, поступающий в двенадцатиперстную кишку, изотоничен плазме крови. Состав электролитов в нем непостоянный, особенно варьирует содержание анионов.
За 24 часа поджелудочная железа человека синтезирует около 15–20 г ферментного белка, т.е. по синтетической способности она превосходит многие органы. Выход ферментов из ацинарных клеток происходит спонтанно (базальный холинергический тонус), но главным образом в результате стимуляции. Экзоцитоз из клеток независим от ферментного синтеза [1, 4]. В целостном организме прямая регуляция продукции и высвобождения ацинарными клетками белка осуществляется секретогенами: ацетилхолином, панкреозимином и секретином. Слабым стимулятором является гастрин. Ацинарные клетки синтезируют и секретируют комплекс мощных дигестивных ферментов: aамилазу для расщепления крахмала, липолитические ферменты для переваривания жиров, протеолитические — для расщепления протеинов, нуклеазы для гидролиза нуклеотидов. В небольшом количестве в панкреатическом соке находятся неферментные белки [3].
Все протеолитические ферменты поступают в сок в неактивной форме, что является самозащитой железы от переваривания. Активация проферментов происходит в двенадцатиперстной кишке. В ее просвете под действием энтерокиназы, вырабатываемой слизистой оболочкой, в присутствии ионов кальция трипсиноген превращается в трипсин и запускается каскадный феномен активации трипсином других молекул трипсиногена и остальных протеолитических ферментов.
Среди протеолитических ферментов различают эндопептидазы, расщепляющие пептидные связи внутри молекул белка и полипептидов, — трипсин, химотрипсин, эластазу — и экзопептидазы, отщепляющие аминокислоты, находящиеся на Стерминальном конце полипептидов и протеинов, — карбоксипептидазу [3, 5].
У человека 19 % протеинов панкреатического сока приходится на трипсиноген I и II, различающиеся по молекулярной массе. Каталитические свойства обоих ферментов сходны, оптимум их действия — при рН 8. Трипсин расщепляет почти все денатурированные белки, не действуя при этом на живые ткани.
Химотрипсин у человека существует в виде двух молекулярных форм: А и В. Фермент в активной форме выводится с калом. Определение активности химотрипсина в кале имеет диагностическое значение для оценки функции поджелудочной железы.
С помощью электрофореза доказано существование двух форм проэластазы. Эластаза участвует в переваривании эластина, денатурированных белков. Она отличается стабильностью в широком диапазоне — рН 4–10,5.
Карбоксипептидазы А и В имеют большую молекулярную массу, чем остальные протеолитические ферменты. Карбоксипептидаза вызывает деградацию протеинов и полипептидов.
В панкреатическом соке содержится ингибитор трипсина. На его долю приходится 0,3–0,6 % от всех протеинов. Ингибитор трипсина существует в виде нескольких хроматографических форм. Из всех охарактеризованных панкреатических ферментов он имеет минимальную молекулярную массу. Ингибирующее действие его осуществляется при рН 5,5–11.
В панкреатическом соке 10 % всего белка приходится на aамилазу. Это гликопротеин, расщепляющий внутри молекулы крахмала a1,4гликозидную связь с образованием декстрина, мальтотетраозы, мальтотриозы и мальтозы. У человека имеется 6 изоферментов панкреатической амилазы, отличимых при помощи электрофореза. Оптимум рН находится в пределах 6–7. Определение активности амилазы в моче было первым энзимологическим исследованием в медицине, проведенным J. Wohlgemuth в 1908 г. Определение активности aамилазы в моче, сыворотке крови и экссудатах и в настоящее время используется как тестмаркер (хотя и неспецифический) при воспалении железы [2].
Липолитические ферменты, секретируемые поджелудочной железой, — это липаза, колипаза, фосфолипаза, карбоксилэстергидролаза. На долю липазы приходится 1–3 % всех протеинов панкреатического сока. Липаза — гликопротеин, представленный двумя изоферментами. Панкреатическая липаза действует на поверхности тонких жировых капель. Под ее влиянием триглицериды гидролизуются до 1,2диглицеридов и затем 2моноглицеридов с высвобождением жирных кислот. Эмульгированию жиров до мелких капель способствуют желчные кислоты, но, в свою очередь, они тормозят активность фермента. Восстанавливает ее колипаза, мелкий протеин (молекулярная масса менее 11 000), действующий только вместе с липазой. Для полного действия липазы на поверхности тонких эмульгированных жировых капель образуется комплекс из 1 молекулы липазы, 1 молекулы колипазы и 1 — мицеллы [1, 2, 5].
Фосфолипаза А находится в панкреатическом соке в неактивной форме. Профермент активизируется трипсином в двенадцатиперстной кишке. Преждевременному активированию ее в поджелудочной железе отводится особая роль в патогенезе острого панкреатита.
Карбоксилэстергидролаза — неспецифически действующая эстераза, наличие которой в панкреатическом соке человека доказано. Она расщепляет водорастворимые карбоксилэстеры, например холестерин. Имеет наибольшую молекулярную массу из всех охарактеризованных энзимов (100 000–300 000). Желчные кислоты активируют энзим.
Секреторный цикл ацинарных клеток включает шесть стадий: синтез, сегрегацию, внутриклеточный транспорт, концентрирование ферментного материала, депонирование и экзоцитоз. Главным фактором, вызывающим выделение профермента из клетки, является холецистокинин. Вместе с предшественниками ферментов в дольки поджелудочной железы выделяется раствор электролитов. Образуется первичный секрет. Электролитный состав его меняется по мере прохождения протоков (особенно во внутридольковых протоках) за счет прежде всего обмена в них Cl– на HCO3–, в результате чего образуется вторичный панкреатический сок, поступающий в двенадцатиперстную кишку [3].
Доказано наличие феномена адаптации панкреатических ферментов к характеру употребляемой пищи. Речь идет о феномене приспособления не к однократно использованной пищи, а к особенностям питания вообще. Изменение ферментообразования в соответствии с характером употребляемой пищи происходит в течение нескольких дней. При адаптации наблюдается увеличение синтеза, а не активация имеющихся ферментных молекул [4].
Предполагается существование механизма обратной связи между двенадцатиперстной кишкой и поджелудочной железой. Полагают, что трипсин в двенадцатиперстной кишке тормозит высвобождение панкреозимина, а его отсутствие — стимулирует [6].
У детей протеолитическая активность пищеварительного сока поджелудочной железы находится на довольно высоком уровне уже с первых месяцев жизни, достигая максимума к 4–6 годам. Липолитическая активность увеличивается в течение первого года жизни ребенка. Активность поджелудочной амилазы к концу первого года жизни возрастает в 4 раза, достигая максимальных значений к 9 годам. При естественном вскармливании концентрация панкреатических ферментов в дуоденальном соке низкая, при смешанном — увеличивается в 1,5–2 раза, а при искусственном — в 4–5 раз [4].
В соответствии с двумя главными функциями панкреатического сока — нейтрализацией поступающего в двенадцатиперстную кишку желудочного содержимого и перевариванием нутриентов — секреция одного компонента (жидкости и бикарбонатов) определяется главным образом количеством находящейся в нем кислоты, а другого (энзимного) — присутствием в нем продуктов переваривания жира и белка. Реакция поджелудочной железы на еду представляет интегрированный ответ на нервное и гуморальное раздражение. Выделяют мозговую, желудочную и кишечную фазу панкреатической секреции.
Еще И.П. Павлов в 1896 г. в опытах с мнимым кормлением собак обнаружил, что вид и психическая подготовка к еде стимулируют панкреатическую секрецию. У людей также доказано существование мозговой фазы секреции. Это условные и безусловные рефлексы, которые передаются через блуждающий нерв. Прием пищи, которая пережевывается, но не проглатывается, у человека вызывает сильную секрецию ферментов и выраженную секрецию бикарбонатов [5].
В мозговую фазу секреции, помимо прямого воздействия на железу, путем вагусного же влияния высвобождается гастрин. Этот пептид является агонистом панкреозимина в воздействии на ферментную панкреатическую секрецию. С другой стороны, индуцированная им уже в эту фазу секреция кислоты при последующем поступлении в двенадцатиперстную кишку и высвобождении секретина (переход в кишечную фазу) стимулирует выделение бикарбонатов протоковыми клетками.
С поступлением кислоты и пищевой кашицы в двенадцатиперстную кишку начинается интестинальная фаза панкреатической секреции. Как количество, так и продолжительность поступления желудочного содержимого в тонкую кишку существенно детерминируют дальнейшую стимуляцию поджелудочной железы. Жиры удаляются из желудка очень медленно, углеводы — быстро, белки занимают промежуточную позицию. Стимуляция панкреатической секреции начинается с приемом пищи и поддерживается еще несколько часов (до 8 ч и более) после опорожнения желудка. На долю кишечной фазы приходится приблизительно 80 % ответа железы на прием пищи. При взаимодействии нервной и гуморальной регуляции происходит дальнейшее возбуждение панкреатической секреции. В эту фазу особенно велика роль гуморального контроля, изучение которого началось с открытия W.M. Bayliss и E.H. Starling в 1902 г. секретина. Стимулятором секреции воды и бикарбонатов является секретин, высвобождаемый эндокринными клетками дуоденальной и еюнальной слизистой оболочки при воздействии хлористоводородной кислоты. Секреция ферментного компонента вызывается панкреозимином, выделение которого стимулируется продуктами переваривания жира и белка [1, 2, 5].
Сильное возбуждение секреции ферментов вызывают пептиды (образовавшиеся уже в желудке), аминокислоты и жирные кислоты, находящиеся в тонкой кишке. Эффект осуществляется путем как высвобождения панкреозимина, главного гуморального стимулятора секреции ферментов, так и дуоденопанкреатического рефлекса, который реализуется посредством блуждающего нерва и короткой рефлекторной дуги. Количество высвобождаемого панкреозимина зависит от количества поступающих пептидов, аминокислот, жирных кислот и от величины поверхности интестинальной слизистой оболочки, вступающей с ними в контакт. Интересно, что кальций и магний в двенадцатиперстной кишке в зависимости от концентрации повышают секрецию ферментов, вероятно, путем высвобождения панкреозимина.
Ненасыщенные жирные кислоты с длинной цепью, помимо секреции ферментов, стимулируют и секрецию бикарбонатов. Желчные кислоты, необходимые как мицеллообразователи для жира, также заметно усиливают секрецию воды и бикарбонатов, вероятно, посредством высвобождения секретина. Углеводы не оказывают возбуждающего действия на секрецию.
По мере того, как нутриенты абсорбируются в тонкой кишке, панкреатическая секреция уменьшается, при большом количестве их в двенадцатиперстной и тощей кишке секреция продолжается.
Наряду с возбуждающим панкреатическую секрецию влиянием имеется и ингибирующее. Оно передается путем симпатического возбуждения и вазоконстрикции, а также путем высвобождения гормональных факторов — ингибиторов — из нижней части тонкой и ободочной кишки.
Лабораторная оценка внешнесекреторной функции поджелудочной железы, как и в целом диагностика панкреатической патологии, традиционно считается трудной задачей. В последние десятилетия, однако, проблема недостатка информации переросла в другую — проблему выбора диагностического подхода, выбора наиболее адекватных методов исследования. Диагностика заболеваний поджелудочной железы основывается на данных анамнеза и характерных клинических симптомах, оценке экзокринной и эндокринной деятельности органа и результатах инструментальных исследований, способных определить наличие структурных изменений. Все методы оценки экзокринной функции поджелудочной железы подразделяются на прямые (обычно зондовые) и косвенные (беззондовые). Прямые методы связаны с непосредственным определением активности ферментов в дуоденальном содержимом, а косвенные — с оценкой процессов переваривания стандартных субстратов.
Для диагностики, в частности, ключевого заболевания поджелудочной железы у детей — обострения хронического панкреатита — важное значение имеет определение активности панкреатических ферментов — амилазы, липазы и трипсина в крови, а также амилазы и липазы в моче. Однократного определения активности фермента может быть недостаточно, поскольку показатели амилазы и липазы в крови натощак обычно повышаются в 1,5–2 раза на короткий период времени (через 2–12 часов после обострения и достигают максимума к концу первых суток с последующим быстрым снижением и нормализацией в течение 2–4 дней). Активность амилазы в моче возрастает примерно на 6 часов позже сывороточной. В то же время повышение активности сывороточной амилазы в два раза и более в сочетании с увеличением уровня липазы и трипсина (или одного из них) является достаточно достоверным тестом обострения заболевания. Однако и нормальные показатели концентрации ферментов в крови и моче не дают основания исключить диагноз хронического панкреатита. В таких случаях применяется провокационный тест, при котором определяется активность ферментов до и после стимуляции. Наиболее широко используют определение амилазы в крови после стимуляции панкреозимином или глюкозой, а также уровня амилазы в моче на фоне стимуляции прозерином. После введения раздражителей наблюдается феномен «уклонения» ферментов (гиперферментемия), что свидетельствует о поражении ткани поджелудочной железы или препятствии для оттока панкреатического сока. Иногда провокационные тесты могут быть отрицательными (уровень ферментов не изменяется или даже снижается), что связано с уменьшением числа ацинарных клеток, продуцирующих эти ферменты при тяжелом панкреатите [2, 6].
Известно, что золотым стандартом определения внешнесекреторной функции поджелудочной железы является секретинхолецистокининовый тест. При этом панкреатический сок получают при гастродуоденальном зондировании с помощью двухканального зонда после откачивания желудочного сока и дуоденального содержимого и введения стимуляторов панкреатической секреции. С целью стимуляции секреции в/в вводят секретин 1,5 Ед/кг и через 30 минут — холецистокинин 0,5 Ед/кг. Секретинхолецистокининовый тест обладает высокой точностью, однако широкое его применение невозможно изза ряда недостатков: высокой стоимости секретина и холецистокинина, необходимости зондирования пациента, длительности процедуры, необходимости внутривенного введения препаратов и, как следствие, возможности побочных реакций [5].
К косвенным методам оценки экзокринной функции поджелудочной железы относится копрологическое исследование. Признаком внешнесекреторной недостаточности поджелудочной железы является полифекалия, когда кал сального вида, сероватого цвета, кашицеобразный, вязкий, с резким гнилостным запахом, плохо смывается со стенок унитаза. При микроскопическом исследовании могут обнаруживаться непереваренные мышечные волокна (креаторея) — признак тяжелого течения панкреатита; наличие капель нейтрального жира (стеаторея) — один из ранних симптомов панкреатической недостаточности [1].
В последние годы альтернативой достаточно инвазивному секретинхолецистокининовому тесту стало определение в кале эластазы1 методом иммуноферментного анализа. Этот фермент секретируется поджелудочной железой и не метаболизируется в кишечнике, его активность в кале объективно отражает состояние экзокринной функции органа, а органоспецифичность исключает возможность ошибки, связанной с активностью кишечных ферментов. Данный метод имеет самую большую специфичность и чувствительность — более 90 %. В отличие от других тестов определение эластазы1 можно проводить, не отменяя препараты заместительной терапии. В норме активность эластазы1 в кале — более 200 мкг/г кала. Снижение концентрации эластазы свидетельствует об экзокринной недостаточности поджелудочной железы, которая может являться симптомом муковисцидоза, острого и хронического панкреатита, травмы поджелудочной железы и некоторых других состояний [1, 5, 7–11].
Таким образом, в настоящее время в педиатрии существуют различные методы оценки экзокринной функции поджелудочной железы, как прямые, так и косвенные. Задача врача состоит в выборе наиболее адекватного метода исследования с учетом основных клинических симптомов заболевания.
Нарушения в работе поджелудочной железы
Нарушения процесса пищеварения в тонкой кишке напрямую связаны с изменением синтеза ферментов, вызванным дисфункцией поджелудочной железы. При наличии в ней патологических процессов угнетается действие липазы, гидролизирующей жиры, что ведет к их недостаточному перевариванию и выведению с калом до 80% от массы, поступившей в организм. Нарушается также расщепление белков, о чем может свидетельствовать креаторея, характерным признаком которой является наличие в каловых массах повышенного объема мышечных волокон. Недостаточность пищеварения может привести к таким негативным последствиям, как диспептический синдром, обезвоживание, нарушения кислотно-основного равновесия и кишечная аутоинтоксикация. Внешняя секреция поджелудочной железы вызывается наличием в организме ряда воспалительных заболеваний и некоторых других патологических процессов:
- панкреатиты в острой и хронической стадии;
- желчнокаменная болезнь;
- наличие в кишечнике паразитов;
- дуодениты, язва двенадцатиперстной кишки, следствием которых является уменьшение продукции панкреатического сока;
- опухоли;
- фатериты;
- избыточный вес тела, гормональный дисбаланс, являющиеся результатом нарушения обменных процессов, вызывающие поражения поджелудочной железы дистрофического характера;
- аллергическая перестройка организма;
- вагальная дистрофия, длительная атропинизация;
- опухолевые новообразования, разрушающие поджелудочную железу.
Развитие в поджелудочной железе обтурационных процессов, которые затрудняют либо полностью перекрывают отток панкреатического сока в двенадцатиперстную кишку, и возникающая вследствие данной патологии гипертензия может вызвать острую боль в этой области, а также внутренние разрывы и разрушения паренхимы органа. В результате деструкции поджелудочной железы происходит всасывание её ферментов, продуктов разрушения в кровь и окружающие органы, что ведет к развитию некрозов и формированию синдрома интоксикации организма.
Эндокринные функции
Внутрисекреторные функции поджелудочной железы не могут происходить без особых веществ – гормонов, продуцированием которых также занимается этот орган. Данная функция именуется эндокринной (внутренняя секреторная функция) и ее активизация также во многом зависит от пищи, которую ест человек в течение всего дня. Однако нужно отметить, что гормоны, которые синтезирует железа, не попадают в органы пищеварения. Их выброс производится в кровь, где и отмечается гуморальная регуляция организма на них.
Клетки, синтезирующие гормоны находятся внутри островков Лангерганса
Эндокринная функция поджелудочной железы выполняется посредством специальных клеток, численность которых не превышает 2% от всего тела органа. Эти клетки образуют скопления, которые в медицине именуются островками Лангерганса.
Существует всего 5 видов клеток, отвечающих за выработку гормонов:
Строение поджелудочной железы
- альфа-клетки – осуществляют секрецию глюкагона;
- бета-клетки – вырабатывают инсулин;
- дельта-клетки – продуцируют соматостатин;
- Д1-клетки – обеспечивают человеческий организм вазоактивными интестинальными полипептидами;
- РР-клетки – синтезируют панкреатический полипептид.
Без этих гормонов работа поджелудочной железы и обменные процессы в организме не могут происходить нормально. Ведь именно они регулируют обмен веществ, а также поддерживают работу почек, кишечника, печени и 12-перстной кишки.
Наиболее известным среди далеких от медицины людей является гормон инсулин. Его выделение в кровь обеспечивает нормализацию уровня глюкозы в крови. Он связывается с молекулами глюкозы, разбивает их на более мелкие структуры и поставляет в клетки и ткани организма, тем самым насыщая их энергией. Если работа бета-клеток нарушается, формируется недостаточность инсулина, которая приводит к увеличению концентрации микрокристалликов сахара в крови и является провокатором развития сахарного диабета и резкого снижения веса. Ведь вместо того чтобы растрачивать энергию, которую клеткам предоставил инсулин, они начинают использовать в качестве топлива жир, что приводит к дистрофии жировой ткани.
Эндокринная функция поджелудочной железы играет очень важную роль в человеческом организме. Несмотря на то что ее выполнением занимается небольшое количество клеток, без нее не могут происходить ни одни процессы в организме. Так как внутрисекреторная функция проявляется в гуморальном управлении, которое является эволюционным ранним способ управления организма. Поджелудочная синтезирует гормоны, выбрасывает их в кровь и обеспечивает гормональное равновесие. В результате этого регулируется работа всех внутренних органов и систем.