Генно-инженерная биологическая терапия (ГИБТ) при воспалительных заболеваниях кишечника (ВЗК) прочно вошла в схемы лечения пациентов с язвенным колитом (ЯК) и болезнью Крона. В последние годы пришло осознание того, что схемы лекарственной терапии необходимо оценивать не только с позиции «дорого» или «дешево», а в первую очередь с позиции соотношения затрат, клинической эффективности и безопасности. Происходит смещение парадигмы современного здравоохранения в сторону ценностно-ориентированной модели, когда при лечении конкретного больного с ВЗК фокус смещается от стоимости к результату лечения.
Неотъемлемой составляющей работы медицинской организации, в состав которой входит Центр ВЗК, является выбор ГИБТ с учетом затрат и эффективности, своевременное формирование годовых заявок согласно истинной потребности пациентов с ВЗК, состоящих на диспансерном учете, адресное обоснование назначения ГИБТ с учетом индивидуального «профиля» пациента. Понимание аспектов безопасности новых препаратов (ГИБП) в терапии ВЗК важно для достижения и поддержания клинических результатов, минимизации рисков и устранения побочных эффектов или осложнений в случае их возникновения.
Известно, что у пациентов с ВЗК имеет место повышенный риск инфекционных осложнений, включая грипп, пневмонию, опоясывающий лишай, Clostridium difficile, туберкулез и другие, по сравнению с популяцией без ВЗК. В качестве препарата с минимальным риском активации инфекции, по данным многоцентровых исследований, выступает ведолизумаб (энтивио) [1—3].
В данной статье приводится описание собственного клинического наблюдения ведения пациентки с длительным течением тотального ЯК, в анамнезе перенесшей туберкулез легких.
Описание свечей Салофальк
Данные свечи оказывают противовоспалительное действие благодаря входящему в их состав активному веществу под названием месалазин. При этом лекарство Салофальк выпускается не только в форме суппозиториев, но и в виде таблеток, гранул и клизмы.
Лекарственную форму выбирает лечащий врач в зависимости от протяженности и локализации поражения кишечника.
Например, при язвенном неспецифическом колите пациентам назначают Салофальк в таблетках, при проктите и проктосигмоидите — в форме свечей и клизм. Иногда рекомендуют комбинировать суппозитории вместе с таблетками.
Свечи Салофальк назначают при:
- болезни Крона
- язвенном колите
- дивертикулите
Также они могут использоваться в качестве профилактики рака толстой кишки у людей, которые склонны к этому заболеванию.
Однако существует ряд противопоказаний, при которых придется поискать аналог Салофалька с другим активным веществом.
Среди них:
- высокая чувствительность к салициловой кислоте
- нарушения в работе почек и печени
- язвенная болезнь желудка и 12-перстной кишки в острой форме
- возраст до 2 лет
Как видим, самостоятельность использовать препарат нельзя. К тому же, в аптеках он продается только по рецепту.
Инструкция по применению САЛОФАЛЬК® (SALOFALK®) таблетки
Общие свойства месалазина
Всасывание
Месалазин всасывается наиболее эффективно в проксимальных отделах и наименее эффективно в дистальных отделах кишечника.
Распределение
Связывание с белками плазмы месалазина и N-Aц-5-АСК составляет соответственно 43% и 78%. Приблизительно 1% дозы месалазина, принятой внутрь, выделяется с грудным молоком, в основном в виде N-Aц-5-АСК.
Метаболизм
Месалазин подвергается пресистемному метаболизму с образованием неактивной N-ацетил-5-аминосалициловой кислоты (N-Ац-5-АСК), как в слизистой оболочке кишечника, так и в печени. Характер ацетилирования не зависит от фенотипа ацетилирования пациента. Часть месалазина также ацетилируется за счет действия бактериальной микрофлоры толстого кишечника.
Выведение
Месалазин и его метаболит N-Aц-5-АСК выделяются с экскрементами (большая часть), почками (количество варьирует от 20% до 50% в зависимости от пути введения, лекарственной формы и механизма высвобождения действующего вещества) и с желчью (меньшая часть). Почками выводится в основном в виде N-Aц-5-АСК.
Специфические особенности препарата Салофальк® в форме таблеток 250 мг
Распределение
Комбинированное фармакосцинтиграфическое/фармакокинетическое исследование продемонстрировало, что при приеме с пищей (пробный завтрак) таблетки, покрытые кишечнорастворимой пленочной оболочкой, растворяются приблизительно через 3-4 ч в подвздошной кишке. Среднее время эвакуации желудочного содержимого составило приблизительно 3 ч. После приблизительно 7 ч таблетки достигли толстой кишки. В последующем исследовании с участием добровольцев время эвакуации из двенадцатиперстной кишки в подвздошную составило приблизительно 3 ч, причем наивысшая концентрация 5-АСК в просвете кишечника была зафиксирована через 7-8 ч после совместного приема таблеток с пробным завтраком. Приблизительно 75% дозы месалазина достигает толстого кишечника в неметаболизированном виде.
Всасывание
Высвобождение месалазина из препарата Салофальк® таблетки 250 мг, покрытые кишечнорастворимой пленочной оболочкой, начинается после лаг-фазы длительностью приблизительно 3-4 ч. Наивысшая концентрация в плазме крови достигается приблизительно через 5 ч (в области подвздошной кишки) и при введении месалазина в дозе 500 мг 3 раза/сут (3×2 таб. Салофальк® 250 мг) при условии установившегося равновесия составляет 2.1±1.7 мкг/мл для месалазина и 2.8±1.7 мкг/мл для его метаболита, N-A4-5-ACK.
Выведение
При длительном лечении с использованием препарата Салофальк® таблетки 250 мг, покрытые кишечнорастворимой пленочной оболочкой, в суточной дозе 500 мг месалазина 3 раза/сут (при условии установившегося равновесия) суммарная скорость выведения почками месалазина и N-A4-5-ACK составила приблизительно 55% (значение, полученное в течение 24 ч после введения последней дозы). Доля неметаболизированного месалазина составила приблизительно 5%. Т1/2 составляет 0.7-2.4 ч (в среднем 1.4±0.6 ч.) при применении месалазина в дозе 500 мг 3 раза/сут.
Специфические особенности препарата Салофальк® в форме таблеток 500 мг
Распределение
Комбинированное фармакосцинтиграфическое/фармакокинетическое исследование продемонстрировало, что при приеме с пищей (пробный завтрак) таблетки, покрытые кишечнорастворимой пленочной оболочкой, растворяются приблизительно через 3-4 ч в подвздошной кишке. Приблизительно после 4-5 ч таблетки достигают толстой кишки. Общее время транзита в толстом кишечнике составляет около 17 ч.
Всасывание
Высвобождение месалазина из препарата Салофальк® таблетки 500 мг, покрытые кишечнорастворимой пленочной оболочкой, начинается после лаг-фазы длительностью приблизительно 3-4 ч. Наивысшая концентрация в плазме крови достигается через приблизительно 5 ч (в области подвздошной кишки) и при введении месалазина в дозе 500 мг 3 раза/сут при условии установившегося равновесия составляет 3±1.6 мкг/мл для месалазина и 3.4±1.6 мкг/мл для его метаболита, N-Ац-5-АСК.
Выведение
Суммарная скорость выведения почками месалазина и N-Ац-5-АСК в течение 24 ч при многократном приеме (1 таб. 500 мг 3 раза /сут, в течение 2 дней; и 1 таб. на третий контрольный день) составила приблизительно 60% (значение, полученное в течение 24 ч после введения последней дозы). Доля неметаболизированного месалазина составляла приблизительно 10%.
Причины и симптомы язвенного колита
Под язвенным колитом понимается хроническое заболевание, при котором поражается слизистая оболочка толстой кишки. При этом она отекает, воспаляется, на ней образуются язвы.
Если говорить о причинах возникновения язвенного колита, то ученые выдвигают ряд теорий. Некоторые склоняются к тому, что язвенный колит является инфекционным заболеванием, но возбудитель еще не установлен.
Другие медики считают, что данная болезнь выступает аутоиммунной, то есть иммунная система человека вырабатывает антитела, уничтожающие слизистую оболочку толстой кишки. И, конечно же, нельзя забывать о генетическом факторе.
Предрасполагающие факторы:
- соблюдение диеты, бедной на белки, но богатой на углеводы
- дисбактериоз
- стресс
- пассивный образ жизни
По статистике, люди, которым удалили аппендицит, язвенным колитом страдают намного реже. С чем это связано, никто не знает.
Язвенный колит у каждого пациента протекает по-разному, однако из общих симптомов можно выделить: недомогание, повышение температуры, слабость, схваткообразные боли в животе, частый стул (до 5-ти раз в сутки). В кале может быть примесь крови.
Как видим, медлить с обращением к врачу, используя народные средства, не стоит. Это чревато серьезными осложнениями, которые намного сложнее вылечить.
ЯЗВЕННЫЙ КОЛИТ: ФАРМАЦЕВТИЧЕСКИЕ АСПЕКТЫ
Т. Л. Михайлова, О. В. Головенко Государственный научный центр колопроктологии МЗ РФ Москва
Язвенный колит (ЯК) — это хроническое рецидивирующее заболевание толстой кишки неизвестной этиологии, характеризующееся геморрагически-гнойным воспалением толстой кишки с развитием местных и системных осложнений.
Точные данные о распространенности ЯК получить трудно, так как легкие случаи ЯК, особенно в начальном периоде заболевания, часто остаются неучтенными. Пациенты в этих случаях, как правило, наблюдаются в неспециализированных амбулаторных учреждениях и трудно поддаются учету.
Эпидемиология. ЯК наиболее широко распространен в урбанизированных странах, в частности в Европе и Северной Америке. В этих регионах частота возникновения ЯК (первичная заболеваемость) колеблется от 4 до 20 случаев на 100 000 человек, составляя при этом в среднем 8-10 случаев в год. Распространенность ЯК (численность больных) составляет 40 — 117 больных на 100 000 жителей. Наибольшее число случаев приходится на возраст 20 — 40 лет. Второй пик заболеваемости отмечается в старшей возрастной группе — после 55 лет. Наивысшие показатели смертности отмечаются в течение первого года болезни вследствие случаев крайне тяжелого молниеносного течения заболевания и через 10 лет после его начала из-за развития у ряда пациентов колоректального рака.
Остается неясной роль факторов окружающей среды, в частности курения. В многочисленных эпидемиологических исследованиях показано, что ЯК чаще встречается у некурящих. Это даже позволило предложить никотин в качестве лечебного средства. Люди, перенесшие аппендэктомию, имеют меньший риск заболеть ЯК, также как лица, подвергающиеся чрезмерным физическим нагрузкам. По сравнению со здоровыми лицами рацион пациентов, страдающих ЯК, содержит меньше пищевых волокон и больше углеводов. В анамнезе пациентов ЯК чаще, чем в общей популяции, наблюдаются случаи детских инфекционных заболеваний.
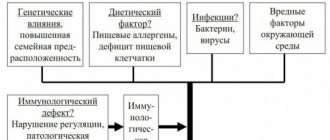
Этиология. Точная этиология ЯК к настоящему времени неизвестна. Обсуждаются три основных концепции:
— заболевание вызывается непосредственным воздействием некоторых экзогенных факторов окружающей среды, которые пока не установлены. В качестве основной причины рассматривается инфекция;
— ЯК является аутоиммунным заболеванием. При наличии генетической предрасположенности организма воздействие одного или нескольких “пусковых” ( триггерных ) факторов запускает каскад механизмов, направленных против собственных антигенов. Аналогичная модель характерна для других аутоиммунных заболеваний;
— ЯК — это заболевание, обусловленное дисбалансом иммунной системы желудочно-кишечного тракта. На этом фоне воздействие разнообразных неблагоприятных факторов приводит к чрезмерному воспалительному ответу, который возникает из-за наследственных или приобретенных нарушений в механизмах регуляции иммунной системы.
Патогенез. В развитии воспаления при ЯК задействованы многочисленные механизмы тканевого и клеточного повреждения. Бактериальные и тканевые антигены вызывают стимуляцию Т- и В- лимфоцитов. При обострении ЯК обнаруживается дефицит иммуноглобулинов, что способствует проникновению микробов, компенсаторной стимуляции В-клеток с образованием иммуноглобулинов M и G. Дефицит Т- супрессоров приводит к усилению аутоиммунной реакции . Усиленный синтез иммуноглобулинов M и G сопровождается образованием иммунных комплексов и активацией системы комплемента, который обладает цитотоксическим действием, стимулирует хемотаксис нейтрофилов и фагоцитов с последующим выделением медиаторов воспаления, которые и вызывают деструкцию эпителиальных клеток. Среди медиаторов воспаления прежде всего следует назвать цитокины IL-1b , IF-g , IL-2, IL-4, IL-15, которые влияют на рост , движение, дифференциацию и эффекторные функции многочисленных клеточных типов, вовлеченных в патологический процесс при ЯК. Помимо патологических иммунных реакций, повреждающее действие на ткани оказывают активный кислород и протеазы; отмечается изменение апоптоза, то есть механизма клеточной смерти.
Важная роль в патогенезе ЯК отводится нарушению барьерной функции слизистой оболочки кишечника и ее способности к восстановлению. Считается, что через дефекты слизистой в более глубокие ткани кишки могут проникать разнообразные пищевые и бактериальные агенты, которые затем запускают каскад воспалительных и иммунных реакций.
Большое значение в патогенезе ЯК и провокации рецидива заболевания имеют особенности личности больного и психогенные влияния. Индивидуальная реакция на стресс с аномальным нейрогуморальным ответом может явиться пусковым механизмом развития болезни. В нервно-психическом статусе больного ЯК отмечаются особенности, которые выражаются в эмоциональной нестабильности.
Клиника. Современная клиническая классификация ЯК учитывает распространенность процесса, выраженность клинических проявлений, характер рецидивирования.
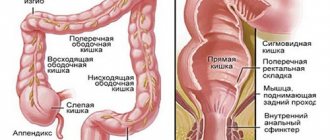
По протяженности процесса различают:
— дистальный колит ( в виде проктита или проктосигмоидита);
— левосторонний колит (поражение ободочной кишки до правого изгиба);
— тотальный колит ( поражение всей ободочной кишки с вовлечением в патологический процесс в ряде случаев терминального отрезка подвздошной кишки).
По тяжести клинических проявлений различают легкое течение заболевания, средней тяжести и тяжелое.
По характеру рецидивирования могут быть:
— острая форма язвенного колита (первая атака);
— молниеносная форма (как правило, с летальным исходом);
— хроническая рецидивирующая форма (с повторяющимися обострениями, чаще сезонного характера);
— непрерывная форма заболевания (затянувшееся обострение более 6 месяцев при условии адекватного лечения).
Отмечается корреляция между протяженностью поражения и степенью выраженностии симптоматики, что, в свою очередь, определяет объем и характер лечения.
Диагноз ЯК формулируется с учетом характера течения (рецидивирования) заболевания, распространенности процесса ( дистальный, левосторонний, тотальный колит), степени тяжести заболевания ( легкое, средней тяжести, тяжелое), фазы болезни (обострение, ремиссия) с указанием местных и системных осложнений. Например: неспецифический язвенный колит, тотальное поражение, хроническое рецидивирующее течение, средней степени тяжести.
К моменту установления диагноза приблизительно у 20 % пациентов выявляется тотальный колит, у 30 — 40 % — левостороннее поражение и у 40 — 50 % — проктит или проктосигмоидит.
Для клинической картины ЯК характерны местные симптомы (кишечные кровотечения, диарея, запор, боли в животе, тенезмы) и общие проявления токсемии (лихорадка, снижение массы тела, тошнота, рвота, слабость и др.). Интенсивность симптомов при ЯК коррелирует с протяженностью патологического процесса по кишке и тяжестью воспалительных изменений.
Для тяжелого тотального поражения толстой кишки характерны профузная диарея с примесью значительного количества крови в каловых массах, иногда выделение крови сгустками, схваткообразная боль в животе перед актом дефекации, анемия, симптомы интоксикации (лихорадка, уменьшение массы тела, выраженная общая слабость). При этом варианте ЯК могут развиваться осложнения, угрожающие жизни, — токсический мегаколон, перфорация толстой кишки и массивное кишечное кровотечение. Особенно неблагоприятное течение ЯК наблюдается у больных с молниеносной формой ЯК. Летальность при тяжелой форме ЯК в течение первых 5 лет достигает 40 % и половина этих случаев приходится на период первой атаки.
При обострении средней тяжести отмечается учащенный стул до 5 — 6 раз в сутки с постоянной примесью крови, схваткообразные боли в животе, субфебрильная температура, быстрая утомляемость. У ряда больных наблюдаются внекишечные симптомы — артрит, узловатая эритема, увеит и др. Среднетяжелые атаки ЯК в большинстве случаев успешно поддаются консервативной терапии современными противовоспалительными средствами, в первую очередь кортикостероидами.
Тяжелые и среднетяжелые обострения ЯК характерны для тотального и в ряде случаев левостороннего поражения толстой кишки. Легкие атаки ЯК при тотальном поражении проявляются незначительным учащением стула и незначительной примесью крови в кале.
В клинической картине больных проктитом и проктосигмоидитом очень часто манифестирует не диарея , а запор и ложные позывы к дефекации с выделением свежей крови, слизи и гноя, тенезмы. Если через воспаленные дистальные отделы толстой кишки транзит кишечного содержимого ускорен, то в проксимальных сегментах наблюдается стаз. С этим патофизиологическим механизмом связывают запор при дистальном колите. Пациенты могут длительное время не замечать примесь крови в кале; общее состояние ухудшается малозаметно, трудоспособность сохраняется. Этот латентный период с момента возникновения ЯК до установления диагноза может быть очень длительным — иногда до нескольких лет.
Осложнения ЯК. При ЯК наблюдается большое число разнообразных осложнений. Их можно условно разделить на две категории — местные и системные.
Местные осложнения включают перфорацию толстой кишки, острую токсическую дилатацию толстой кишки ( или токсический мегаколон ), массивные кишечные кровотечения, рак толстой кишки.
Острая токсическая дилатация толстой кишки — одно из самых опасных осложнений ЯК. Она развивается вследствие тяжелого язвенно-некротического процесса и связанного с ним токсикоза. Токсическая дилатация характеризуется расширением сегмента или всей пораженной кишки во время тяжелой атаки ЯК. Больные с токсической дилатацией толстой кишки на начальных стадиях нуждаются в интенсивной консервативной терапии. При ее неэффективности выполняется оперативное вмешательство.
Перфорация толстой кишки является наиболее частой причиной смерти при молниеносной форме ЯК, особенно при развитии острой токсической дилатации. Вследствие обширного язвенно-некротического процесса стенка толстой кишки истончается, теряет свои барьерные функции и становится проницаемой для разнообразных токсических продуктов, находящихся в просвете кишки. Помимо растяжения кишечной стенки, решающую роль в возникновении перфорации играют нарушения микроциркуляции и пролиферация бактериальной флоры, особенно кишечной палочки с патогенными свойствами. В хронической стадии заболевания данное осложнение встречается редко и протекает в основном в форме периколитического абсцесса. Лечение перфорации — только хирургическое.
Массивные кишечные кровотечения встречаются сравнительно редко и как осложнение представляют собой менее сложную проблему, чем острая токсическая дилатация толстой кишки и перфорация. У большинства больных с кровотечением адекватная противовоспалительная и гемостатическая терапия позволяют избежать операции. При продолжающихся массивных кишечных кровотечениях у больных ЯК показано хирургическое вмешательство.
Риск развития рака толстой кишки при ЯК резко возрастает при длительности заболевания свыше 10 лет, если колит начался в возрасте моложе 18 лет и особенно 10 лет.
Системные осложнения при ЯК иначе называют внекишечными проявлениями. У больных могут встречаться поражения печени, слизистой оболочки полости рта, кожи, суставов. Точный генез внекишечных проявлений до конца не изучен. В их формировании участвуют чужеродные, том числе токсические агенты, поступающие в организм из просвета кишки, и имунные механизмы. Узловатая эритема встречается не только как реакция на прием сульфасалазина ( связана с сульфапиридином ), но наблюдается у 2 — 4 % пациентов с ЯК или БК и вне связи с приемом препарата. Гангренозная пиодермия достаточно редкое осложнение и отмечается у 1 — 2 % пациентов. Эписклерит встречается у 5 — 8 % больных с обострением ЯК; острая артропатия — у 10 — 15 %. Артропатия проявляется ассиметричным поражением крупных суставов. Анкилозирующий спондилит выявляется у 1 — 2 % пациентов. Поражения печени, по нашим данным, наблюдаются у 33,3 % больных ЯК и БК, проявляясь у большинства либо транзиторным повышением уровня трансаминаз в крови, либо гепатомегалией. Самым характерным серьезным гепатобилиарным заболеванием при ЯК является первичный склерозирующий холангит, представляющий собой хроническое стенозирующее воспаление внутри- и внепеченочных желчных протоков. Он встречается у приблизительно у 3% больных ЯК.
Лечение. Лечебная тактика при ЯК определяется локализацией патологического процесса в толстой кишке, его протяженностью, тяжестью атаки, наличием местных и/или системных осложнений. Консервативная терапия ЯК направлена на наиболее быстрое купирование атаки, предупреждение рецидива заболевания и прогрессирования процесса. Дистальные формы ЯК — проктит или проктосигмоидит — характеризуются более легким течением, поэтому чаще всего лечатся амбулаторно. Больные с левосторонним и тотальным поражением, как правило, лечатся в стационаре, так как течение заболевания у них отличается большей выраженностью клинической симптоматики и большими органическими изменениями.
Пища больных должна быть калорийной и включать продукты, богатые белками, витаминами, с ограничением жиров животного происхождения и исключением грубой растительной клетчатки. Рекомендуются нежирные сорта рыбы, мясо (говядина, курица, индейка, кролик ), приготовленные в отварном виде или на пару, протертые каши, картофель, яйца, подсушенный хлеб, грецкие орехи. Исключаются из рациона сырые овощи и фрукты, поскольку они способствуют развитию диареи. Нередко у больных отмечается лактазная недостаточность, поэтому молочные продукты добавляют лишь при их хорошей переносимости. Эти рекомендации соответствуют диетам 4, 4Б, 4В Института питания РАМН.
Все лекарственные препараты, используемые в схемах лечения ЯК, можно условно разделить на две большие группы. Первая объединяет базисные противовоспалительные препараты и включает в себя аминосалицилаты, то есть препараты, содержащие 5-аминосалициловую кислоту (5-АСК, месалазин), кортикостероиды и иммунодепрессанты. Все другие препараты играют либо вспомогательную роль в терапии ЯК, либо находятся на стадии клинического изучения.
Первым препаратом, содержащим в своем составе 5-АСК, был сульфасалазин (салазосульфапиридин), который был внедрен в клиническую практику в 1942 г. Сульфасалазин состоит из двух компонентов, связанных между собой азотной связью — сульфаниламида сульфапиридина и 5-АСК. Доказано, что противовоспалительным действием обладает только 5-АСК. Сульфапиридин был вынужденно включен в состав молекулы сульфасалазина, так как “чистая” 5-АСК хорошо всасывается в тонкой кишке, а в слизистой оболочке превращается в неактивный метаболит — N-ацетил — 5 -АСК. Сульфапиридин выступает в сульфасалазине исключительно в роли “носителя”, который позволяет доставить 5-АСК к пораженным участкам толстой кишки. Под воздействием толстокишечной микрофлоры азотная связь разрушается. Cульфапиридин всасывается в толстой кишке, подвергается в печени детоксикации посредством ацетилирования и выделяется с мочой, а 5-АСК, контактируя со слизистой оболочкой, оказывает противовоспалительное действие.
Механизмы, благодаря которым 5-АСК оказывает противовоспалительное действие, до конца не изучены. Тем не менее известны многочисленные эффекты, благодаря которым месалазин тормозит развитие воспаления. Так, посредством ингибирования циклооксигеназы месалазин тормозит образование простагландинов. Подавляется также липооксигеназный путь метаболизма арахидоновой кислоты, тормозится освобождение лейкотриена В4 и сульфопептида лейкотриенов.
В высоких концентрациях месалазин может ингибировать определенные функции нейтрофильных гранулоцитов у человека ( например, миграцию, дегрануляцию, фагоцитоз и образование свободных токсичных кислородных радикалов). Кроме того, месалазин тормозит синтез фактора, активирующего тромбоциты (ФАГ). Благодаря своим антиоксидантным свойствам месалазин оказывается способным улавливать свободные кислородные радикалы.
Месалазин эффективно тормозит образование цитокинов — интерлейкина-1 и интерлейкина-6 (ИЛ-1, ИЛ-6) в слизистой оболочке кишечника, а также подавляет образование рецепторов интерлейкина-2. Тем самым месалазин вмешивается непосредственно в течение иммунных процессов.
Было показано, что “балластный” компонент сульфапиридин является в основном ответственным за всю частоту побочных эффектов сульфасалазина. Данные литературы о частоте побочных эффектов, вызываемых сульфасалазином, колеблются от 5 до 55 %, составляя в среднем 21%. Кроме тошноты, головной боли, мужского бесплодия встречаются анорексия, диспепсические расстройства, гематологические реакции ( лейкопения и гемолитическая анемия ) и реакции гиперчувствительности с полиорганными поражениями.
Для того чтобы сохранить противовоспалительную активность, присущую сульфасалазину, и в то же время избежать побочных эффектов, связанных с сульфапиридиновым компонентом, в последние годы были разработаны препараты, содержащие “чистую” 5-АСК. В качестве примера нового поколения аминосалицилатов можно привести препарат Салофальк, разработанный немецкой фармацевтической фирмой “Доктор Фальк Фарма”. Препарат выпускается в трех лекарственных формах — таблетках, суппозиториях и микроклизмах. В таблетках месалазин защищен от контакта с желудочным содержимым с помощью специальной кислотоустойчивой полимерной оболочки, которая растворяется при показателях Рн свыше 6.5. Именно такие значения Рн, как правило, регистрируются в просвете подвздошной кишки. После растворения оболочки в подвздошной и толстой кишках создается высокая концентрация активного противовоспалительного компонента (месалазина ). Выбор конкретной лекарственной формы Салофалька определяется протяженностью зоны воспаления в толстой кишке. При проктите целесообразно применение суппозиториев, при левостороннем поражении — микроклизм, а при тотальном колите — таблеток.
Суточная доза аминосалицилатов определяется тяжестью атаки ЯК и характером клинического ответа на прием препарата. Для купирования острой и среднетяжелой атаки ЯК обычно назначают 3 — 4 г сульфасалазина или 1,5 — 2 г месалазина сутки, разделенных на 3 — 4 приема. При отсутствии хорошего клинического ответа суточная доза месалазина может быть удвоена, однако увеличить суточную дозу сульфасалазина свыше 4 г обычно не удается из-за развития выраженных побочных эффектов.
Сульфасалазин блокирует конъюгацию фолиевой кислоты в щеточной кайме тощей кишки, тормозит транспорт этого витамина, угнетает активность связанных с ним ферментативных систем в печени. Поэтому в лечебный комплекс больных ЯК, получающих лечение сульфасалазином, необходимо включать фолиевую кислоту в дозе 0,002 х 3 раза в сутки.
Для купирования атаки ЯК обычно требуется 3 — 6 недель. После этого проводится противорецидивное лечение сульфасалазином — 2 г в сутки или месалазином – 1,5 г в сутки.
Из современных препаратов для лечения проктосигмоидита и левостороннего колита чаще всего применяется суспензия Салофалька. В одноразовых резервуарах содержится соответственно 4 г месалазина в 60 мл суспензии или 2 г месалазина в 30 мл суспензии. Препарат вводится в прямую кишку 1 — 2 раза в сутки. Суточная доза составляет 2 — 4 г в зависимости от тяжести процесса в кишке. Если протяженность воспалительного процесса в прямой кишке не более 12 от края ануса, целесообразно применение свечей Салофалька. Обычная суточная доза в этих случаях – 1,5 — 2 г.
При использовании аминосалицилатов удается добиться ремиссии в 75 — 80 % случаев ЯК.
Наиболее эффективными противовоспалительными средствами в лечении ЯК остаются стероидные гормоны, которые при тяжелых формах заболевания превосходят по активности аминосалицилаты. Кортикостероиды накапливаются в воспалительной ткани и блокируют освобождение арахидоновой кислоты, предотвращая образование простагландинов и лейкотриенов, обуславливающих воспалительный процесс. Блокируя хемотаксис, стероидные гормоны опосредованно проявляют иммуномодулирующее действие. Влияние на тканевой фибринолиз приводит к уменьшению кровоточивости.
Показанием для проведения стероидной терапии являются:
— острые тяжелые и среднетяжелые формы заболевания и наличие внекишечных осложнений;
— левосторонние и тотальные формы язвенного колита с тяжелым и среднетяжелым течением при наличии III степени активности воспалительных изменений в кишке (по данным эндоскопического исследования);
— отсутствие эффекта от других методов лечения при хронических формах ЯК.
В таблице приводится схема лечения ЯК в зависимости от тяжести заболевания и протяженности процесса по кишке (Табл. 1).
Таблица 1 Медикаментозное лечение при язвенном колите
Распространенность поражения
| Тяжелая форма | Среднетяжелая форма | Легкая форма | |
| Тотальное поражение | Гидрокортизон внутривенно, внутримышечно 500 мг/сут ( по 125мг 4 раза ) в течение 5-7 дней, затем Преднизолон 1-1.5 мг/кг массы тела в сутки | Гидрокортизон внутримышечно 250-375 мг/сут ( по 125мг 2-3 раза) или Преднизолон 1-1,5 мг/кг массы тела в сутки | Салофальк 1.5-2г в сутки ( в упорных случаях -3-4г) или Сульфасалазин 4 — 6г в сутки; при отсутствии эффекта — Преднизолон 0,5-1,0 мг/кг массы тела в сутки |
| Левостороннее поражение | Гидрокортизон внутримышечно 250-375 мг/сут (по 125мг 2-3 раза ) в течение 5-7 дней или Преднизолон 1-1,5 мг/кг массы тела сутки | Преднизолон 1-1,5 мг/кг массы тела сутки, либо Салофальк 4г в сутки перорально или ректально ( возможен одновременный прием таблеток и ректальное введение суспензии или свечей ) | Суспензия Салофалька ректально – 30-60мл ( 2-4г Месалазина ), либо Сульфасалзин 4г в сутки + Гидрокортизон ректально 65-250 мг/сут |
| Дистальное поражение (проктит, проктосигмоидит) | Преднизолон 0.5-1.0 мг/кг массы тела сутки, | Ректально суспензия Салофалька — 30-60мл (2-4 г Месалазина), или суппозитории Салофалька 3-4 г (при распространенности процесса в прямой кишке до 12 см); сульфасалзин 4-6 г в сутки + гидрокортизон ректально 65 мг 2 раза в сутки. | Ректально суспензия Салофалька — 30-60 мл (2-4 г Месалазина) или суппозитории Салофалька 1.5-2 г (при протяженности процесса в прямой кишке до 12 см); Гидрокортизон ректально 125 мг на ночь или суппозитории с Преднизолоном 5 мг 2 раза в сутки. |
При острой тяжелой форме ЯК или тяжелой атаке хронических форм заболевания лечение следует начинать с внутривенного введения гидрокортизона не менее 500 мг в сутки, равномерно распределенного на 4 — 6 введений с одновременной коррекцией водно-электролитных нарушений, введения крови и кровезаменителей и при возможности проведения гемосорбции с целью быстрого устранения эндотоксемии. Суспензия Гидрокортизона может вводиться и внутримышечно, однако продолжительность такого введения ограничивается 5 — 7 днями из-за возможного развития абсцессов в местах инъекций при более продолжительном введении и возможной задержке жидкости. Через 5 — 7 дней следует перейти на пероральное назначение Преднизолона. За это время проводится гастроскопия для исключения язвенной болезни желудка и 12- перстной кишки. При среднетяжелой форме и отсутствии клинических признаков, а также анамнестических указаний на гастродуоденальные язвы лечение следует сразу начинать с перорального приема Преднизолона. Обычно Преднизолон назначается в дозе 1-1,5 мг/кг массы тела в сутки. Дозу в 100 мг следует считать максимальной.
При хорошей переносимости гормональных препаратов назначенную дозу рекомендуется принимать до получения стойкого положительного результата — в течение 6 — 8 недель. После этого проводят снижение по так называемой “быстрой ступенчатой” схеме: на 10 мг каждые 3 — 5 дней. Начиная с 30 — 40 мг рекомендуется однократный прием Преднизолона в утренние часы, что практически не вызывает серьезных осложнений. В это же время в лечебную схему включают Салофальк или Сульфасалазин, которые следует принимать до полной отмены гормонов. Начиная с 30 мг, отмену Преднизолона проводят более медленно — по 5 мг в неделю в течение 2 — 2,5 месяцев. Таким образом, полный курс гормональной терапии продолжается от 8 до 16 недель в зависимости от формы ЯК.
При дистальных формах поражения и I — II степени активности процесса по данным ректороманоскопии следует назначать Гидрокортизон ректально капельно или в микроклизмах. Причем, если больные плохо удерживают большие объемы, то начинать введение Гидрокортизона (65 — 125 мг) следует в 50 мл физраствора и по мере стихания воспаления, уменьшения частоты ложных позывов увеличить постепенно объем до 200 — 250 мл на лечебную клизму. Препарат обычно вводят после стула утром или перед сном.
При язвенных проктитах и сфинктеритах достаточно хороший эффект оказывают свечи с Преднизолоном (5 мг), вводимые 3 — 4 раза в сутки. При более тяжелом течении дистальных форм, сопровождающихся повышением температуры, общей слабостью, анемией и III — IV степенью активности по данным ректоскопии, в случаях отсутствия эффекта от Сульфасалазина или Салофалька показано лечение Преднизолоном внутрь в дозе 30 — 50 мг в сутки.
У больных среднего и пожилого возраста доза Преднизолона не должна превышать 60 мг, так как для них характерно наличие сопутствующих заболеваний: атеросклероз, гипертоническая болезнь, сахарный диабет и др. В тех случаях, когда ЯК протекает на фоне атеросклеротического поражения брыжеечных артерий, в лечебный комплекс следует вводить сосудистые препараты: Трентал, Продектин и др.
Проведение гормональной терапии сопряжено с развитием побочных эффектов: задержка в тканях жидкости, хлоридов и натрия (возможны отеки), артериальная гипертензия, гипокалиемия, потеря кальция, остеопороз, различные вегетативные расстройства, нарушение углеводного обмена, надпочечниковая недостаточность, язвы желудка, желудочно-кишечное кровотечение. В этих случаях рекомендуется назначение адекватной симтоматической терапии: гипотензивных препаратов, диуретических средств, препаратов кальция, антацидных средств. При нарушении углеводного обмена необходима диета с ограничением углеводов, по показаниям дробное введение инсулина (соответственно гликемии) или назначаются пероральные противодиабетические лекарства. Для профилактики развития тромбозов у больных с тяжелыми формами ЯК, получающих гормональное лечение, следует проводить постоянный контроль свертывающей системы крови и одновременно назначать дезагреганты: Курантил, Продектин и др.
АКТГ-цинк фосфат эффективен только при острой форме ЯК, поскольку его влияние опосредовано сохраненной функцией собственных надпочечников. Препарат вводят внутримышечно в дозе 20 — 40 мг в зависимости от тяжести атаки.
В последние годы при лечении воспалительных заболеваний кишечника, особенно БК активно используются препараты, содержащие в качестве активного компонента глюкокортикостероид ( ГКС ) будесонид. В отличие от традиционных, ГКС будесонид обладает очень высокой степенью сродства с рецепторами и высоким метаболизмом в печени при “первом прохождении” (около 90 %). За счет этого он оказывает очень мощное местное противовоспалительное действие при минимальном количестве системных побочных эффектов. В качестве альтернативы Преднизолону и Гидрокортизону можно рекомендовать препарат Буденофальк. При разработке структуры Буденофалька учитывались физиологические характеристики желудочно-кишечного тракта. В каждой капсуле Буденофалька находится около 350 микросфер, состоящих из будесонида, покрытого полимерной оболочкой, устойчивой к действию желудочного сока. Освобождение будесонида из микросфер происходит в подвздошной и толстой кишках при значениях Рн > 6.4. Буденофальк применяется для лечения легких и среднетяжелых обострений ЯК. Рекомендуемая суточная доза составляет одну капсулу Буденофалька, содержащую 3 мг будесонида, 3 раза в сутки.
Для лечения крайне тяжелых форм ЯК, торпидных к терапии кортикостероидами, в последнее время с успехом применяется иммунодепрессант Циклоспорин А, который вводится внутривенно (суточная доза 4 мг/кг массы тела). Терапия Циклоспорином А позволяет избежать колэктомии у 40 — 50 % пациентов. Широкое использование препарата ограничивают его высокая стоимость и значительное число побочных эффектов.
При хроническом непрерывном течении ЯК и в случаях гормональной зависимости целесообразно применение Азатиоприна (1,5 – 2,5 мг/кг массы тела в сутки ). Было показано, что применение азатиоприна или 6-меркаптопурина в этих клинических ситуациях позволяло добиться положительного эффекта ( наступление ремиссии, уменьшение дозы или полная отмена кортикостероидов) почти у 60 % пациентов.
Нарушение барьерных функций толстой кишки при ЯК может быть причиной развития синдрома токсемии. Для ее коррекции необходимо назначение соответствующего комплекса, восстановление эубиоза, антибактериальная терапия, гемосорбция, УФО аутокрови.
Учитывая выраженные обменные нарушения и катаболическое действие стероидных гормонов, целесообразно парентеральное введение белковых препаратов: сывороточного альбумина, протеина плазмы, незаменимых аминокислот.
Для улучшения процессов микроциркуляции и транскапиллярного обмена показано введение Реополиглюкина, Гемодеза (в обычных дозировках).
При анемии (гемоглобин 90 г/л и ниже), являющейся признаком тяжелой атаки ЯК, рекомендуется проведение гемотрансфузии по 250 мл одногруппной крови с интервалом в 3 — 4 дня. При снижении уровня железа в сыворотке крови необходимо включение в лечебный комплекс препаратов железа.
Учитывая иммунологические нарушения при ЯК, в терапии заболевания используются иммуномодуляторы, Левамизол, Тималин и др. Однако роль их при ЯК до конца не ясна, терапевтический эффект от их применения кратковременный, поэтому активность этих препаратов как базисных средств сомнительна.
Целесообразно рекомендовать использование иммуномодуляторов в сочетании с базисным противовоспалительным лечением.
Назначаются витамины группы В, С, А, Д, К , которые также способствуют восстановлению эубиоза в кишечнике.
В лечебный комплекс включают психотропные средства в обычных дозировках, ориентируясь на индивидуальную переносимость.
Обострение ЯК в отдельных случаях сопровождается синдромом раздраженного кишечника, чаще всего проявляющегося запорами. В этом случае оправдано назначение пшеничных отрубей или патентованных препаратов, содержащих балластные вещества (Мукофальк и др.), которые способствуют нормализации стула и одновременно являются энтеросорбентами.
Стационарное лечение заканчивается при достижении клинико-эндоскопической ремиссии, после чего больной подлежит диспансерному наблюдению в поликлинике у врача-терапевта, гастроэнтеролога или проктолога.
Противорецидивное лечение при ЯК. Вопрос о характере и длительности противорецидивного лечения при ЯК пока остается нерешенным. Согласно одной из точек зрения, противорецидивное лечение рекомендуется проводить пожизненно, однако, учитывая высокую стоимость препаратов (табл. 2) и риск возникновения побочных эффектов при их длительном применении, в гастроэнтерологическом отделениии ГНЦ колопроктологии придерживаются следующей тактики. После купирования атаки ЯК рекомендуется поддерживающая доза аминосалицилатов на срок 6 мес. Если за этот период времени не было отмечено клинических признаков обострения заболевания, а при контрольном эндоскопическом исследовании через полгода констатируется ремиссия, противорецидивное лечение можно отменить. Если же во время курса противорецидивной терапии состояние больного было нестабильным, иногда требовалось увеличить дозу аминосалицилатов для устранения симптомов обострения, а при контрольной эндоскопии выявляются признаки активного воспаления, противорецидивное лечение необходимо продлить еще на полгода. Больные с хроническим непрерывным течением ЯК нуждаются в длительном непрерывном лечении, как правило, высокими дозами аминосалицилатов, однако эта терапия не является в полном смысле этого слова “противорецидивной” . Это скорее сдерживающее противовоспалительное лечение. У этой категории больных также широко используются цитостатики (азатиоприн или 6-меркаптопурин) и интермиттирующие схемы приема кортикостероидов.
Таблица 2
| Наименование препарата | Изготовитель | Стоимость (в рублях) |
| Сульфасалазин | “Словения” | Таблетки 50шт*500мг =195руб. — 359 руб. |
| Салофальк | “Доктор Фальк” (Германия) | Таблетки 100шт*250 мг =580руб 00 коп – 980 руб. 00коп |
| — “ — | — “ — | Суспензия 2 г-=500 руб. 1036руб. 4 г. -= 1300 руб. 2179 руб. |
| Фолиевая кислота | Россия | Таблетки 100 шт*400 мкг =155 руб. |
| Гидрокортизон | Гидеон Рихтер (Венгрия) | Инекции 2,5 %(2 мл) 5*2=109 руб. – 123 руб. |
| Преднизолон | Hafslund | Таблетки 30шт*5 мг = 40 руб. – 70 руб 00 коп. |
| Глюкокортикоид (будесонид) | Познан-ФЗ-Польфо | Аэрозоль 1 шт*0,2 мг (10 мл)= 195 руб. – 372 руб. |
| Реополиглюкин | Беларусь | Инекции = 51 руб. — 80 руб. |
| Гемодез Мукофальк | Россия “Доктор Фальк” Германия | Инъекции 200 мл –24 руб. 400 мл. – 59 руб. 150 г — 191 руб. –212 руб. |
Источник публикации: www.webmed.ru
Болезнь Крона: причины и симптомы
Хроническая воспалительная болезнь Крона характеризуется тем, что она поражает полностью весь желудочно-кишечный тракт, начиная с полости рта и заканчивая анальным отверстием. При этом, как правило, воспаление начинается в подвздошной кишке, а потом переходит на остальные отделы кишечника.
Симптомы воспаления подвздошной кишки идентичны с симптомами острого аппендицита. Поэтому часто, начав пациента оперировать, врачи обнаруживают болезнь Крона и ставят правильный диагноз.
Что касается причин возникновения этого недуга, то врачи склоняются к инфекционной природе, поскольку с ним хорошо справляются антибиотики.
Предрасполагающие факторы:
- перенесение кори
- пищевая аллергия
- стресс
- курение
- наследственность
В клинической картине выделяют местные, общие и внекишечные симптомы проявления болезни Крона.
Клинический случай
Пациентка Л., 1981 года рождения. Заболевание дебютировало в возрасте 14 лет диареей с примесью крови 5—6 раз в сутки. С подозрением на ЯК наблюдалась у детского гастроэнтеролога. В возрасте 16 лет диагноз верифицирован в условиях гастроэнтерологического отделения БУ «Республиканская клиническая больница» г. Чебоксары. В протоколе колоноскопии (КС) от 1998 г. вынесено заключение: «Слизистая оболочка прямой кишки отечная, ярко гиперемирована, с налетом белого цвета. Слизистая оболочка сигмовидной кишки ярко гиперемирована, зернистая. На расстоянии 25—30 см от ануса группа эрозий размером 0,1×0,2×0,4 см, некоторые с налетом фибрина. Проксимальнее селезеночного угла толстой кишки слизистая оболочка отечная, гиперемирована, эрозирована, отмечается умеренная контактная кровоточивость». В анализе крови, взятой за сутки до проведения КС, отмечена нормохромная анемия легкой степени (гемоглобин — 115 г/л), нейтрофильный лейкоцитоз (12,6·109/л), ускоренная до 30 мм/ч СОЭ и двукратное повышение уровня С-реактивного белка.
На основании приведенных клинико-лабораторных данных и данных анамнеза (у пациентки фиксировались более чем полугодовые периоды ремиссии) сформулирован следующий клинический диагноз: «Язвенный колит, хроническое рецидивирующее течение, тотальный (в соответствии с Монреальской классификацией), среднетяжелая атака (согласно критериям Truelove-Witts), умеренная эндоскопическая активность (по Schroeder)».
С учетом тотальной локализации ЯК III степени активности и средней степени тяжести начата терапия сульфасалазином в дозе 3,0 г/сут в сочетании с глюкокортикоидами (ГКС) 60 мг/сут. Достигнуто клиническое улучшение, ГКС постепенно удалось полностью отменить. До 2004 г. регулярно принимала сульфасалазин 2,0 г/сут или салофальк 3,0 г/сут и местно салофальк свечи 2 раза в день. Периодически к лечению подключали ГКС в стартовой дозе 60 мг/сут с полной отменой при достижении клинической ремиссии.
Эндоскопическая картина в 2004 г. описана следующим образом: «Слизистая оболочка прямой, сигмовидной и ободочной кишки умеренно отечная, зернистая, с очагами гиперемии. Баугиниева заслонка розовая, эластичная. Устье аппендикса без признаков воспаления. Слизистая оболочка слепой кишки отечная, с усиленным сосудистым рисунком».
В 2004 г. пациентка забеременела. В сроке 11 нед развилось обострение заболевания: появилась диарея с кровью до 10 раз в сутки. Назначены преднизолон внутрь в дозе 40 мг, внутривенные инфузии свежезамороженной плазмы. Состояние удалось относительно стабилизировать, но в сроке 28 нед возник приступ мочекаменной болезни, по поводу чего проводилась катетеризация мочеточника. В последующем сохранялась угроза прерывания беременности, в сроке 34 нед произошли преждевременные роды.
В соответствии с рекомендациями Российской гастроэнтерологической ассоциации и ассоциации колопроктологов России по диагностике и лечению взрослых больных ЯК беременность необходимо планировать в период ремиссии. При этом большинство препаратов для лечения ЯК сопряжены с низким риском неблагоприятного воздействия на плод (за исключением метотрексата). Побочные эффекты применения ГКС могут быть снижены сопутствующим приемом кальция, ингибиторов протонного насоса, мониторингом уровня глюкозы в крови [4].
До 2008 г. пациентка чувствовала себя удовлетворительно, сохранялась клиническая ремиссия. В 2009 г. развилось очередное обострение: диарея до 12 раз в сутки с примесью крови, гноя, слизи, абдоминальный болевой синдром. Доза преднизолона увеличена до 60 мг/сут, добавлен метронидазол 1,0 г/сут. При попытках снижения дозы ГКС до суточной (10 мг) все симптомы заболевания возвращались в течение нескольких дней. Таким образом, у пациентки сформировалась гормонозависимость. Для ее преодоления к лечению добавлен азатиоприн в дозе 150 мг/сут.
В литературе приводятся сведения о повышении риска развития оппортунистических инфекций на фоне применения ГКС в 2,2 раза, иммуносупрессивной терапии — в 3,4 раза и при их сочетанном применении — в 17,5 раза [5, 6].
У пациентки на фоне проводимой терапии в 2009 г. развился инфильтративный туберкулез верхушки левого легкого, что потребовало отмены цитостатика и проведения противотуберкулезного лечения по поликомпонентной схеме с рифампицином в течение 1 года. При этом полностью отменить ГКС не удавалось, и пациентка продолжала получать преднизолон 10 мг/сут до 2014 г. В июне 2014 г. проконсультирована в ФГАОУ ВО «РНИМУ им. Н.И. Пирогова» (Москва). Ранее установленный диагноз подтвержден, рекомендовано возобновить терапию азатиоприном 100 мг/сут в сочетании с метилпреднизолоном 16 мг/сут. Удалось добиться некоторого клинического улучшения течения заболевания, однако стали возникать осложнения проводимой терапии (фурункул кожи лица, фурункул большой половой губы). С октября 2014 г. возобновились ноющие боли по ходу толстой кишки, наиболее выраженные в левой подвздошной области, уменьшающиеся после отхождения газов и дефекации, урчание и переливание в животе, повышенное газообразование. Отмечался жидкий стул до 7 раз в сутки с примесью гноя, крови, слизи, с остатками непереваренной пищи, беспокоили ложные позывы и тенезмы. Кроме того, пациентка отмечала выраженную общую слабость (за 2 мес похудела на 5 кг), артралгии в крупных суставах нижних конечностей. Пациентка самостоятельно прекратила прием азатиоприна, что привело к выраженному обострению заболевания. В течение последующего года неоднократно госпитализирована. На тот период по лабораторным данным отмечены гипохромная анемия (гемоглобин — 105 г/л), нейтрофильный лейкоцитоз (14,6·109/л), СОЭ — 36 мм/ч и двукратное повышение уровня С-реактивного белка. При эндоскопическом исследовании выявлены деструктивные изменения слизистой оболочки, гнойный налет, множество эрозий и язв размером до 4—5 мм, умеренная контактная и спонтанная кровоточивость. Проводилось внутривенное введение преднизолона 125 мг в течение 7 дней с последующим переходом на прием внутрь в дозе 75 мг с постепенным уменьшением до суточной дозы 40 мг и подключением сульфасалазина 2,0 г/сут. Осуществляли инфузии метронидазола 500 мг/сут, коррекцию электролитных нарушений. Лечение продолжено амбулаторно препаратами аминосалициловой кислоты по 3,0 г/сут в сочетании с будесонидом в дозе 9 мг/сут. При достижении относительно стабильного состояния рекомендован рифаксимин 800 мг/сут в течение 7 дней в сочетании с бифиформом.
В мае 2022 г. — вновь ухудшение состояния: жидкий стул 14 раз в сутки небольшим объемом со слизью и кровью, чаще в ночное время, вздутие живота, тенезмы, периодические ноющие или спастические боли невысокой интенсивности в левой половине живота, иногда усиливающиеся после дефекации, артралгии, слабость, отсутствие аппетита, жажда, бессонница. Сохранялась субфебрильная температура тела, нарастала анемия (гемоглобин — 95 г/л), нейтрофильный лейкоцитоз (15,6·109/л), СОЭ — 53 мм/ч, уровень C-реактивного белка повышен трехкратно. Кроме того, отмечалось повышение панкреатической амилазы до 51 Ед/л (референсные значения — до 50 Ед/л) и эластазы 1-го типа до 26 мкг/л (референсные значения — до 3,5 мкг/л). Уровень фекального кальпротектина превышал норму почти в 20 раз и достигал 980 мкг/г.
При колоноскопии — слизистая оболочка во всех отделах толстой кишки резко отечна с обилием острых язв разной величины (некоторые из язв со следами продолжающегося кровотечения) и острых эрозий, многочисленных подслизистых геморрагий. Выраженная контактная кровоточивость, множественные полиповидные образования в сигмовидной, прямой, поперечно-ободочной кишке.
Для дифференциальной диагностики с болезнью Крона проведено исследование на антинейтрофильные цитоплазматические антитела (pANCA), IgG/IgA, антитела к Saccharomyces cerevisiae (ASCA), IgG/IgA, антитела к бокаловидным клеткам кишечника, антитела к экзокринной части поджелудочной железы. Указанные антитела в крови больной не обнаружены.
Назначена комплексная терапия (ГКС, метронидазол, сульфасалазин), однако достичь ремиссии и преодолеть гормональную зависимость не удавалось. С августа 2022 г. возобновлен прием азатиоприна, однако сохранялась клинико-эндоскопическая активность процесса. В соответствии с клиническими рекомендациями при рецидиве, возникшем на фоне поддерживающей терапии тиопуринами, показано повторное назначение ГКС, однако во избежание формирования стероидозависимости более целесообразным признано назначение биологических препаратов [4].
Учитывая неэффективность предшествующей терапии иммуносупрессорами, высокую степень воспалительной активности заболевания, формирование гормонозависимости, решено начать подбор биологического препарата для пациентки. До начала антицитокиновой терапии необходимо проводить скрининг на наличие туберкулезной инфекции, который включает в себя: тщательный сбор анамнеза, рентгенографию (не флюорографию!) грудной клетки в двух проекциях, проведение пробы Манту с внутрикожным ведением 2 туберкулиновых единиц, при необходимости — квантифероновую пробу или диаскинтест [7].
Биологические препараты — блокаторы фактора некроза опухоли альфа (ФНО-α) — инфликсимаб, адалимумаб, голимумаб имеют достаточно широкий спектр показаний [8]. Помимо воспалительных заболеваний кишечника они применяются при ревматоидном и псориатическом артрите, анкилозирующем спондилоартрите, неинфекционном увеите, псориазе [9—12]. Препараты, содержащие моноклональные антитела к ФНО-α, приводят к определенному снижению уровня иммунной защиты организма и повышению его восприимчивости к различным инфекциям, включая туберкулез, повышают риск разрушения туберкулезной гранулемы и реактивации латентного туберкулеза [4]. У пациентки уже имелся инфильтративный туберкулез в анамнезе, поэтому решено воздержаться от применения этой группы препаратов.
Ведолизумаб (энтивио) — единственный из зарегистрированных в РФ биологических препаратов только для лечения ВЗК, селективно блокирует воспаление в кишечнике [11]. Он представляет собой гуманизированные моноклональные антитела IgG, связывающиеся с интегрином α4β7 на поверхности лимфоцитов и селективно блокирующие его взаимодействие с молекулами клеточной адгезии MADCAM-1 слизистой оболочки кишечника. Именно эти молекулы играют ведущую роль в миграции Т-хелперных лимфоцитов, вызывающих хронический воспалительный процесс, характерный для ЯК и болезни Крона [11].
Данные о безопасности более 4800 пациенто-лет экспозиции демонстрируют отсутствие повышенного риска инфекций, в том числе тяжелых, при применении препарата ведолизумаб. Частота нежелательных явлений при применении в стандартных дозах сопоставима с плацебо, что позволяет использовать препарат длительно [13]. Вероятность стойкой ремиссии после курсового введения ведолизумаба при прочих равных условиях в 2—4 раза превосходит таковую при применении препаратов из группы ФНО-α при среднетяжелом и тяжелом ЯК в случае резистентности к стандартной терапии [14]. Вероятность отмены ведолизумаба вследствие развития неблагоприятных побочных реакций в 4,8—7 раз ниже, чем при терапии адалимумабом или голимумабом в процессе 52-недельной поддерживающей терапии у пациентов, впервые получающих лечение препаратами моноклональных антител [14].
Клинические испытания и постмаркетинговые данные показали, что частота оппортунистических инфекций и туберкулеза у пациентов, получающих ведолизумаб, была низкой. Не сообщалось о вирусной реактивации гепатита В или С [15]. Высокая селективность иммуносупрессивного действия ведолизумаба позволяет назначать его даже пациентам с повышенным риском развития оппортунистических инфекций или пожилым людям [16]. Схожая тенденция отмечается и в отношении частоты развития новообразований: доказано, что ведолизумаб имеет благоприятный профиль безопасности с низкими показателями заболеваемости злокачественными новообразованиями в течение длительного периода лечения [17].
У данной пациентки имелись следующие показания к применению данного препарата: среднетяжелый и/или тяжелый активный ЯК, неадекватный ответ и/или неэффективность лечения (или снижение эффективности), непереносимость одного или нескольких препаратов стандартной терапии [11].
После скрининга на туберкулез, иерсиниоз, вирусные гепатиты начата индукционная терапия ведолизумабом в ноябре 2022 г. и продолжен прием азатиоприна в дозе 150 мг/сут.
Ведолизумаб (энтивио) вводят внутривенно капельно 300 мг в течение 30 мин, затем в той же дозе через 2 нед и через 6 нед после первого введения, далее — каждые 8 недель [11]. По данным литературы, терапевтический эффект проявляется уже после первого применения ведолизумаба [18].
Инфузии препарата пациентка перенесла удовлетворительно. Признаки значительного улучшения самочувствия и регрессии симптоматики отмечены через 3 нед (после второго введения): исчезли тенезмы, нормализовалась температура тела, уменьшились частота стула и количество патологических примесей в нем, стала существенно меньше беспокоить слабость.
С четвертой недели терапии пациентка отметила значительное улучшение: стул — без патологических примесей, кратностью не более трех раз в сутки, нормализовались сон и аппетит, уменьшилась слабость. Клиническое улучшение подтверждалось лабораторными данными: уровень гемоглобина повысился до 110 г/л, уменьшилась выраженность лейкоцитоза до 9,0×109/л, нормализовались СОЭ (13 мм/ч), уровни панкреатической амилазы и С-реактивного белка. Фекальный кальпротектин с 890 снизился до 90 мкг/г (референсные значения — до 50 мкг/г). Эндоскопически: прямая кишка расправляется, на стенках мутная слизь, слизистая оболочка отечная, с очагами атрофии и рубцами.
На настоящий момент пациентке проведено 7 инфузий энтивио по 300 мг каждые 8 недель. Клинический ответ и ремиссию оценивали в соответствии с общепринятыми стандартами, широко используемыми в клинических исследованиях ВЗК. Клинический ответ определяли как снижение ≥3 баллов индекса Харви—Брэдшоу (HBI), а также абсолютного показателя Simple Clinical Colitis Activity Index (SCCAI) ≤2 при последующем наблюдении по сравнению с исходным уровнем. Клиническую ремиссию определяли как SCCAI ≤2. Нежелательные явления, связанные с получением препарата, не отмечены, развитие оппортунистических инфекций, туберкулеза, онкопроцесса не зарегистрировано. Состояние пациентки расценивается как хорошее. Достигнута полная клиническо-эндоскопическая ремиссия.