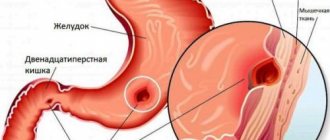
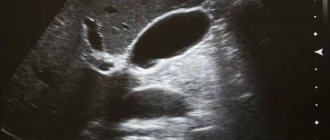
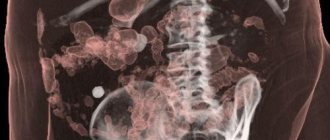
Необратимым явлением, во время которого свою жизненную активность прекращают клетки, ткани, органы, называют некроз. Его спровоцировать могут болезнетворные микробы, механические, термические, химические, инфекционно-токсические агенты, которые способствовали разрушению тканей. Кроме этого, некроз может возникнуть, как результат аллергии, нарушенного кровообращения. Учитывая состояние организма и неблагоприятные местные факторы, можно определить выраженную степень омертвления клеток.
Провоцирующим фактором возникновения некроза являются патогенные микроорганизмы, грибки, вирусы. При нарушенном кровообращении и наличии переохлаждения этого участка тела, произойдет усиление спазма сосудов и сильное нарушение циркуляции крови. При чрезмерном перегревании повышается обмен веществ, а если кровообращение нарушено, повышается риск развития некротического процесса.
Как проявляется некроз
Если говорить о первых симптомах некроза, они представлены в виде онемения, отсутствии чувствительности. В такой ситуации необходимо безотлагательно посетить опытного и квалифицированного врача медицинского центра. Кроме этого, кожные покровы становятся бледными. Это происходит потому, что нарушено кровообращение. С течением времени кожа приобретет синюшный оттенок, затем станет чёрной или тёмно-зелёной. При наличии некроза в нижней конечности, человек отмечает быстрое утомление во время ходьбы, ощущение холода, появляются судороги, а также хромота, в результате чего, произойдет образование незаживающих трофических язв, которые со временем будут некротизироваться.
Из-за того, что перестает нормально функционировать дыхательная и центральная нервная система, почки, печень, нарушается кровообращение, у человека ухудшается общее состояние всего организма. Кроме этого, снижается иммунная система, так как появляются сопутствующие заболевания крови, анемия, а также, нарушаются обменные процессы, организм истощается, наблюдается наличие гиповитаминоза и переутомления.
Подготовка к лечению
Перед операцией обычно проводятся диагностические тесты, чтобы проверить общее состояние здоровья и убедиться, что операция может быть проведена. Это может быть забор крови, рентгенография грудной клетки, электрокардиограмма (ЭКГ), ангиография, КТ или УЗИ, эндоскопия. Следует соблюдать диету, исключающую бобовые, выпечку, спиртное, свежие фрукты и овощи. Жидкая диета вводится, по крайней мере, за день до операции, при этом ничего не принимается в день операции. В зависимости от типа резекции кишечника может потребоваться очистить кишечник. Обычно это включает прием слабительного препарата за 1-2 дня до операции. Также могут быть сделаны очищающие клизмы в больнице. Непосредственно перед процедурой назначаются антибиотики, чтобы помочь предотвратить инфекцию. Кроме того, следует сказать врачу о всех принимаемых лекарствах, пищевых добавках и травяных сборах.
Разновидности
Учитывая происходящие изменения в ткани, существуют некоторые формы некроза. А именно:
- Причиной возникновения коагуляционного или сухого некроза является сворачивание, уплотнение, высыхание тканевого белка, который затем становится творожистой массой. Это является результатом того, что перестала прибывать кровь и испарилась влага. Участки ткани становятся сухими, ломкими, а также, приобретают тёмно-коричневый или желтовато серый оттенок с четкими демаркационными линиями. На том месте, где произошло отторжение омертвевшей ткани, появятся язвы, произойдёт развитие гнойного процесса, формирование абсцесса. Локализацией сухого некроза является селезенка, почки, культя пуповины у новорожденного ребенка.
- При колликвационном или влажном некрозе происходит набухание, размягчение и разжижение омертвевшей ткани, а также, образуется масса с серым оттенком, появляется гнилостный запах.
Существуют некоторые виды некроза
1. Если внезапно прекратилось кровоснабжение в ткани или органе, появляется инфаркт. Под термином ишемический некроз подразумевают омертвление какой-либо части жизненно важного органа (мозг, сердце, кишечник, лёгкие, почки, селезенка). Если инфаркт небольшой, наблюдается наличие аутолитического расплавления или рассасывания с последующим восстановлением тканей. Инфаркт может закончиться нарушенной жизнедеятельностью тканей, различными осложнениями, и даже смертью.
2. Если произошло омертвение участка костной ткани, локализацией которого является секвестральная полость, это называется секвестром. В такой ситуации произойдет отделение этого участка от здоровых тканей. Причиной этому служит гнойный процесс.
3. Омертвение кожи, слизистой поверхности, мышечной ткани, называют гангреной. Причиной развития гангрены является некроз ткани.
4. Наличие пролежней наблюдается у того человека, который полностью обездвижен. Объясняется это длительным сдавливанием ткани и повреждением кожи. В результате этого, образуются глубокие гнойные язвы.
Возможные осложнения при лечении
Побочные эффекты, которые могут возникнуть, зависят главным образом от типа резекции кишечника и общего состояния здоровья. Они включают в себя:
- обструкцию (непроходимость) кишечника,
- парализованный или неактивный кишечник,
- повреждение ближайших органов, таких как мочевой пузырь, мочеточник или селезенка, анастомотическую утечку, связанную с инфекционными проблемами,
- чрезмерную кровоточащую раневую инфекцию,
- грыжу,
- тромбофлебит,
- невозможность контролировать мочеиспускание.
Лечащий врач должен быть проинформирован о любой из следующих проблем после операции: сильная боль, отек, покраснение, дренаж или кровотечение в области разреза, мышечные боли, головокружение или лихорадка, запоры, тошнота или рвота, ректальное кровотечение или черный, смолистый стул.
Стадии заболевания
Выделяют некоторые стадии развития данной болезни. Первая стадия характеризуется незначительным изменением костных тканей, когда у тазобедренного сустава сохранена функциональность, а болезненные ощущения имеют периодический характер. На второй стадии начинают образовываться трещины на поверхности сустава, нарушается его подвижность, человек испытывает постоянную боль. Третью стадию называют вторичным артрозом, когда в процесс происходит вовлечение вертлужной впадины. Наблюдается значительное снижение подвижности сустава. Такая стадия проявляется постоянными и сильными болезненными ощущениями. На четвёртой стадии начинает разрушаться кость, атрофируются мышцы, боль не устраняют лекарственные препараты.
Стадирование и классификация рака сигмовидной кишки
По типу опухолевого роста различают экзофитный и эндофитный рак. Экзофитные опухоли растут в просвет кишечника и имеют вид узлового образования или нароста. При чрезмерном разрастании, они могут обтурировать просвет кишки, вызывая кишечную непроходимость.
Эндофитная, или инфильтративная форма рака характеризуется тем, что растет в толще кишечной стенки. Опухоль может циркулярно охватывать стенку кишки, сужая ее просвет, что также вызывает кишечную непроходимость.
Стадирование заболевания осуществляется на основании данных о степени распространения опухоли:
- рак in situ — злокачественные клетки обнаруживаются только в поверхностном слое слизистой оболочки кишки.
- 1 стадия — опухоль прорастает слизистую оболочку кишечника и достигает подслизистой основы и мышечного слоя.
- 2 стадия — рак инфильтрирует всю стенку кишки и может выходить за ее пределы, но метастазов пока не дает.
- 3 стадия — появляются метастазы в регионарные лимфатические узлы. Опухоль может быть любых размеров.
- 4 стадия — имеются отдаленные метастазы, либо опухоль распространяется по брюшине (канцероматоз брюшины).
Что такое асептический некроз головки бедра
Головку бедренной кости относят к проблемной зоне, где повышен риск возникновения закупорки артерий, накопительных повреждений, причиной которых становятся перегрузки и бытовые травмы. Наличие различных патологических процессов могут спровоцировать асептический некроз бедра.
К основным причинам можно отнести длительный прием гормональных препаратов, антибактериальных средств. А также, если человек злоупотребляет алкоголем, часто находится в стрессовом состоянии. Провоцирующим фактором может быть наличие врожденного вывиха бедра, остеопении, остеопороза, системной красной волчанки, болезни Бехтерева, ревматоидного артрита.
Основное количество случаев отличается неутешительным ортопедическим прогнозом, наличием тяжёлого деформирующего артроза. В такой ситуации пациенту назначается проведение эндопротезирования, артродеза суставов или корригирующей остеотомии. Если своевременно провести магнитно-резонансную томографию, можно выявить болезнь на ранней стадии, которую можно вылечить с помощью консервативных методов.
Программа наблюдения после метода лечения
После резекции кишечника нужно будет оставаться в больнице в течение нескольких дней. В течение 1-2 дней после операции пациенту следует давать теплую, жидкую пищу. Твердые продукты и блюда будут вводится постепенно. Если была проведена колостомия или илеостомия, специально подготовленный медицинский работник научит пациента заботиться о себе. Временные остомии обычно остаются на месте в течение нескольких месяцев. После того, как остальная часть толстой кишки исцелится, будет проведена другая операция, анастомоз. Отверстие в животе будет закрыто. Назогастральная трубка вводится через нос в желудок во время операции и может быть оставлена на месте в течение 24-48 часов после операции. Это устраняет желудочные выделения и предотвращает тошноту и рвоту. Она останется до возобновления активности кишечника. Послеоперационный уход за пациентом включает также мониторинг артериального давления, пульса, дыхания и температуры. Измеряется потребление и выход жидкости, а в месте разреза наблюдают за цветом и количеством дренажа из раны. Пациент может вставать с постели примерно через 8-24 часа после операции. Большинство пациентов будут находиться в больнице в течение 5-7 дней, хотя лапароскопическая хирургия может уменьшить это пребывание до 2-3 дней. Послеоперационная потеря веса сопровождает почти все резекции кишечника. Вес и сила медленно восстанавливаются в течение нескольких месяцев. Необходимо будет соблюдать диету, которую назначит врач. Полное восстановление после операции может занять два месяца. Лапароскопическая хирургия может сократить это время до одной-двух недель.
Что такое некроз тазобедренных и коленных суставов
В тазобедренный сустав входят вертлужная впадина, головка бедренной кости. Тазобедренный сустав является самым крупным шарообразным составом в человеческом организме. Он кровоснабжается единственной артерией, проходящие через шейку кости бедра.
Если нарушена циркуляция крови, произойдет нарушение кровоснабжения данного участка, а также, не будет поступать кислород и питательные вещества, костная ткань потеряет свои свойства. Восстановительный процесс станет невозможным, появится остеоартроз, который сопровождается сильной болезненностью.
По истечении некоторого времени развивается некроз тазобедренного сустава. В такой ситуации пациенту необходимо заменить поврежденный сустав. Для этого используется искусственный аналог. Процедура называется эндопротезированием, когда полностью восстанавливается двигательная активность.
Разрушающие процессы в суставе колена появляются в результате травмы и потери кровоснабжения. Сочленения теряют свои функции, человек может стать инвалидом. При асептическом некрозе сустава колена человек испытывает сильные болезненные ощущения, наблюдает, что уменьшилась двигательная способность колена. С помощью магнитно-резонансной томографии и сканирования костей можно выявить начальную стадию изменений, в результате чего предотвращается дальнейшая потеря костной массы.
Используя нестероидные противовоспалительные препараты можно избавиться от болезненных ощущений и снять воспаление. Если человеку показано хирургическое вмешательство, проведут пересадку кости.
Оригинальная методика операций
Резекция и экстирпация проводятся на основе операции — тотальной мезоректальной эксцизии — ТМЭ. Для предупреждения появления сателит-метастазов при выделении прямой кишки традиционным способом, когда лимфоузлы, расположенные в мезоректуме, остаются неудаленными, я выполняю операцию через лапароскопический доступ. Такая методика позволяет свести развитие локальных рецидивов к минимуму, в нашей клинике этот показатель не превышает 5% (вместо 45%).
Наша клиника оснащена самым современным оборудованием и инструментарием, например, для предупреждения стриктуры или несостоятельного шва анастомоза после лечения в ходе операции используются сшивающие аппараты, мобилизация кишки выполняется бескровно благодаря применению аппарата электротермического лигирования тканей «LigaSure» и т. д.
Учитывая, что выведение части кишки на стенку живота может негативно отразиться на психологическом состоянии пациента, я стремлюсь проводить органосохраняющие операции, если это возможно. Поэтому в ходе оперативного лечения моей целью является сохранение непрерывности кишки и анального сфинктера, а также бережное оперирование, позволяющее сохранить нервные структуры в зоне вмешательства. Если формирование анастомоза невозможно, и выведение временной кишечной стомы на брюшную стенку — единственно правильное решение, то через несколько месяцев пациенту может быть проведена восстановительная операция, дающая возможность вернуться к привычному для человека способу опорожнения кишечника.
Что такое некроз таранной, плечевой кости
При таком заболевании появляются болезненные ощущения в плечевом суставе, ограничивается его движения, в результате чего, повышается риск возникновения атрофии. К редкому явлению относят измененную структуру плечевой кости. При прогрессировании заболеванием пациенту назначается проведения хирургического вмешательства, которое называют эндопротезированием. В данной ситуации это единственный способ, с помощью которого можно восстановить утраченные функции верхних конечностей.
Спонтанно возникает и стремительно прогрессирует некроз таранной кости. При дегенеративных изменениях в голеностопном суставе развивается деформирующий артроз. Благодаря современным диагностическим методам, которые используются в медицинском центре, можно определить раннюю стадию изменений голеностопного сустава. В такой ситуации применяется мозаичная остеохондропластика, в результате чего, восстанавливается анатомия сустава.
Группа риска
В настоящее время выделено несколько факторов риска, наличие который увеличивает вероятность развития рака злокачественных новообразований в сигмовидной кишке. Сюда относят:
Особенности питания
Увеличивают вероятность развития колоректального рака следующие особенности питания:
- Чрезмерное употребление жиров животного происхождения и красного мяса.
- Недостаточное содержание в рационе растительной клетчатки.
- Регулярное употребление алкоголя.
- Избыточное питание.
Доказано, что у вегетарианцев колоректальный рак диагностируется на порядок реже, чем у людей со стандартным пищевым рационом. Некоторое время даже было принято считать, то именно мясо является главным канцерогеном для кишечника и приводит к образованию злокачественных опухолей. Современная теория базируется на том, что растительные волокна, коими богат рацион вегетарианцев, очищают кишечник и не дают застаиваться его содержимому. Это уменьшает контакт кишечного эпителия с канцерогенами и предупреждает его злокачественную трансформацию.
Вторым фактором риска является наличие полипов. В подавляющем большинстве случаев рак кишечника развивается в результате малигнизации аденоматозных полипов. Причем, чем дольше он существует и чем больше его размеры, тем более вероятно его злокачественное перерождение.
Наследственность. Роль наследственной предрасположенности доказана в отношении двух синдромов: семейный аденоматозный полипоз (САП) и синдром Линча — наследственный неполипозный рак кишки. На долю наследственного рака приходится 5-7% случаев злокачественных опухолей рака данной локализации.
Другие факторы риска:
- Воспалительные заболевания толстого кишечника — неспецифический язвенный колит, болезнь Крона.
- Рак груди и рак яичников в анамнезе.
- Иммунодефицитные заболевания.
Диагностические мероприятия
При подозрении на наличие некроза, пациента могут отправить на рентгенологическое исследование. Однако следует учесть, что с помощью данного метода не выявляется патология на начальном этапе развития. Рентгеновский снимок способен выявить патологию, если она перешла на вторую или третью стадию. Во время исследования данного заболевания сдача анализа крови тоже не принесет эффективного результата. Благодаря современным аппаратам, которые используются для проведения магнитно-резонансной и компьютерной томографии, можно своевременно и с максимальной точностью выявить наличие изменений в структуре тканей.
Введение
Перекрут и некроз сальниковых отростков (жировых подвесков, appendices epiploicae) ободочной кишки (далее — отростки) относится к редким заболеваниям и встречается у 0,04-0,3% пациентов с острыми хирургическими заболеваниями органов брюшной полости. Изучению заболеваний отростков до настоящего времени уделяется мало внимания. Как правило, в литературе имеются описания единичных случаев диагностики и лечения перекрута и некроза отростков, и лишь отдельные авторы приводят анализ нескольких десятков наблюдений. Диагноз перекрута и некроза отростков редко удается поставить на дооперационном этапе. В большинстве наблюдений заболевание отростков обнаруживается во время лапароскопии или лапаротомии, показаниями к которым, как правило, служат другие заболевания органов брюшной полости и малого таза [8-10, 15, 16].
В развитии перекрута и некроза отростков считают значимым влияние ряда факторов. Предполагают, что развитию перекрута и некроза отростков способствуют нарушения моторной функции кишечника, наличие воспалительного очага (дивертикулита, холецистита, болезни Крона и др.), спаечного процесса в брюшной полости. К провоцирующим факторам развития заболевания отростков относят резкие движения (сгибание, разгибание), тяжелую физическую нагрузку, резкое снижение массы тела, голодание или переедание, закрытую травму живота [3-9, 15, 17]. Перекрут и некроз отростков встречается у лиц зрелого и пожилого возраста, примерно с одинаковой частотой у мужчин и женщин. В большинстве описанных наблюдений пациенты с перекрутом и некрозом отростков имели избыточную массу тела [3, 5, 6, 11, 12, 14-17].
Перекрут и некроз отростков крайне редко диагностируется на дооперационном этапе — не более в 63% наблюдений [1, 3-4, 7, 9]. Это связано в первую очередь с неспецифичностью клинических проявлений заболевания отростков. Как правило, заболевание возникает остро с постоянных болей в животе, являющихся основным симптомом заболевания [3-6, 8, 14-17]. Боли чаще всего локализуются в левой или правой подвздошной области, могут периодически усиливаться, не иррадиируют (при отсутствии вовлечения в воспалительный процесс других органов). Самостоятельный прием различных лекарственных средств (анальгетиков, спазмолитиков) не купирует болевой синдром, что заставляет больных обращаться за медицинской помощью. Тошнота, рвота, задержка стула и газов, диарея не характерны для перекрута и некроза отростков и встречаются не более чем в 30% наблюдений [1, 6, 14]. Температура тела может оставаться нормальной, а в ряде наблюдений повышается до субфебрильной. Перекрут и некроз отростков характеризуется более мягким течением и более медленным нарастанием симптоматики, что обусловливает позднюю обращаемость ряда пациентов (до 8 сут от начала заболевания). В среднем сроки поступления больных в стационар от начала заболевания составляют 1-3 дня [2, 6, 8, 14, 15].
Физикальное обследование больных, как правило, позволяет выявить только локальную болезненность при пальпации, в ряде наблюдений — локальное напряжение мышц передней брюшной стенки. Существенные диагностические трудности возникают при локализации болей в правой подвздошной области, так как нередко у этих пациентов выявляются симптомы острого аппендицита (Ровзинга, Ситковского и др.) [3, 6, 9].
При длительном существовании перекрута и некроза отростков возможно развитие инфильтратов, вовлекающих соседние органы брюшной полости и малого таза, на что могут указывать жалобы на дизурические явления (при вовлечении стенки мочевого пузыря), боли в правом подреберье (при вовлечении желчного пузыря, печени) и др. Это нередко приводит к постановке ошибочного диагноза и неверной тактике ведения больного [3-6, 9, 14-16].
Лабораторные методы исследования не позволяют обнаружить каких-либо специфических изменений: в анализах крови могут отмечаться умеренный лейкоцитоз (до 12’109/л), незначительное повышение уровня С-реактивного белка. Зарубежные авторы подчеркивают значительную роль ультразвукового исследования, компьютерной и магнитно-резонансной томографии брюшной полости в диагностике перекрута и некроза отростков [11, 12, 14]. Эти неинвазивные методы позволяют визуализировать измененный отросток, провести дифференциальную диагностику с другими заболеваниями органов брюшной полости и малого таза. Тем не менее в 50-63,4% наблюдений неинвазивные лучевые методы не позволяют обнаружить изменений отростков либо при этом их трактуют как другое заболевание [13, 15]. В связи с этим на дооперационном этапе, как правило, устанавливают диагноз других заболеваний органов брюшной полости и малого таза, наиболее частыми являются дивертикулит (до 50% наблюдений), острый аппендицит (13-76,5%), почечная колика (до 35%), перитонит (до 27,3%), заболевания придатков матки (до 19,6%) [1-3, 6-8]. Основным методом диагностики перекрута и некроза отростков большинство авторов считают лапароскопию, позволяющую верифицировать диагноз в 83-100% наблюдений [1, 8-10, 13, 15-16].
В настоящее время вопрос о лечебной тактике при перекруте и некрозе отростков окончательно не решен. Зарубежные авторы придерживаются мнения о консервативном лечении этого заболевания [11, 12], однако такая тактика может приводить к развитию осложнений, рецидиву заболевания (до 10% наблюдений). Большинство авторов являются сторонниками хирургического лечения — удаления пораженного отростка, которое может быть выполнено с использованием как лапароскопического, так и лапаротомного доступов [1, 6, 8, 12, 16]. Некоторые хирурги [3, 6,] предпочитают всегда при перекруте и некрозе отростков выполнять операцию из лапаротомного доступа, в ряде наблюдений сочетая удаление отростка с перитонизацией его ложа серозно-мышечными швами. В последнее время появляется все больше работ, посвященных лапароскопическим вмешательствам при перекруте и некрозе отростков [7, 13, 15-16]. При отсутствии некротических изменений перекрученного отростка ряд авторов предлагают производить эндоскопическую деторсию с помощью манипулятора с последующей оценкой жизнеспособности отростка (выполняется в 4,3-10% наблюдений). В 14,3-100% наблюдений выполняется лапароскопическое удаление патологически измененных отростков с различными способами обработки и пересечения ножки отростка: коагуляцией, клипированием, лигированием [2, 4, 5, 7, 8, 15-16].
Редкая встречаемость, неосведомленность врачей о заболевании отростков, необходимость хирургического лечения заболевания обусловливают актуальность изучения особенностей клинической картины, возможностей различных лабораторно-инструментальных методов в диагностике заболеваний сальниковых отростков ободочной кишки.
Цель исследования — изучение особенностей клинической симптоматики и оценка возможностей лапароскопии в современной диагностике и лечении больных с патологическими изменениями сальниковых отростков ободочной кишки.
Материал и методы
Проведен ретроспективный анализ историй болезни 87 пациентов с диагнозом перекрута и некроза сальниковых отростков ободочной кишки, которым было выполнено лапароскопическое вмешательство в клинике с января 1995 г. по декабрь 2012 г. Возраст больных составил от 20 лет до 81 года (в среднем 44±16 лет). Мужчин было 44 (50,6%), женщин — 43 (49,4%).
Статистический анализ данных осуществлялся с помощью программы SPSS 19. Для качественных признаков данные представлены в абсолютных величинах и долях в процентах. Для количественных признаков с нормальным распределением результатов данные приведены в виде M
±
SD
, где
М
— средняя арифметическая величина,
SD
— среднее квадратичное отклонение. Для количественных признаков с распределением результатов, отличающимся от нормального, данные представлены в виде Me [25; 75], где Me — медиана, 25 и 75 — 25-й и 75-й перцентили.
Результаты и обсуждение
В экстренном порядке в клинику поступали 84 (96,6%) пациента, из них 64 (76,2%) были доставлены бригадой скорой медицинской помощи, 20 (23,8%) самостоятельно обратились в приемное отделение клиники. 3 пациентки поступали в плановом порядке для хирургического лечения других заболеваний (папиллярная цистаденома левого яичника, хронический сальпингоофорит, полип сигмовидной кишки). Диагноз перекрута и некроза отростков был заподозрен на догоспитальном этапе врачом поликлиники лишь в 1 наблюдении; врачами приемного отделения — в 5 наблюдениях. Время от начала заболевания до поступления значительно варьировало, составляя от 2 ч до 7 сут (в среднем 48 [24; 69] ч).
Диагностика в стационаре на дооперационном этапе базировалась на жалобах больных, данных анамнеза, физикального обследования, данных лабораторных и инструментальных методов исследования. Клинические проявления перекрута и некроза отростков были скудными и неспецифичными, что приводило к постановке ошибочного диагноза на дооперационном этапе у большинства больных. Основные клинические проявления у пациентов с перекрутом и некрозом отростков приведены в табл. 1
.
Ведущим симптомом были постоянные боли в животе, отмечавшиеся у 85 (97,7%) больных. Преимущественной локализацией болей были нижние отделы живота — у 67 (78,8%) больных, часть из них отмечали локальные боли в правой или левой подвздошной области (см. табл. 1)
. У 7 (8,0%) больных имел место симптом Кохера-Волковича. Иррадиация болей присутствовала у 16 (18,4%) пациентов, чаще в правое бедро. Объяснить возникновение иррадиации болей у этих больных интраоперационными данными не удалось, лишь у 8 из них некротизированные отростки были спаяны с окружающими органами и тканями — стенкой толстой кишки, соседними отростками, большим сальником, париетальной брюшиной или придатками матки. У 14 (16,1%) больных боли усиливались при движении.
При выяснении данных анамнеза 7 (8,0%) больных отмечали наличие провоцирующих факторов: тяжелой физической нагрузки (3), резкого движения (1), приема антибактериальных препаратов (1), пищи (1), алкоголя (1). 26 (29,9%) больных самостоятельно принимали различные лекарственные средства (спазмолитики, анальгетики, антибактериальные препараты), которые не купировали болевой синдром. Неэффективность самостоятельного приема лекарственных препаратов и нарастающая интенсивность болей заставляли больных обращаться за медицинской помощью.
Жалобы на сухость во рту предъявляли 27 (31,0%) больных, на тошноту — 19 (21,8%). Рвота и нарушения стула отмечались у единичных больных. Лихорадкой страдали 33 (37,9%) пациента, чаще с подъемом температуры тела до субфебрильных значений. Нехарактерные жалобы были у 4 пациентов, что заставляло врачей заподозрить другое заболевание и приводило к постановке ошибочного предоперационного диагноза. С учетом данных интраоперационной лапароскопической картины возникновение жалоб можно связать с наличием сочетанных заболеваний, а также с развитием инфильтрата вокруг некротизированного отростка. 2 пациентки предъявляли жалобы на головокружение (интраоперационно, помимо заболевания отростка, обнаружены напряженная киста желтого тела у 1 и цистаденома левого яичника и маточная беременность 5 нед у 1). У одной пациентки были мажущие кровяные выделения из половых путей в течение 11 дней (интраоперационно диагностирован наружный эндометриоз малого таза). Один пациент предъявлял жалобы на учащенное мочеиспускание с резями над лоном (интраоперационно обнаружен плотный инфильтрат вокруг некротизированного отростка, вовлекающий большой сальник, стенку сигмовидной кишки, соседние отростки и фиксированный к париетальной брюшине в области дна мочевого пузыря).
Состояние 81 (93,1%) больного оценивалось как удовлетворительное, 5 (5,8%) — средней тяжести, 1 (1,1%) — тяжелое. Степень тяжести у последних 6 пациентов была связана с наличием сочетанных заболеваний — острого гангренозно-перфоративного аппендицита (1), перфорации дивертикула левой половины ободочной кишки (1), сопутствующих заболеваний терапевтического и неврологического профиля (4). Следует отметить, что 50 (57,5%) больных имели избыточную массу тела, в том числе предожирение выявлено у 13 (15,0%) пациентов, ожирение I степени — у 29 (33,3%), ожирение II степени — у 6 (6,9%), ожирение III степени — у 3 (2,3%). Средний индекс массы тела больных с перекрутом и некрозом отростков составил 29,7±5,0 кг/м2.
Основные данные, полученные при физикальном обследовании и лабораторно-инструментальных методах исследования, представлены в табл. 2
.
Язык был влажным у 79 (90,8%), светлый налет на языке отмечался у 60 (69,0%) больных. При осмотре живот у всех больных был симметричным, притупления в отлогих местах живота не было обнаружено ни у одного пациента. Живот был вздут у 5 больных. У большинства пациентов перистальтика была обычной звучности, лишь в 4 наблюдениях отмечалось ее ослабление, у 2 из этих больных интраоперационно обнаружен местный фибринозно-гнойный перитонит.
Локальное напряжение мышц передней брюшной стенки обнаружено у 15 (17,2%) больных.
В большинстве наблюдений — 83 (95,4%) — отмечалась болезненность при пальпации живота, нередко локальная — у 52 (59,8%) больных. Области, в которых выявлена максимальная болезненность при пальпации живота, представлены на рисунке
.
Рисунок 1. Болезненность при пальпации живота.
В 77 (88,5%) наблюдениях болезненность при пальпации обнаруживалась в нижних отделах живота, из них в 44 (50,6%) максимальная болезненность выявлена в правой подвздошной области, в 29 (33,3%) — в левой подвздошной области. Симптомы острого аппендицита (Ровзинга, Ситковского, Воскресенского) были обнаружены у 31 (35,6%) больного, что приводило к постановке диагноза острого аппендицита на дооперационном этапе в этих наблюдениях. Во время лапароскопии лишь у 3 из них выявлен острый аппендицит: флегмонозный — у 2, гангренозно-перфоративный — у 1. Симптом Щеткина-Блюмберга от сомнительного до положительного обнаружен у 29 (33,3%) пациентов.
Пальпируемое образование в брюшной полости обнаружено у 3 больных. Интраоперационно у них выявлены рыхлый инфильтрат, состоящий из петли сигмовидной кишки, правой маточной трубы, сальниковых отростков сигмовидной кишки (1), перекрут двух отростков сигмовидной кишки между собой (1), спаянный с париетальной брюшиной отросток сигмовидной кишки (1).
Существенные диагностические трудности на дооперационном этапе встретились у одной больной, предъявляющей жалобы на боли в правом подреберье. При осмотре у нее, помимо болезненности в данной области, выявлялся сомнительный симптом Ортнера, в связи с чем она в течение суток лечилась по поводу острого холецистита. Лишь на следующие сутки боли локализовались в левой подвздошной области, больной была выполнена диагностическая лапароскопия с целью дифференциальной диагностики между дивертикулезом и дивертикулитом левой половины ободочной кишки и перекрутом отростка сигмовидной кишки, последний диагноз подтвержден. Малоподвижное, плотное, болезненное пальпируемое образование в брюшной полости при ректальном, а также двуручном исследовании описано у одной больной. Интраоперационно был обнаружен рыхлый инфильтрат вокруг некротизированного отростка сигмовидной кишки, вовлекающий прядь большого сальника, подпаянный к париетальной брюшине малого таза и правого латерального канала.
При вагинальном исследовании у 6 (14,0%) больных обнаружено болезненное смещаемое образование слева или справа от матки, что заставляло на предоперационном этапе проводить дифференциальную диагностику с гинекологическими заболеваниями: перекрутом цистаденомы яичника (4), разрывом эндометриоидной кисты яичника (1), обострением хронического сальпингоофорита с формированием пиосальпинкса (1). У всех 6 больных во время лапароскопии обнаружен перекрученный и некротизированный отросток сигмовидной кишки, при этом у 2 из них вокруг отростков сформировался рыхлый инфильтрат. Лишь у одной больной из 6 было обнаружено сочетанное заболевание — цистаденома яичника без нарушения питания.
Лабораторные методы обследования у всех больных включали общий анализ крови с определением уровня гемоглобина, эритроцитов и лейкоцитов, общий анализ мочи. Показатели гемоглобина (среднее значение 146 [135; 150] г/л) и эритроцитов (среднее значение 4,88 [4,38; 5,21]’1012/л) в общем анализе крови были в пределах нормы у всех пациентов. Уровень лейкоцитов был повышен у 45 (51,7%) больных: у 28 (32,2%) отмечался умеренный лейкоцитоз с повышением уровня лейкоцитов до (9-12)’109/л, у 17 (19,5%) — более 12’109/л. У 9 больных в процессе динамического наблюдения проводили повторный анализ крови с определением уровня лейкоцитов, его повышение отмечено у 8 из них. Средний уровень лейкоцитов составил 9,0 [8,2; 11,4]’109/л. У 39 (44,8%) больных измеряли СОЭ, среднее значение составило 16 [10; 16] мм/ч.
С целью дообследования и проведения дифференциальной диагностики между различными хирургическими, гинекологическими и урологическими заболеваниями в ряде наблюдений были выполнены рентгенография брюшной полости в поисках свободного газа и уровней жидкости (12), УЗИ органов брюшной полости (7), УЗИ органов малого таза у женщин (8), обзорная урография (12), УЗИ почек (6), экстренная эзофагогастродуоденоскопия (1), экскреторная урография (1), колоноскопия (1). Данные, полученные при перечисленных инструментальных методах исследования, чаще всего были неспецифичны, позволяли исключить другие заболевания брюшной полости и малого таза, но не давали возможности диагностировать перекрут и некроз отростков.
На основании данных рентгенографии брюшной полости выявлен умеренный пневматоз толстой кишки у 4 больных, пневматоз тонкой кишки и единичный уровень жидкости в тонкой кишке у 2 из 12 больных. По данным УЗИ органов брюшной полости обнаружены свободная жидкость в брюшной полости (1), инфильтрат (2; не подтверждено интраоперационными данными).
Интерес представляет больная, поступившая в плановом порядке для полипэктомии по поводу полипа сигмовидной кишки, однако при колоноскопии изменений не обнаружено. Это заставило уточнить анамнез (боли в нижних отделах живота) и назначить консультацию гинеколога, УЗИ органов малого таза. По данным УЗИ малого таза выявлено образование размером до 32 мм, расположенное медиальнее левого яичника и интимно к нему прилежащее, гипоэхогенной ячеистой структуры без кровотока при ЦДК. Выполнена лапароскопия с целью дифференциальной диагностики между цистаденомой яичника с перекрутом в анамнезе и перекрутом отростка кишки (интраоперационно: перекрут отростка сигмовидной кишки). Остальным 7 больным, которым было выполнено УЗИ органов малого таза, на основании обнаруженных изменений и клинических данных поставлены диагнозы гинекологических заболеваний, не подтвержденные интраоперационными данными.
Обзорная урография (12), УЗИ почек (6), экскреторная урография (1) проводились с целью дифференциальной диагностики с почечной коликой на предоперационном этапе, лишь в одном наблюдении нельзя было исключить этот диагноз. Экстренная эзофагогастродуоденоскопия (1) была выполнена на операционном столе в связи с предоперационным диагнозом перфорации язвы луковицы двенадцатиперстной кишки, однако язв и эрозий обнаружено не было.
Ряду больных были назначены консультации специалистов. 24 (55,8%) пациенткам назначена консультация гинеколога, 14 из них был поставлен диагноз острых гинекологических заболеваний. 19 (21,8%) пациентов были консультированы урологом, лишь у 1 из них нельзя было исключить диагноз правосторонней почечной колики. Больные с сопутствующими заболеваниями терапевтического и неврологического профиля консультированы перед лапароскопическим вмешательством терапевтом (11) и неврологом (1), противопоказаний к операции выявлено не было.
Перекрут и некроз отростков по результатам обследования до операции был заподозрен у 30 (34,5%) больных. У 7 (8,0%) из них он был основным диагнозом в предоперационном эпикризе, у 25 (27,5%) подозревался при проведении дифференциальной диагностики с другими острыми хирургическими и гинекологическими заболеваниями. У остальных 57 (65,5%) больных показанием к оперативному вмешательству послужили подозрение на другие острые хирургические и гинекологические заболевания органов брюшной полости и необходимость дифференциальной диагностики между ними. Основные диагнозы в предоперационном эпикризе, по поводу которых выполнялось лапароскопическое вмешательство, представлены в табл. 3
.
Наиболее частыми предоперационными диагнозами были острый аппендицит (51,7%), дивертикулез с дивертикулитом (13,8%), перфорация полого органа (6,9%), цистаденома яичника (5,7%), апоплексия яичника (3,4%). Стоит отметить, что трудности диагностики перекрута и некроза отростков приводили к тому, что у большинства больных — 60 (68,9%) — лапароскопическое вмешательство проводилось с целью дифференциальной диагностики между несколькими хирургическими — 52 (59,7%), хирургическими и гинекологическими — 6 (6,9%) и несколькими гинекологическими — 2 (2,3%) заболеваниями органов брюшной полости. У 58 (66,7%) больных дифференциальная диагностика проводилась между двумя заболеваниями. У одного больного проводилась дифференциальная диагностика между тремя заболеваниями (острым аппендицитом, острым мезаденитом и перекрутом и некрозом отростка), у одного больного — между четырьмя заболеваниями (дивертикулезом левой половины толстой кишки с дивертикулитом, опухолью толстой кишки с перифокальным воспалением, перекрутом и некрозом отростка и сигмоидитом). Лишь у 27 (31,1%) больных лапароскопическое вмешательство было предпринято в связи с подозрением на наличие какого-либо одного заболевания.
Лапароскопические вмешательства в 74 (85,1%) наблюдениях были выполнены в первые 6 ч после поступления. В среднем время от момента поступления до лапароскопического вмешательства составило 3 [2; 4] ч. 3 больных были оперированы более чем через сутки после поступления: 2 поступившие для планового лечения и 1 получавшая консервативное лечение в связи с диагнозом болевой формы апоплексии яичника.
Лапароскопическая ревизия брюшной полости позволила установить диагноз перекрута и некроза отростков у 84 (96,6%) из 87 больных. У остальных 3 (3,4%) больных диагноз перекрута и некроза отростков был установлен после конверсии, произведенной в связи с наличием плотного инфильтрата брюшной полости (2) и небезопасностью вскрытия абсцесса малого таза, стенкой которого являлась стенка мочевого пузыря (1).
Лапароскопическое лечение перекрута и некроза отростков проведено у 79 (90,8%) из 87 больных. Удаление перекрученных и некротизированных отростков с применением монополярной коагуляции произведено в 61 (77,2%) наблюдении, клипирования — в 9 (11,4%), лигирования — в 1 наблюдении. Самоампутировавшиеся при манипуляциях некротизированные отростки удалены в 7 из 79 наблюдений. У одной больной выполнено иссечение гидатиды маточной трубы, которая вызвала перекрут отростка, после чего отросток признан жизнеспособным и не удалялся.
У остальных 8 (9,2%) больных измененный отросток удален путем лигирования и последующего отсечения ножницами во время лапаротомии. Причинами конверсии у этих 8 больных послужили плотная фиксация отростка к стенке кишки (3), плотный инфильтрат брюшной полости (2), абсцесс малого таза (1), сочетанные заболевания — перфорация дивертикула (1), острый гангренозно-перфоративный аппендицит с ретроцекальным ретроперитонеальным расположением червеобразного отростка (1).
Дооперационная диагностика заболеваний отростков осложняется также возможным сочетанием перекрута и некроза отростков с другими заболеваниями органов брюшной полости и малого таза. Сочетанные заболевания по данным лапароскопического вмешательства были выявлены у 20 (23,0%) больных (табл. 4)
.
Сочетанное лапароскопическое вмешательство выполнено в 8 (9,2%) наблюдениях, в том числе адгезиолизис (4), удаление гидатиды маточной трубы (2), лапароскопическая аппендэктомия (2), электрокоагуляция очагов эндометриоза (1), вскрытие и коагуляция напряженной кисты желтого тела (1).
Интраабдоминальных осложнений не было. Послеоперационное осложнение в ближайшем послеоперационном периоде наблюдалось у 1 из 79 больных, которым было выполнено лапароскопическое лечение перекрута и некроза отростков. На 9-е сутки после лапароскопического вмешательства у этого больного был выявлен инфильтрат в проекции раны в левой подвздошной области; на 11-е сутки диагностирован неполный наружный толстокишечный свищ. Развитие этого осложнения, по-видимому, было связано с наличием сочетанного заболевания — дивертикулеза левой половины толстой кишки и микроперфорации дивертикула с последующим образованием наружного толстокишечного свища через дренажный ход, что подтверждалось данными фистулографии и ирригоскопии. Послеоперационный период после лапароскопического вмешательства у большинства больных с перекрутом и некрозом отростков протекал без осложнений. Средняя длительность пребывания в стационаре после операции составила 5 [5; 8] сут.
Летальный исход после лапароскопического лечения перекрута и некроза отростков имел место у 1 больной из 79 через 25 ч после вмешательства.
Больная Л.
, 76 лет, с выраженными сопутствующими терапевтическими (ишемическая болезнь сердца — стенокардия напряжения IV функционального класса, гипертоническая болезнь III стадии, пароксизмальная форма мерцательной аритмии на фоне атеросклеротического кардиосклероза) и неврологическими (атеросклероз сосудов головного мозга, 2 перенесенных острых нарушения мозгового кровообращения с развитием правостороннего гемипареза и дизартрии) заболеваниями поступила в клинику в тяжелом состоянии. В результате обследования возникло подозрение на мезентериальный тромбоз, перитонит в нижних отделах живота, в связи с чем было принято решение о выполнении диагностической лапароскопии. После подготовки в условиях отделения реанимации через 33 ч от начала заболевания, 4 ч после поступления больная была оперирована, диагностирован перекрут и некроз отростка сигмовидной кишки. Произведено лапароскопическое удаление некротизированного отростка путем коагуляции его ножки (в течение 10 мин). Лапароскопическое вмешательство без особенностей, с интраабдоминальным давлением 8 мм рт.ст. Летальный исход был связан с пароксизмом мерцательной аритмии и развитием ишемического инсульта в височно-лобной области левого полушария головного мозга, возникшем через 25 ч после лапароскопического вмешательства.
В 8 наблюдениях была произведена конверсия, при этом осложнение в ближайшем послеоперационном периоде развилось у 1 больной, у которой на 9-е сутки после удаления некротизированного отростка, аппендэктомии (по поводу некроза отростка сигмовидной кишки, вторичного аппендицита) при снятии швов выявлена гематома послеоперационной раны. В последующем проводили консервативное лечение: эвакуацию гематомы, санирующие перевязки, повязки с левомеколем, химотрипсином, обезболивающую и десенсибилизирующую терапию; отмечено медленное заживление раны вторичным натяжением, что было связано с наличием у пациентки сахарного диабета II типа.
Рецидив заболевания отростка после лапароскопического лечения отмечен у 1 (1,3%) из 79 больных. У больной Г.
, 25 лет, через 28 дней после лапароскопического удаления некротизированного отростка сигмовидной кишки произошел рецидив заболевания с появлением аналогичной клинической картины, напоминающей таковую при остром аппендиците. Выполнена диагностическая лапароскопия, при которой выявлены перекрут и некроз отростка восходящей ободочной кишки; произведено его лапароскопическое удаление с использованием монополярной электрокоагуляции с благоприятным исходом.
Таким образом, клиническая картина и данные лабораторно-инструментальных методов исследования при перекруте и некрозе отростков скудны и неспецифичны, что существенно затрудняет дооперационную диагностику данного заболевания. Предположение о наличии перекрута и некроза отростков до операции возникает в 34,5% наблюдений. В неясных диагностических ситуациях лапароскопия является методом выбора и позволяет диагностировать перекрут и некроз отростков в 96,6% наблюдений. Успешное оперативное лечение с применением лапароскопического доступа возможно в 90,8% наблюдений.
Чем оканчивается некроз
Благоприятный исход патологии будет при ферментативном расплавлении тканей, прорастании соединительных тканей в оставшуюся омертвевшую ткань с последующим образованием рубца. Участок некроза может обрасти соединительными тканями, в результате чего, происходит образование капсулы. Кроме этого, в омертвевшем участке способна образовываться кость. Это явление называют оссификацией.
Неблагоприятный исход патологического состояния характеризуется гнойным расплавлением, вследствие этого повышается риск возникновения кровотечения, распространения очага. Так будет происходить развитие сепсиса.
При ишемическом инсульте, инфаркте миокарда, некрозе почки или поджелудочной железы, то есть когда поражаются жизненно важные органы, высока вероятность смертельного исхода.