Авторы: Marco Di Serafino, Valerio Vitale, Rosa Severino, Luigi Barbuto, Norberto Vezzali, Federica Ferro, Eugenio Rossi, Maria Grazia Caprio, Valeria Raia, Gianfranco Vallone
Анатомия, техника и сонографические аспекты
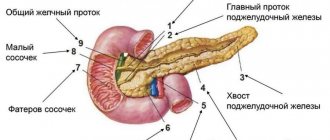
Поджелудочная железа расположена в переднем околопочечном пространстве, в забрюшинном пространстве, и направлена наклонно, а ее головная часть расположена справа, на уровне ниже хвоста. Головка заключена в дуоденальной впадине, а хвост – между желудком и селезенкой. Верхние чревные сосуды, наряду с верхними сосудами брыжейки и осью селезеночной вены, представляют собой важный анатомический ориентир для поджелудочной железы (рис. 1).
Рисунок 1: Схематическое изображение анатомических ориентиров поджелудочной железы: она расположена в забрюшинном пространстве, впереди основных брюшных сосудов и поясничного отдела позвоночника. Селезеночная вена – важный анатомический ориентир (звездочка). Поджелудочная железа разделена на головку (1) справа, тело (2) посередине и хвост (3) слева.
На УЗИ железы лучше визуализируются у детей, чем у взрослых, из-за их меньшего размера и относительно большой левой доли печени, которая служит акустическим окном, а также легко распознаваемой из-за нескольких важных анатомических ориентиров, таких как аорта, нижняя полая вена, селезеночная вена и мезентериальные сосуды.
Обследование поджелудочной железы обычно начинается с поперечного сканирования, за которым следуют продольное и наклонное сканирование с использованием левой доли печени в качестве акустического окна для головки и тела (рис. 2), селезенки для хвоста (рис. 3) и, наконец, окна желудка, наполненного водой для визуализации тела перешейка (рис. 4).
Рисунок 2: Продольное ультразвуковое сканирование эпигастрия от медиального до латерального направления. Головка и тело поджелудочной железы (звездочка) идентифицируются через акустическое окно левой доли печени (стрелка).
Рисунок 3: Продольное (а) и поперечное (b) УЗИ левого подреберья. Хвост поджелудочной железы идентифицируется через акустическое окно селезенки.
Рисунок 4: Поперечное эпигастральное УЗИ. Тело перешейка поджелудочной железы (звездочка) хорошо отображается, если окно кишечника расширено водой. Слева направо прогрессивное наполнение желудка.
Общее соотношение размера железы к размеру тела пациента с возрастом уменьшается. Обычно у детей головка поджелудочной железы относительно более выражена, чем тело и хвост, и это не следует принимать за патологические процессы.
Поджелудочная железа в основном растет в течение первого года жизни, медленнее между 2-м и 18-м годом, увеличивая свой передне-задний диаметр (диаметр а – р) со временем (рис. 5 и таблица 1).
Рисунок 5: Поперечное эпигастральное УЗИ поджелудочной железы. Для оценки диаметра железы измеряют переднезадний диаметр поджелудочной железы (штангенциркуль). Головка (a), тело (b) и хвост (c) атрофированной поджелудочной железы.
Таблица 1.
| Возраст | Головка | Тело | Хвост |
| Новорожденные | 0.5–1.0 | 0.5–1.1 | 0.5–0.8 |
| 0-6 | 1.0–1.9 | 0.4–1.0 | 0.8–1.6 |
| 7-12 | 1.7–2.0 | 0.6–1.0 | 1.3–1.6 |
| 13-18 | 1.8–2.2 | 0.7–1.2 | 0.3–1.9 |
Обычно экоструктура поджелудочной железы изоэхогенна или немного более эхогенна по сравнению с печенью, потому что паренхима замещена фиброзом и жиром, но менее выражена из-за ее железистой структуры, которая вызывает несколько границ раздела (рис. 6); Вирсунгов проток также идентифицируется при УЗИ как трубчатая безэховая структура (рис. 7). Средний диаметр протока поджелудочной железы у здоровых детей составляет 1,65 ± 0,45 мм.
Рисунок 6: Косое УЗИ поджелудочной железы в эпигастрии с пациентом в положении на правом боку. Поджелудочная железа ориентирована горизонтально и характеризуется однородной эхоструктурой, которая может выглядеть как гипоэхогенной (а), так и гиперэхогенной (b).
Рисунок 7: Поперечное эпигастральное УЗИ поджелудочной железы. В поджелудочной железе, которая кажется изогипоэхогенной, имеется тонкая анэхогенная трубчатая структура, представляющая канал Вирсунга (наконечники стрел).
Признаки тяжелой патологии
Несмотря на многообразие клинических проявлений патологий, при которых может увеличиваться поджелудочная железа, некоторые симптомы могут говорить о наличии патологического процесса в органе. Особое внимание следует обратить на следующие явления:
- горький привкус во рту, отрыжка;
- снижение аппетита вплоть до полного его отсутствия, тошнота и рвота после еды;
- диарея или запоры;
- болезненные ощущения в верхней части живота или под ребрами. Нередко боль отдает в спину или левую руку, иногда она может быть жгучей.
Если перечисленные выше симптомы сопровождаются повышенной температурой тела, следует заподозрить воспаление железы – панкреатит. Обычно в таких случаях клиническая картина возникает быстро, постепенно усиливается. Нередко это сопровождается значительным ухудшением общего состояния.
Воспаление поджелудочной часто сопровождается повышением температуры
Если же у ребенка увеличен хвост поджелудочной железы, проявления болезни появятся не сразу. Возможно возникновение небольшого жжения в районе верхней части живота, снижения аппетита или тошноты. Если у малыша отмечается регулярное появление таких симптомов, стоит как можно раньше обратиться к врачу.
Своевременная диагностика очень важна для предотвращения осложнений болезни. Это связано с тем, что поджелудочная железа расположена близко к другим органам пищеварительной системы. Поэтому при увеличении головки может возникнуть кишечная непроходимость.
Анатомические варианты
Анатомические аномалии поджелудочной железы классифицируются как аномалии слияния (pancreas divisum), миграция аномальной кольцевидной поджелудочной железы (эктопическая поджелудочная железа) или аномалия дупликации (изменение количества или формы).
Деление поджелудочной железы возникает в результате нарушения слияния вентрального и дорсального зачатков. Вентральный (Вирсунгов) проток дренирует только вентральный зачаток поджелудочной железы, тогда как большая часть железы впадает в малый сосочек через дорсальный (Санторини) проток.
По оценкам, заболеваемость варьирует примерно от 5 до 10% населения. Его не часто идентифицируют с помощью сонографии, хотя его можно легко распознать, когда протоки эктазичны, а также при течение панкреатита (рис. 8).
Рисунок 8: Поперечное эпигастральное УЗИ поджелудочной железы. Pancreas divisum: дорсальный проток поджелудочной железы (стрелка) находится в непосредственной связи с протоком Санторини; вентральный канал Вирсунга (наконечник стрелки) впадает в просвет кишки. Обратите внимание на увеличенную головку поджелудочной железы (пунктирная двунаправленная стрелка) при остром панкреатите.
Кольцевидная поджелудочная железа – редкая врожденная аномалия, характеризующаяся тем, что ткани поджелудочной железы полностью или не полностью покрывают нисходящую двенадцатиперстную кишку. Распространенность составляет примерно 1 на 2000 человек. Это часто связано с другими врожденными аномалиями, такими как атрезия пищевода, неперфорированный задний проход, врожденные пороки сердца, мальротация средней кишки и синдром Дауна.
Было предложено два типа: экстрамуральный подтип, когда вентральный проток поджелудочной железы окружает двенадцатиперстную кишку, чтобы присоединиться к главному протоку поджелудочной железы, и интрамуральный подтип, где ткань поджелудочной железы смешивается с мышечными волокнами стенки двенадцатиперстной кишки, а многочисленные небольшие протоки впадают непосредственно в двенадцатиперстную кишку. Он может иметь широкий диапазон клинической степени тяжести и может поражать новорожденных и пожилых людей, что затрудняет диагностику.
Примерно у половины пациентов с дуоденальной непроходимостью в неонатальном возрасте может наблюдаться «двойной пузырь» на рентгенограмме брюшной полости, если непроходимость полная. Это состояние трудно подтвердить с помощью УЗИ, но округлая головка поджелудочной железы и проксимальная часть двенадцатиперстной кишки, проходящая через головку, должны вызывать подозрение. Магнитно-резонансная томография (МРТ) легко подтверждает диагноз; последний метод визуализации предпочтителен для оценки как поджелудочной железы, так и протоков (рис. 9).
Рисунок 9: Поперечное эпигастральное УЗИ поджелудочной железы. Кольцевидная поджелудочная железа: головка поджелудочной железы, окружающая двенадцатиперстную кишку, с нормальной перистальтикой (верхняя линия a – c). Кольцевая поджелудочная железа хорошо видна на МРТ (нижняя строка).
Лечение хронического панкреатита у детей
Отек поджелудочной железы при остром панкреатите (компьютерная томограмма)
По современным представлениям ХП — это воспалительно-дегенеративный процесс в ПЖ, конечной стадией которого является фиброз паренхимы с постепенным снижением экзокринной и эндокринной функций.
Этиология
| Применение октреотида при хроническом панкреатите дает возможность быстро купировать боль и снизить ферментативную активность |
Среди множества этиологических факторов панкреатита у детей ведущую роль играет патология двенадцатиперстной кишки
(41,8%),
желчевыводящих путей
(41,3%),
аномалии развития железы, травмы живота.
Другими причинами ХП могут быть
инфекции
(эпидемический паротит, вирусы гепатита, энтеровирусы, сальмонеллез и др.), гельминтозы и другие заболевания, в частности, болезни соединительной ткани, гиперлипидемии, чаще I и V типа, гиперкальциемия, хроническая почечная недостаточность. Известно токсическое действие некоторых
лекарственных препаратов
(кортикостероиды, сульфаниламиды, цитостатики, фуросемид и др.) на ацинарную ткань. Особое место среди причин занимает наследственный панкреатит, муковисцидоз, синдром Швахмана, изолированный дефицит панкреатических ферментов и другие
наследственные болезни
, протекающие с панкреатической недостаточностью. По нашим данным,
ХП у детей в большинстве случаев развивается вторично, а как первичное заболевание встречается только у 14% больных
[1,4].
Патогенез
| Использование антипротеазв педиатрии целесообразно на начальных этапах панкреатита, так как подавляя трипсиновую и кининовую активность, они предотвращает формирование системных осложнений |
Как известно, основными патогенетическими механизмами развития большинства форм ХП является внутрипротоковая гипертензия
и активация панкреатических ферментов (
аутолиз
), что приводит к отеку, некрозу и в дальнейшем, при рецидивировании процесса, к склерозированию паренхимы. Поэтому при выборе лечебной программы при ХП необходимо учитывать особенности клинико-морфологических вариантов: интерстициально-отечного, паренхиматозного, фиброзно-склеротического, кистозного [5, 6].
Лечение
Просмотреть
[ ]
ХП у детей требует индивидуального терапевтического подхода. В период обострения показаны пребывание ребенка в стационаре, создание физиологического покоя и щажение больного органа, что обеспечивает назначение седативных средств, постельный режим.
Диетотерапия
Просмотреть
[ ]
Важное место в комплексе консервативных мероприятий принадлежит лечебному питанию, основная цель
которого состоит
в снижении панкреатической секреции
. Хорошо известна высокая чувствительность больных с панкреатитами к качественному и количественному составу пищи. С помощью диеты снижается панкреатическая секреция, облегчается всасывание пищевых ингредиентов и компенсируются энергетические и пластические потребности организма.
При составлении панкреатической диеты (стол № 5п) необходимо учитывать возраст больного, физический статус, период болезни, особенности метаболических процессов, наличие сопутствующей гастроэнтерологической патологии, режим питания, способ кулинарной обработки. Диета в фазе обострения
панкреатита характеризуется физиологическим содержанием белка, умеренным ограничением жиров, углеводов и максимально полным исключением экстрактивных веществ и сокогонных продуктов (сырые овощи, фрукты, соки). В
первые дни
выраженного обострения рекомендуется воздержание от приема пищи. Разрешается отвар шиповника, несладкий чай, щелочные минеральные воды (Боржоми, Славяновская, Смирновская). Постоянно с помощью назогастрального зонда производят аспирацию желудочного содержимого.
| Заместительная ферментная терапия направлена на ликвидацию нарушений абсорбции жиров, белков и углеводов, которые наблюдаются при тяжелом течении панкреатита |
По мере стихания симптомов болезни постепенно переходят к пероральному приему пищи, соблюдая принцип частого и дробного кормления. В рацион вводят протертые каши, протертый творог, молочный кисель, а с 5-го дня
— овощной протертый суп, овощные пюре,
на 7-8-й день
паровые фрикадельки и котлеты, отварную рыбу (стол №5 (панкреатический) — протертая пища). Через
2-3 нед
добавляются фруктовые и овощные соки, небольшими порциями в дополнение к пище, а затем — свежие овощи и фрукты. Через 1-1,5 мес ребенка переводят на расширенную диету 5п (непротертая пища). Больным запрещены крепкие вегетарианские навары, мясные, рыбные бульоны, жирные сорта мяса, рыбы, жареные, копченые продукты, грубая клетчатка, острые закуски, приправы, консервы, колбасы, свежеиспеченный хлеб, мороженое, холодные и газированные напитки, шоколад. Однако абсолютный запрет перечисленных продуктов нередко вызывает у больных ощущение неполноценности, поэтому при хорошем состоянии допустимо прибегать к ?зигзагам? в диете [2, 5].
В фазе стихания
панкреатита назначают щадящее питание, обеспечивающее физиологическую потребность в основных пищевых веществах и энергии. Рекомендуется увеличение белка на 25% от возрастной нормы. Основная цель диетотерапии в
фазе ремиссии
направлена на профилактику рецидива, для этого используют вариант диеты №5 п в течение 5-6 мес.
Просмотреть
[ ]
Медикаментозная терапия
Важнейшее значение в остром периоде панкреатита имеет ликвидация болевого синдрома
. Необходимо проводить лечебные мероприятия направленные на устранение причин, вызывающих боль. В арсенале медикаментозных средств должны быть холино- и спазмолитики, анальгетики, Н2-блокаторы гистаминовых рецепторов, антациды, ферментные и антиферментные препараты [7 — 9]. С анальгезирующей целью назначаются
спазмолитики
— но-шпа, папаверин, эуфиллин, в сочетании с простыми анальгетиками, которые в первые дни обострения вводят парентерально, а по мере улучшения состояния — внутрь. Это позволяет ликвидировать спазм сфинктера Одди, снизить внутрипротоковое давление и обеспечить пассаж панкреатического сока и желчи в двенадцатиперстную кишку. Традиционно и успешно при обострении ХП для торможения желудочной и панкреатической секреции используются
антихолинергические средства
(0,1% раствор атропина, 0,2% раствор платифиллина, 0,1 % раствор метацина и др.).
Важнейшее значение в остром периоде панкреатита имеет . Необходимо проводить лечебные мероприятия направленные на устранение причин, вызывающих боль. В арсенале медикаментозных средств должны быть холино- и спазмолитики, анальгетики, Н-блокаторы гистаминовых рецепторов, антациды, ферментные и антиферментные препараты [7 — 9]. С анальгезирующей целью назначаются — но-шпа, папаверин, эуфиллин, в сочетании с простыми анальгетиками, которые в первые дни обострения вводят парентерально, а по мере улучшения состояния — внутрь. Это позволяет ликвидировать спазм сфинктера Одди, снизить внутрипротоковое давление и обеспечить пассаж панкреатического сока и желчи в двенадцатиперстную кишку. Традиционно и успешно при обострении ХП для торможения желудочной и панкреатической секреции используются (0,1% раствор атропина, 0,2% раствор платифиллина, 0,1 % раствор метацина и др.).
| Диспансеризация детей с ХП требует систематического этапного наблюдения, проведения ежеквартальных противорецидивных курсов заместительной ферментной терапии |
В последние годы с целью подавления желудочной секреции используют современные антисекреторные средства: селективные блокаторы Н2-гистаминовых рецепторов
— ранитидин, фамотидин, низатидин;
ингибиторы протонной помпы
— омепразол, лансопразол. Эти препараты назначают 1-2 раза в сутки или однократно на ночь в течение 2-3 нед.
Снижение стимулирующего действия соляной кислоты достигается назначением антацидных препаратов
на 3-4 нед: гастерин-гель (гель фосфата алюминия и пектин для перорального применения), гелусил и гелусил лак (магний и алюминий силикат), маалокс (гидроокись алюминия и магния), мегалак (кремнекислый водный алюминий-магний), протаб (гидроокись алюминия и магния, метилпосилоксан), ремагель (гидрооксиды алюминия и магния), топалкан (альгиновая кислота, гидроокись алюминия и гидрокарбонат магния, гидратированный кремний), фосфалюгель (коллоидный фосфат алюминия), тамс (карбонат кальция и карбонат магния).
Перспективным является использование регуляторных пептидов
. Средством выбора в терапии панкреатита следует считать октреотид — аналог эндогенного соматостатина — гуморального ингибитора экзокринной и эндокринной секреции ПЖ и кишечника (табл.1). Он также эффективен при желудочно-кишечных кровотечениях различного генеза, благодаря избирательным гемодинамическим эффектам [1, 5].
Как показывает наш опыт, применение октреотида дает возможность быстро купировать болевой синдром и снизить ферментативную активность. Курс терапии октреотидом не превышает 5-7 дней. Выраженных побочных явлений не отмечено. Уже после 1-2 инъекций у оперированных больных объем отделяемого по дренажу из протока или сальниковой сумки сокращается в 2-4 раза. В среднем через 3-5 нед происходит закрытие свищей. Быстро улучшается состояние больного, уменьшаются боли в животе, ликвидируется парез кишечника, нормализуется активность ферментов в крови и моче.
Дезинтоксикация
Особое значение в период выраженного обострения панкреатита приобретает инфузионная терапия
, направленная на устранение нарушений обмена веществ на фоне эндогенной интоксикации. С этой целью больному вводят гемодез, реополиглюкин, 5% раствор глюкозы, 10% раствор альбумина, свежезамороженную плазму, глюкозо-новокаиновую смесь.
В детской гастроэнтерологии не утратили своего значения антиферментные препараты
— ингибиторы протеаз, действие которых направлено на инактивацию циркулирующего в крови трипсина. Назначение их показано при панкреатите, сопровождающемся высокой ферментемией, ферментурией, для ликвидации (феномена уклонения ферментов). По нашему мнению, несмотря на существующее в терапевтических и хирургических клиниках представления о невысокой эффективности антипротеаз даже при очень высоких дозах, использование этих препаратов в педиатрии особенно целесообразно при начальных этапах панкреатита, так как подавляя трипсиновую и кининовую активность, они предотвращают формирование системных проявлений (как следствие кининового взрыва и избыточной продукции интерлейкинов). В то же время они не оказывают влияния на активность ферментов, обладающих выраженным липолитическим действием [2, 4, 5, 8].
В период купирования обострения на фоне ограничения перорального питания очень важно назначение парентерального и энтерального питания.
Смеси аминокислот (аминостерил, аминосол, альвезин, полиамин и другие), вводят внутривенно капельно (30-40 капель в 1 мин). К ним рекомендуется добавление растворов электролитов (калия хлорид, кальция глюконат 1%) с учетом показателей кислотно-щелочного баланса. Наряду с ними используют жировые эмульсии для связывания активной липазы и восполнения дефицита жирных кислот в крови: 10-20% интралипид или липофундин внутривенно с гепарином капельно со скоростью 20-30 капель в 1 мин, из расчета 1-2 г жира на 1 кг веса.
Энтеральное питание
По мере исчезновения диспептических расстройств целесообразно переходить на энтеральное питание, главным преимуществом которого является уменьшение частоты развития осложнений. Следует отметить, что чем дистальнее вводятся в пищеварительный тракт нутриенты, тем меньше стимулируется экзокринная функция ПЖ [6, 7, 10].
Вводить смеси аминокислот
можно энтерально (интрадуоденально и даже интраеюнально) утром натощак, в подогретом до 37оС виде, в объеме от 50 до 200 мл в зависимости от возраста через день, курсом до 5-7 процедур. Такой путь введения аминокислот не дает побочных реакций, легко переносится больными и имеет отчетливый терапевтический эффект.
Энтеральное питание осуществляется смесями на основе гидролизатов белка
с высокой степенью гидролиза с включением среднецепочечных триглицеридов, продуктов на молочной основе низкожировых и с измененным жировым компонентом. Постепенно переходят на смеси с низкой степенью гидролиза (табл.2), так как эти продукты всасываются в кишечнике без предшествующей ферментации. Их можно вводить интрадуоденально в теплом виде через зонд.
Учитывая, что у большинства больных панкреатитом диагностируют значительные нарушения двигательной функции двенадцатиперстной кишки, желчевыводящих путей, чаще с явлениями дуоденостаза и гипомоторной дискинезии, в комплексе лечения показано использование прокинетиков.
Из них наиболее целесообразно отдавать предпочтение домперидону и цизаприду, как препаратам с минимальными побочными реакциями по сравнению с метоклопрамидом.
Патогенетическая терапия включает антигистаминные средства
(дифенгирдрамин, хлоропирамин, клемастин, прометазин), помимо основного действия они оказывают также седативный и противорвотный эффекты.
Антибактериальная терапия
показана для предупреждения вторичного инфицирования, при угрозе формирования кист и свищей, перитонита и развития других осложнений.
В восстановительный период возможно применение эссенциальных фосфолипидов, витаминных комплексов, антиоксидантов. Ввиду дефицита витаминов, особенно группы В и С, при ХП рекомендуется их парентеральное введение, а при легком течении — внутрь. Репаративные процессы в поджелудочной железе хорошо стимулируют препараты пиримидинового ряда (пентоксил, метилурацил), которые обладают ингибиторным, противовоспалительным, противоотечным действием [1].
Заместительная терапия
Сложным вопросом лечения панкреатической недостаточности является выбор ферментной терапии. Заместительная терапия ферментами направлена на ликвидацию нарушений абсорбции жиров, белков и углеводов, которые наблюдаются при тяжелом течении панкреатита (наследственный и посттравматический панкреатит). В большинстве случаев показано кратковременное (не более 2-4 нед) назначение ферментов прерывистыми курсами. Доза подбирается индивидуально до получения терапевтического эффекта. Сначала предпочтение отдается некомбинированным препаратам панкреатина, затем через 2-3 нед при стихании обострения используются ферменты с добавлением желчных кислот и/или гемицеллюлазы. Среди множества ферментных препаратов, как показали данные других авторов и наши собственные исследования, лучшим эффектом обладают микрогранулированные ферменты с кислотоустойчивой оболочкой, полученные по новым технологиям (ликреаза, креон, панцитрат), характеристика которых представлена в табл. 3, 4. Они отвечают требованиям к ферментным препаратам: отсутствие токсичности, побочных явлений, хорошая переносимость, оптимум действия в интервале рН 5-7, устойчивость к соляной кислоте, пепсину и другим протеазам, достаточное содержание активных пищеварительных ферментов.
Эффективность ферментов и адекватность используемой дозы оценивается по динамике клинических данных (исчезновение болевого и диспепсического синдромов), нормализации копрограммы и уровня ферментов дуоденального содержимого, крови и мочи, положительной динамике массы тела ребенка. Следует подчеркнуть, что у детей с ХП и гипосекреторным типом функции,
несмотря на клиническое улучшение, восстановления экзокринной функции не происходит, поэтому вопрос о заместительной ферментной терапии решается строго индивидуально. Длительное бесконтрольное применение этих препаратов подавляет собственную энзимную продукцию по механизму обратной связи. Абсолютным показанием к пожизненному назначению заместительной терапии является муковисцидоз, наследственный панкреатит, врожденный дефицит ферментов, синдром Швахмана.
Санаторно-курортное лечение
В период ремиссии больные могут быть направлены на санаторно-курортное лечение (Железноводск, Ессентуки, Боржоми, Трускавец, Моршин) и местные гастроэнтерологические санатории. Бальнеолечен е
основан на применении слаботермальных и термальных вод малой и средней минерализации. Ощелачивающее действие минеральных вод препятствует раннему закислению дуоденального содержимого, индуцирует продукцию эндогенного холецистокинина и секретина. Содержащиеся в воде ионы магния и кальция, как коферменты, значительно потенцируют действие секретина и других регуляторных пептидов, чем обеспечивают стимулирующее влияние на дегрануляцию зимогенных гранул, внутридуоденальную активность ферментов. Курс терапии составляет 24-30 дней, минеральную воду назначают из расчета 10-15 мл на год жизни ребенка в сутки, начиная с небольшого объема (1/3 суточной дозы) и однократного приема в первые дни, постепенно доводя при хорошей переносимости до полной дозы при трехкратном приеме.
Грязелечение
(иловой, торфяной, сапропелевой грязью) проводят осторожно из-за опасности обострения. У детей применяют сегментарную аппликацию при невысокой температуре, курсом 8-10 процедур, с одновременным исследованием ферментов крови и мочи, клиническим обследованием больного.
Диспансеризация
Диспансеризация детей с ХП требует систематического этапного наблюдения, проведения ежеквартальных противорецидивных курсов заместительной ферментной терапии, витаминотерапии, репарантов, гепатопротекторов, физиолечения. Необходимо диетологическое воспитание ребенка и родителей, формирование традиций лечебного питания, с целью создания психологического комфорта в семье. Обязателен контроль за состоянием смежных органов пищеварения (по показаниям — проведение ЭГДС). Амбулаторно рекомендуется не реже чем 1 раз в 3 мес проводить копроскопию, контролировать уровень амилазы крови, мочи. Один раз в полгода — выполнять ультразвуковое исследование органов брюшной полости. При отсутствии эффекта от настойчивого консервативного лечения с использованием всех современных методов, при появлении осложнений больной наблюдается совместно педиатром и хирургом для решения вопроса о необходимости проведения оперативного лечения.
Литература
1. Заболевания органов пищеварения у детей / Под ред. А.А. Баранова, Е.В. Климанской, Г.В. Римарчук. М. 1996; 304 с.
1. Заболевания органов пищеварения у детей / Под ред. А.А. Баранова, Е.В. Климанской, Г.В. Римарчук. М. 1996; 304 с.
2. Руководство по гастроэнтерологии / Под общей ред. Ф.И. Комарова, А.Л. Гребенева. М., Медицина, 1996; 3: 719 с.
3. Римарчук Г.В. Современные аспекты диагностики хронического панкреатита у детей. Рос. педиатр. журнал 1998;1: 43-9.
4. ДиМагно Ю.П. Определение степени тяжести течения и лечение острого панкреатита. Рос. журн. гастроэнтерол., гепатол., колопроктол. 1998; 8 (5): 88-90.
5. Хазанов А.И. Лечение хронического панкреатита. Рос. журн. гастроэнтерол., гепатол., колопроктол. 1997; 7 (2): 87-92.
6. Хирургия поджелудочной железы, руководство для врачей / Под ред. М.В. Данилова, В.Д. Федорова. М., Медицина. 1995; 510 с.
7. Филин В.И., Костюченко А.Л. Неотложная панкреатология. СПб, Питер, 1994; 410 с.
8. Справочник практического врача по гастроэнтерологии / Под ред. В.Т. Ивашкина, С.И. Рапопорта. М., 1999; 426 с.
9. ДиМагно Ю.П. Осложнения хронического панкреатита. Рос. журн. гастроэнтерол., гепатол., колопроктол. 1998; 8 (5): 90-92.
10. McClave Stephen A. Comparison of the Safety of Early Enternal vs Parenteral Nutrition in Mild Acute Pancreatitis. J. of Parenteral and Enternal Nutrition 1997; 21 (1): 14-20.
Панкреатит
Острый панкреатит
– это воспалительный процесс поджелудочной железы, очаговый или диффузный, который определяется у детей как наличие по крайней мере двух из следующих трех критериев:
- боль в животе, совместимая с панкреатическим происхождением.
- амилаза и / или липаза, по крайней мере, в три раза превышающие верхние пределы нормы.
- результаты визуализации, предполагающие и / или совместимые с воспалением поджелудочной железы.
С точки зрения визуализации, острый панкреатит может проявляться как в незначительной (интерстициальный отек и некроз поджелудочной железы), так и в тяжелых формах (расширенный некроз жировой ткани, некроз паренхимы и кровоизлияние).
При УЗИ поджелудочная железа может демонстрировать разные модели визуализации. Незначительные формы могут иметь либо полностью нормальную железу (50% случаев), либо очаговое или диффузное увеличение объема со сниженной эхогенностью, связанной с отеком (рис. 10, 11), и плохо определенные ребер.
Также может присутствовать расширение протока поджелудочной железы. Протоки поджелудочной железы диаметром более 1,5 мм у детей в возрасте от 1 до 6 лет, более 1,9 мм в возрасте 7–12 лет или более 2,2 мм в возрасте 13–18 лет часто связаны с наличием острого панкреатита.
Перипанкреатическая жидкость – частая находка и наиболее часто обнаруживается в переднем околопочечном пространстве, малом мешочке, малом сальнике и поперечной ободочной кишке.
Более тяжелые формы характеризуются различными паттернами УЗИ в зависимости от времени обследования, степени паренхиматозного некроза, наличия кровоизлияния и степени экстрапанкреатической диффузии воспалительного процесса. Тем не менее, тяжелый острый некротический панкреатит и связанные с ним осложнения лучше всего демонстрируются на изображениях компьютерной томографии (КТ), а также на МРТ. Последние часто являются дополнительными к УЗИ.
Рисунок 10: Поперечное (а) и продольное (b, с) сканирование панкреатического пространства. Острый панкреатит: наблюдается увеличение объема поджелудочной железы, что также характеризуется слегка гипоэхогенной эхоструктурой и размытыми краями из-за отека (а, b, звездочка); кроме того, имеются скопления анэхогенной жидкости в забрюшинном околопочечном пространстве, рядом с правой почкой (c, стрелки).
Рисунок 11: Поперечное (а) и продольное (b, с) сканирование панкреатического пространства. Острый панкреатит: наблюдается значительное увеличение объема железы, особенно головки (b, желтые стрелки); кроме того, имеется небольшое скопление околопочечной жидкости (а, белая стрелка).
Хронический панкреатит
в детском возрасте встречается крайне редко и связан с наследственными и семейными заболеваниями (наследственный панкреатит, аминокислотный хронический панкреатит и хронический геморрагический панкреатит).
При УЗИ объем и эхоструктура поджелудочной железы сохраняются в 70% случаев. В оставшихся 30% мы можем найти некоторые патогномоничные находки: расширение Вирсунгового протока (30%) (рис. 12), кальцификаты (10%) (рис. 13), псевдокисты (10%) (рис. 14). Последние развиваются из острой коллекции, и на их формирование может уйти несколько недель. Большинство из них проходят спонтанно, но могут возникнуть такие осложнения, как инфекция, кровотечение, непроходимость желчных протоков или даже разрыв.
Рисунок 12: Пример случая у 17-летнего мальчика. Поперечное эпигастральное УЗИ поджелудочной железы. Множественные гиперэхогенные пятна с затуханием кзади из-за внутрипанкреатических кальцификатов (слева, стрелки); кроме того, имеется расширенный канал Вирсунга с признаками гиперэхогенного камня внутри (справа).
Рисунок 13: Поперечное эпигастральное УЗИ поджелудочной железы. Хронический панкреатит: небольшое диффузное увеличение эхоструктуры поджелудочной железы с более выраженными гиперэхогенными пятнами в головной части из-за кальцификатов паренхимы.
Рисунок 14: Поперечное эпигастральное УЗИ поджелудочной железы. Хронический панкреатит: прогрессивное сканирование (верхняя линия) от головки до хвоста поджелудочной железы с множественными диффузными кальцификациями и двумя скоплениями жидкости псевдокист (звездочка). МРТ (нижняя линия) с мультипланарной реконструкцией MRCP. Хронический панкреатит у того же пациента (см. Выше): аксиальные МРТ-изображения с Т1 после контрастирования (в центре и справа), подтвердили два вышеуказанных скопления жидкости псевдокист (звездочка) без связи с протоком поджелудочной железы на MRCP (слева).
Аутоиммунный панкреатит
(АИП) становится все более широко признанным заболеванием, но данные о детях ограничены.
AИП встречается в двух формах (типы 1 и 2). Тип 2, по-видимому, чаще встречается у детей и связан с воспалительными заболеваниями кишечника и другими аутоиммунными заболеваниями. У взрослых диагноз аутоиммунного панкреатита 1 типа основан на повышенных уровнях иммуноглобулина G4 (IgG4). У детей повышение уровня IgG4 может отсутствовать даже при типичной гистологии.
При УЗИ можно увидеть диффузное или сегментарное увеличение поджелудочной железы со сниженной эхогенностью, связанное с флогозом, а также нерегулярное сужение протока поджелудочной железы, сдавленного паренхимой железы.
Симптомы реактивного панкреатита
Инфекционное заболевания может спровоцировать реактивный панкреатит.
Эта форма заболевания – наиболее часто отмечается у детей любого возраста. Практически любое инфекционное заболевание может спровоцировать реактивный панкреатит (отравление и следующий за ним гастроэнтерит, ОРВИ, ОРЗ).
Причиной его возникновения у грудных детей становится слишком раннее введение в рацион мясных блюд, различных приправ со взрослого стола, что затрудняет работу незрелой поджелудочной железы. Симптомы реактивного панкреатита у детей:
- Характер боли – резкая, опоясывающая. Боль уменьшается, если ребенок садится, наклонившись немного вперед.
- Локализация боли – выше пупка.
- Рвота содержимым желудка, сильная тошнота.
- Субфебрильная температура (37?С)в первые часы заболевания.
- Сильный понос.
- Обложенный белым налетом язык, жажда и ощущение сухости во рту.
- Ухудшение общего самочувствия, плаксивость.
- Повышенное газообразование.
Диагностирование проводится при помощи УЗИ органов брюшной полости, лабораторных исследований кала и биохимии крови.
Панкреатическая недостаточность
Муковисцидоз
Муковисцидоз (МВ) – рецессивное аутосомное наследственное заболевание, которое может не показывать каких-либо значимых результатов визуализации на ранних стадиях, но в конечном итоге может привести к внешнесекреторной недостаточности поджелудочной железы.
Паренхима поджелудочной железы замещается фиброзом и жиром, поэтому на более поздних стадиях она выглядит атрофичной, маленькой и гиперэхогенной (рис. 15). Жировая инфильтрация поджелудочной железы в МВ связана с увеличением мягкости при точечной эластографии сдвиговой волной (pSWE) (рис. 16); этот параметр может использоваться для мониторинга инволюции поджелудочной железы при этом прогрессирующем заболевании.
Кроме того, могут быть обнаружены небольшие ретенционные кисты (цистоз поджелудочной железы), обычно не более 3 мм, и области пониженной эхогенности из-за фиброза.
Рисунок 15: Поперечное эпигастральное УЗИ поджелудочной железы. Муковисцидоз: поджелудочная железа выглядит диффузно гиперэхогенной по сравнению с печенью из-за жировой инфильтрации.
Рисунок 16: Поперечное эпигастральное УЗИ поджелудочной железы. Измерение скорости поперечной волны в головке поджелудочной железы у пациента с муковисцидозом.
Панкреатит – редкое осложнение среди пациентов с МВ, которое следует учитывать при наличии предполагающих клинических признаков.
Наконец, УЗИ поджелудочной железы у детей, страдающих муковисцидозом, всегда необходимо интегрировать с оценкой печени, поскольку первичная патология часто может сосуществовать с билиарным циррозом (рис.17).
Рисунок 17: Продольные ультразвуковые исследования правой доли печени. Муковисцидоз: диффузные эхоструктурные изменения печени с чередованием гипоэхогенных и гиперэхогенных участков. Также производится измерение скоростей поперечных волн.
Синдром Швахмана-Даймонда
Синдром Швахмана-Даймонда (СШД) – редкое аутосомно-рецессивное мультисистемное заболевание, характеризующееся внешнесекреторной недостаточностью поджелудочной железы, нарушением кроветворения и предрасположенностью к лейкемии.
Другие клинические особенности включают скелетные, иммунологические, печеночные и сердечные заболевания. При УЗИ диффузное повышение эхогенности поджелудочной железы, связанное с жировой инфильтрацией, типично для СШД (рис. 18).
Рисунок 18: Поперечное эпигастральное УЗИ поджелудочной железы (а, b). Синдром Швахмана-Даймонда: поджелудочная железа диффузно гиперэхогенная по сравнению с прилегающей левой долей печени из-за значительной жировой инфильтрации.
Периоды повышенного риска
Существует несколько периодов, когда у ребенка наиболее велика вероятность нарушения функции железы:
- при введении прикорма;
- смене грудного вскармливания на искусственное;
- в начале посещения детского сада;
- при переходе из детского сада в школу;
- в период полового созревания.
Как правило, в эти периоды изменяется обстановка, питание, эмоциональный фон ребенка. Все эти факторы могут повысить риск нарушения деятельности пищеварительной системы. Немаловажное влияние на здоровье оказывает и гормональный фон.
В такие периоды рекомендуется внимательно следить за состоянием ребенка. Если у него появляются какие-либо симптомы, связанные с повреждением поджелудочной, нужно обратиться к врачу и пройти обследование. Для определения характера и степени поражения органа следует выполнить УЗИ брюшной полости, а также применить лабораторные методы исследования.
Опухоли
Примитивные новообразования поджелудочной железы в детском возрасте встречаются довольно редко. Эти опухоли можно разделить на три основные группы: экзокринные, эндокринные и кистозные поражения
.
Чаще встречается вторичное поражение неходжкинской лимфомы, нейроэктодермических опухолей и забрюшинные новообразования (нейробластома).
Панкреатобластома – самая частая опухоль поджелудочной железы у детей раннего возраста. Это карцинома поджелудочной железы инфантильного типа с гистологическим сходством с нормальной эмбриональной поджелудочной железой на 8-й неделе беременности и демонстрирует повышенный уровень альфа-фетопротеина в одной трети случаев.
При УЗИ большая часть панкреатобластомы представляет собой четко очерченные гетерогенные образования с твердыми и кистозными компонентами. Кистозные образования гипоэхогенны с гиперэхогенными внутренними перегородками. Иногда обнаруживается гипоэхогенное твердое образование. Описаны врожденные случаи панкреатобластомы в сочетании с синдромом Беквита – Видемана, и они преимущественно кистозные.
Хотя панкреатобластома считается наиболее распространенной злокачественной опухолью у детей, недавние исследования показали, что солидное псевдопапиллярное эпителиальное новообразование (SPEN) является наиболее частой опухолью поджелудочной железы у детей.
SPEN – это поражение с низким потенциалом злокачественности, чаще всего поражающее женщин репродуктивного возраста. При УЗИ опухоль обычно выглядит как четко выраженная большая масса с различными характеристиками в зависимости от наличия кистозных и солидных компонентов, внутриопухолевого кровоизлияния и кальцификатов. Фиброзная капсула может быть идентифицирована как эхогенный или, реже, гипоэхогенный ободок.
Нейроэндокринные опухоли возникают из островковых клеток поджелудочной железы. При УЗИ инсулиномы обычно круглые или яйцевидные, гипоэхогенные с гиперэхогенным ободком. Опухоли с более крупными островковыми клетками, обычно злокачественные инсулиномы, гастриномы (или другие нейроэндокринные опухоли), могут иметь неоднородный ультразвуковой вид в зависимости от наличия кистозных областей, кровоизлияний, некроза и кальцификатов.
Несидиобластома представляет собой аналогичное опухолевое заболевание поджелудочной железы, характеризующееся новой дифференциацией островков Лангерганса от эпителия протоков поджелудочной железы с последующей гиперпродукцией инсулина. УЗИ показывает повышенную эхогенность и объем поджелудочной железы. Несидиобластоз часто связан с гипогликемией и синдромом Беквита – Видермана.
Более того, поджелудочная железа может быть вовлечена в неходжкинскую лимфому, особенно в крупноклеточную лимфому и спорадическую лимфому Беркитта. На УЗИ эти опухоли очень гипоэхогенные и могут по-разному проявляться в виде одиночных или множественных поражений или диффузной инфильтрации поджелудочной железы.
О заболевании
Из-за неправильного питания клетки поджелудочной железы погибают и вызывают воспалительный процесс.
Панкреатит – очень опасная патология поджелудочной железы, воспалительный процесс в которой может закончиться серьезными осложнениями. Из-за погрешностей в питании и прочих проблем клетки поджелудочной железы погибают, вызывая воспалительный процесс в окружающих тканях.
Нарушение функций железы приводит к застою продуцируемого ею сока, который вместо того, чтобы поступать в 12-перстную кишку, вызывает отек железы и разрушение ее тканей. Нехватка ферментов поджелудочного сока приводит к тому, что питательные вещества не поступают в кишечник и не стимулируют переваривание пищи.
Нарушается тщательно отлаженная система обеспечения питанием детского организма.В острых случаях боль при панкреатите может быть настолько сильной, что больной подвергается болевому шоку. Виды панкреатита у детей:
- Острая форма заболевания. Возникает после травмы, отравления, как последствия вирусной инфекции.
- Хроническая форма панкреатита. Возникает после недолеченного острого панкреатита, нарушения рекомендаций врача по поводу диеты и лечения, характеризуется частыми обострениями.
- Реактивная форма панкреатита. Возникает, как реакция на нарушения функций ЖКТ, как осложнение воспалительных процессов органов брюшной полости. После лечения основного заболевания — прогноз благоприятный.