- Главная
- Лечение рака (онкологии)
- Опухоли ЖКТ
- Операции при раке пищевода
—
—
—
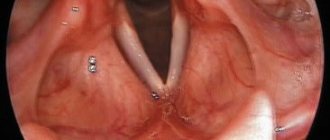
При раке пищевода злокачественная опухоль поражает сначала внутренний слой, слизистую оболочку, а затем наружный – подслизистый и мышечный слои.
Разделяют 2 типа данной патологии:
- Плоскоклеточный рак. Развивается в клетках слизистой оболочки пищевода. Возникает в районе шеи и грудной клетки.
- Железистый рак (аденокарцинома). Развивается в нижней части пищевода.
Основной способ лечения злокачественной опухоли в пищеводе – это операция. Рекомендуется хирургическое вмешательство в следующих случаях:
- Для полной резекции патологического очага.
- Для удаления максимальной части опухоли.
- Для восстановления ЖКТ после удаления пищевода.
- Для ослабления симптомов на позднем сроке при наличии метастаз.
Чтобы понять, какая именно операция необходима пациенту, врач смотрит на объем, степень и место патологического очага, на наличие или отсутствие ранее проведенных операций, на возраст и физическое состояние больного.
Малоинвазивные операции
- Дистанционные консультацияя
- Подберем лучшее лечение для вас
Перезвоните мне!
Реконструктивная хирургия рака пищевода
Данная операция помогает возобновить работу пищеварительного тракта после удаления злокачественной опухоли. Обычно проводится сразу после вырезания патологического очага.
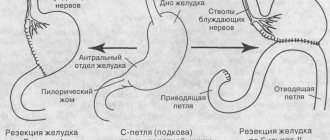
Пластика с помощью желудка
При резекции части или целого пищевода самый оптимальный выход – подтянуть желудок вверх, образовать из органа трубку и соединить с оставшемся сегментом пищевода. Такая процедура называется пищеводно-желудочной анастомоз.
Реконструкция с помощью толстого или тонкого кишечника
Бывают случаи, когда желудок невозможно задействовать в восстановительной операции. Тогда врач использует часть кишечника. Обычно это сегмент толстой или тонкой кишки.
Преимущества данной методики:
- безопасность: контролируемая глубина воздействия (снижает риск развития рубцовых изменений пищевода);
- эффективность: эрадикация (искоренение) после первой процедуры ≥ 90%;
- снижение риска “захороненного” Барретта за счёт контролируемого применения энергии и равномерного удаления эпителия;
- лёгкость в применении, не требует много времени: передача энергии
- быстрое восстановление нормальной слизистой;
- возможность применения при больших очагах;
- является минимальным вмешательством, не требует длительного пребывания в стационаре.
Европейское сообщество Гастроинтестинальной эндоскопии рекомендует РЧА как самую эффективную и безопасную методику лечения пищевода Барретта.
Подходы к хирургии при раке пищевода
Полостной (открытый) подход
При операции делают длинные разрезы в районе брюшной полости, груди или шеи. Далее питательную трубку располагают в желудке или средней части тонкой кишки. Это помогает пациенту восстановиться и получить нужное питание.
Трансхиатальный подход
Врач разрезает брюшную полость, освобождает внутренние органы от тканей и удаляет опухоль, часть желудка и некоторые лимфоузлы.
Возможен вариант, при котором разрезают левую сторону шеи, освобождают некоторые отделы пищевода от тканей и накладывают анастомоз.
Трансторакальный подход (подход Айвора-Льюиса)
Брюшная полость разрезается, желудок освобождают от тканей, грудь разрезают с правой стороны. Затем удаляют пищевод или какую-то его часть. Далее из желудка делают трубку и подключают к оставшемуся сегменту пищевода.
Торакоабдоминальный подход
Рекомендован, когда рак распространился на нижнюю часть пищевода или верхнюю часть желудка. Живот пациента разрезают от середины вверх, к левой части грудной клетки. Удаляют патологический очаг, а затем формируют трубку так же, как в предыдущем подходе.
Радикальная эзофагэктомия
Данную процедуру выполняют, когда рак 1-3 стадии распространился в нижней части пищевода и есть риск его распространения на другие органы. В ходе операции удаляют пищевод, ткани брюшной полости, лимфоузлы, селезенку, часть желудка. Иногда могут провести резекцию и других близ прилегающих органов. Далее желудок или часть кишечника подключают к оставшемуся пищеводу.
Лапароскопическая эзофагэктомия
Используют на начальной стадии рака. На теле человека делают 4-6 маленьких разреза и с помощью лапароскопа удаляют опухоль. После данной процедуры пациент быстрее восстанавливается, а риски получить осложнения уменьшаются.
Наш эксперт в этой сфере:
Рудакова Мария Николаевна
Заместитель главного врача, онколог-хирург, д.м.н
Доктор медицинских наук
Опыт работы: Более 30 лет
Позвонить врачу
Позвонить врачу
Отправьте документы на почту Возможность проведения лечения рассмотрит главный врач клиники.
Хирургическое лечение
ЗАПИСЬ НА КОНСУЛЬТАЦИЮ +7 (812) 951-7-951
Хирургическое лечение рака пищевода является одним из самых сложных разделов в хирургии и онкологии. При выборе объема оперативного вмешательства производится комплексное обследование больного. В комплекс обязательно, наряду с клиническими исследованиями (тщательный сбор анамнеза, осмотр, пальпация, перкуссия, аускультация, исследование показателей крови и мочи, функции внешнего дыхания, ЭКГ, соотношение роста и веса), включаются полипозиционное рентгенологическое исследование пищевода, рентгенологическое исследование легких и желудка, эндоскопическое исследование (эзофагоскопия, трахеобронхоскопия), ультразвуковое исследование органов брюшной полости (печень, поджелудочная железа, почки, клетчатка забрюшинного пространства в зоне развилки чревного ствола, парааортальной зоны) и средостения, а также компьютерную томографию (рентгеновскую или ЯМР). Кроме того, проводят обследование на наличие сопутствующих заболеваний. При выявлении сопутствующих заболеваний сердечно-сосудистой системы считаются функционально операбельными больные без клинических признаков декомпенсации или неустойчивой компенсации кровообращения, нестабильной стенокардии, некорригируемой артериальной гипертензии. Наличие признаков ишемии, рубцовых изменений миокарда, блокад, нарушений ритма сердца расцениваем как относительные противопоказания к операции, которые требуют углубленного исследования сердечно-сосудистой системы, коронарного кровообращения, толерантности к физической нагрузке. Функционально операбельными считаются пациенты с удовлетворительной толерантностью к физической нагрузке и отсутствии отрицательной динамики на ЭКГ. Абсолютными противопоказаниями к операции являются легочно-вентиляционная недостаточность IY степени и острый инфаркт миокарда в сроки до 6 мес. Риск операции повышен у больных с избытком веса более 20% и значительным его дефицитом. При сопутствующих заболеваниях почек и печени функционально операбельными считаются больные, у которых нет выраженных обострений интеркуррентных заболеваний и клинических и лабораторных признаков печеночно-почечной недостаточности. Завершающим этапом диагностики является ревизионная лапаротомию (абдоминальный этап) с целью окончательного решения вопроса о метастатическом распространении опухолевого процесса ниже диафрагмы. В зависимости от выработанного плана лечения абдоминальный этап может завершаться различным образом. В случаях обширного метастазирования в лимфатические узлы ниже диафрагмы, особенно в парааортальные и забрюшинные (исключая лимфатические узлы вдоль левой желудочной артерии и по верхнему краю поджелудочной железы в области хвоста и тела) абдоминальный этап завершается гастростомией. Наиболее простым в технике исполнения и надежным вариантом такой операции является формирование гастростомы стебельчатого типа из передней стенки желудка ближе к малой кривизне. Выбор показаний к операции определяется также уровнем поражения пищевода. Так чем выше локализуется опухоль пищевода, тем менее вероятно выполнение одномоментной резекции и пластики пищевода. Это связано с необходимостью дополнить хирургическое лечение лучевой терапией или химио-лучевым лечением, и сформированный при пластике искусственный пищевод неизбежно попадал бы в зону облучения, что является нежелательным. Иными словами, показания к операции того или иного объема в зависимости локализации опухолевого процесса в пищеводе следует рассматривать отдельно. Различия показаний к оперативному вмешательству того или иного объема, кроме локализации процесса зависят еще и от особенностей метастазирования рака пищевода и необходимости охвата лечебным воздействием разных зон регионарного метастазирования, а также от степени риска оперативного вмешательства вследствие различий в операционной травме. При раке шейного и верхнегрудного отдела пищевода при планировании объема операции следует отдать предпочтение экстирпации пищевода по методу Добромыслова-Торека. От одномоментной пластики пищевода следует воздержаться вследствие необходимости послеоперационной лучевой терапии на зоны регионарного метастазирования и ложе удаленного пищевода. К субтотальной резекции пищевода по Добромыслову-Тореку, отказываясь от одномоментной резекции и пластики пищевода следует прибегать в случаях паллиативных резекций пищевода, т. е. когда хирургу не удалось полностью удалить опухолевую ткань вследствие прямого прорастания опухоли в соседние анатомические структуры (аорту, главные бронхи, трахею, позвоночник, перикард), либо интимного спаяния с этими органами, а также обширного метастазирования в регионарные лимфатические узлы, доступные удалению, включая случаи с наличием метастазов по обе стороны диафрагмы. Эту операцию следует выполнять также при наличии у пациентов низких функциональных показателей, ограничивающих возможность выполнения травматичных, требующих много времени вмешательств. Пластика пищевода должна выполняться в этих случаях через 4-6 месяцев при отсутствии признаков прогрессирования заболевания по данным углубленного обследования. В остальных случаях, если процесс резектабелен, следует считать одномоментную резекцию и пластику пищевода операцией выбора. При раке нижнегрудного отдела пищевода, а также при поражении абдоминального сегмента пищевода и переходе на желудок показана одномоментная резекция и пластика пищевода изоперистальтическим стеблем из большой кривизны желудка с внеполостным шейным анастомозом. В некоторых случаях, при незначительной распространенности процесса (в пределах I-II стадии) при такой локализации опухолевого поражения может выполняться резекция нижнегрудного отдела пищевода и проксимального отдела желудка с наложением пищеводно-желудочного анастомоза под дугой или на уровне дуги аорты или операция Льюиса или Гэрлока. Оптимальным завершением одномоментной резекции и пластики пищевода можно считать формирование шейного внеполостного пищеводно-желудочного анастомоза. Внеполостное расположение анастомоза имеет еще и то преимущество, что при возникновении несостоятельности швов анастомоза не возникает фатальных последствий для больного. В ряде случаев в связи с операционной травматизацией оставшейся части пищевода и перемещения ее из заднего средостения на шею происходит нарушение ее питания. В этом случае медом выбора является отсроченное формирование шейного пищеводно-желудочного анастомоза. Отсроченная пластика пищевода выполняется, как сказано выше, через 4-6 месяцев после резекции пищевода, если нет признаков прогрессирования процесса. Мы являемся принципиальными стороннниками трубчатой эзофагопластики из большой кривизны желудка, но не отвергаем возможности использования для пластики пищевода других сегментов желудочно-кишечного тракта. Последнее важно в тех случаях, когда операции на пищеводе предшествовала операция на желудке (резекция того или иного объема или гастрэктомия). В случаях невозможности использования желудка в качестве материала для пластики пищевода используются варианты кишечной эзофагопластики, в том числе и свободной пересадкой сегмента тонкой кишки с микрохирургическими межсосудистыми анастомозами. К использованию микрохирургической техники прибегают также при необходимости реваскуляризации желудочной трубки в случаях повреждения правой желудочной артерии и вен, сопровождающих ее, а также в случаях недостаточности венозного оттока и развитии венозного застоя в венах желудочной трубки. Операции Абдоминальный этап. Задачей абдоминального этапа, прежде всего, является ревизия зон регионарного метастазирования ниже диафрагмы. Положение больного — на спине с валиком на уровне мечевидного отростка грудины. Доступ-верхне-срединная лапаротомия. Ревизия и мобилизация для ревизии. Правой рукой пальпаторно оценивают состояние паракардиальных правых и левых лимфатических узлов, узлов малого сальника и по ходу левой желудочной артерии. Для лучшей ориентации и оценки состояния лимфатических узлов в области развилки чревного ствола вскрывается сальниковая сумка в бессосудистом участке ближе к печени. Подозрительные по метастазированию лимфатические узлы верифицируют с помощью пункционной биопсии, в ряде случаев их удаляют для морфологического исследования, а также для исследования чувствительности опухоли к химиопрепаратам. Пальпаторно и визуально оценивают состояние поверхности печени. Подозрительные участки пунктируют. При отсутствии неудалимых метастазов в органы и регионарные лимфатические узлы ниже диафрагмы и локализации опухоли в среднегрудном отделе пищевода или в его нижней трети с переходом на желудок при резектабельном процессе возможно выполнение одномоментной резекции и пластики пищевода в самостоятельном хирургическом плане, либо, что предпочтительнее, в сочетании с послеоперационной лучевой терапией. Последний вариант в настоящее время является доминирующим. При локализации поражения в верхнегрудном и шейном отделе пищевода абдоминальный этап завершается гастростомией из передней стенки желудка. Затем выполняется экстирпация пищевода с формированием фарингостомы или — субтотальная резекция пищевода с формированием высокой эзофагостомы на шее. Техника гастростомии из передней стенки желудка достаточно проста: на переднюю стенку желудка у малой кривизны, отступя от привратника 8-10 см., накладывают лигатурную держалку. Вторую держалку накладывают в 6 см в дистальном направлении. С помощью держалок, поднимая переднюю стенку желудка, формируют складку и на нее в антиперистальтическом направлении накладываю/т бранши аппарата НЖКА-60 таким образом, чтобы сформировалась коническая трубка основанием к желудку. Линию механического шва перитонизируют отдельными узловыми серозно-мышечными швами. Верхушка сформированной трубки через дололнительный разрез в левом подреберье выводится наружу и фиксируется двумя швами к апоневрозу. Кожу при формировании дополнительного разреза лучше рассекать в горизонтальном направлении, а апоневроз- в вертикальном, с сохранением волокон прямой мышцы живота, которые раздвигают крючками Фарабефа. Проверяется брюшная полость на отсутствие кровотечения и после этого лапаротомная рана ушивается наглухо. Затем отсечением верхушки стебля вскрывается его просвет и формируется наружное отверстие гастростомы подшиванием слизистой к коже отдельными узловыми швами. Через отверстие гастростомы в желудок вводят тонкий резиновый зонд для питания и декомпрессии. В последующем, введением желудочных зондов с постепенно возрастающим диаметром ширины отверстия гастростомы доводится до оптимальной величины. Субтотальная резекция пищевода. Целью этой операции является удаление единым блоком грудного отдела пищевода с опухолью, окружающей пищевод клетчаткой, паратрахеальными, верхними и нижними трахеобронхиальными (бифуркационными), задними средостенными (околопищеводными) лимфатическими узлами. Положение больного на левом боку с валиком на уровне угла лопаток. Доступ:правосторонняя передне-боковая торакотомия по пятому межреберью при поражении верхней и средней трети пищевода и по шестому-при поражении его нижней трети. Пальпаторно и визуально оценивают состояние париетальной, висцеральной плевры и легочной ткани с целью обнаружения возможных метастазов. При отсутствии признаков опухолевой диссеминации по плевре легкое отводят кпереди. Пальпаторно оценивают состояние средостенных лимфатических узлов оценивают расположение, уровень и протяженность поражения пищевода. Далее приступают к мобилизации пищевода и ревизии средостения. Мобилизация для ревизии и ревизия. Пересекают нижнюю легочную связку и тупо мобилизуют легкое до нижней легочной вены, смещая лимфатические узлы к пищеводу. Над пищеводом спереди него и сзади на всем протяжении от диафрагмы до купола плевры рассекают медиастинальную плевру, оставляя на пищеводе полоску шириной около 3 см. Далее пальпаторно определяют верхний и нижний край опухоли, оценивают ее связь с позвоночником, аортой, трахеей, главными бронхами. Выше и ниже опухоли на расстоянии 3-4 см пальцем обходят вокруг пищевода, через образовавшиеся каналы проводят резиновые держалки. При потягивании за них еще раз оценивают возможность удаления пищевода.
Мобилизация для резекции. Тупым и острым путем с помощью зажимов и лигирования сосудистых образований выделяют пищевод с окружающей клетчаткой, околопищеводными лимфатическими узлами (от диафрагмы до верхне грудной апертуры), единым блоком с бифуркационными лимфатическими узлами. При этом по возможности нужно сохранять веточки блуждающих нервов, отходящие к легким. При мобилизации в средней трети пищевода пересекают и лигируют пищеводные артерии отходящие, как правило, от передней поверхности аорты. Ниже отхождения легочных ветвей блуждающие нервы пересекают. При прорастании опухолью непарной вены ее выделяют, прошивают аппаратом УС и дополнительно перевязывают. При отсутствии прорастания непарную вену сохраняют. После мобилизации пищевода и околопищеводной клетчатки на всем протяжении внутригрудного отдела пищевода надсекают пищеводно-диафрагмальную связку и мобилизуют пищевод в области пищеводного отверстия диафрагмы. Потягивая за пищевод в плевральную полость выводят кардиальный отдел желудка. На уровне кардиального жома пересекают блуждающие нервы, прошивают пищевод двумя аппаратами УО и пересекают между механическими швами. Проксимальный конец пищевода помещают в резиновый колпачок или укрывают салфеткой. Дистальную линию механического шва погружают узловыми швами, затем ушивают пищеводное отверстие диафрагмы. Проксимальная граница резекции пищевода должна отстоять от верхнего края опухоли не менее 5 см. На этом уровне пищевод прошивают аппаратом УО и ниже накладывают зажим. Пересекают пищевод между аппаратом и зажимом. Препарат удаляют. Если опухоль локализуется в в верхней трети пищевода пищевод прошивают аппаратом УО и пересекают под куполом плевры. Производят срочное морфологическое исследования по проксимальному и дистальному краям резекции для исключения возможного пересечения пищевода по опухоли. Плевральная полость промывается растворами антисептков и после проверки на гемостаз и герметичность легкого(если производились манипуляции на нем) ушивают наглухо с оставлением двух плевральных дренажей(верхнего — на уровне 2 межреберья и нижнего -на уровне 7 межреберья). Шейный этап операции. В положении больного на спине с валиком на уровне лопаток и небольшим поворотом головы вправо послойно рассекают кожу и мягкие ткани по медиальному краю левой кивательной мышцы(грудино-ключично-сосцевидной) до претрахеальной фасциальной пластинки, рассекают ее продольно. Сосудистый пучок тупым крючком смещают кнаружи. В рану выводят оставшуюся часть шейного отдела пищевода и подшивают в глубине раны к окружающим мышцам, герметизируя средостение. Рану ушивают до пищевода. Мышечная стенка пищевода над механическим швом рассекается до подслизистого слоя. Часть пищевода с механическим швом удаляют. Слизистую подшивают к коже шеи. При получении данных срочного морфологического исследования о наличии опухолевых элементов в крае резекции дополнительно резецируют 1-2 см. пищевода и только затем формируют эзофагостому. В тех случаях, когда опухолевое поражение локализуется высоко, вплоть до глотки, производят экстирпацию оставшейся части пищевода. Для этого разрез продлевают выше, широко обнажают левую долю щитовидной железы, пересекают с лигированием нижнюю щитовидную артерию, проследив ход и сохранив левый возвратный нерв и паращитовидные тельца. Вытягивая культю пищевода мобилизуют ее до гортаноглотки. Край кивательной мышцы подшивают к предпозвоночной фасции в глубине раны. Этим достигается укрытие сосудистого пучка и герметизация верхнего средостения. Края кожи отсепаровываются в стороны. Вскрывается гортаноглотка, край кожи подшивается по краю остающейся части гортаноглотки в глубине раны, формируя боковую фарингостому. Отсроченная эзофагопластика изоперистальтическим стеблем из большой кривизны желудка. В положении больного на спине. Доступ- верхне-срединная лапаротомия. Послойно с иссечением послеоперационного (после абдоминального этапа) рубца вскрывается брюшная полость. Ревизия осуществляется также как при выполнении абдоминального этапа. При отсутствии опухолевой диссеминации по брюшной полости и неудалимых метастазов в регионарных зонах приступают к мобилизации желудка. Иссекается наружное отверстие гастростомы. Отверстие ее ушивается, а трубка перемещается в брюшную полость с предварительно ушитым устьем гастростомы. Желудок мобилизуется по большой кривизне от привратника до дна пересекая и лигируя желудочно-ободочную связку, отступя 5 см от стенки желудка с целью сохранения желудочно-сальниковых сосудов. В последующем эти сосуды будут основной магистралью кровообращения для искусственного пищевода. Короткие желудочные сосуды лигируют и пересекают непосредственно у ворот селезенки. Затем приступают к мобилизации желудка по малой кривизне. Ближе к печени лигируют и пересекают малый сальник на всем протяжении. На расстоянии ок 4-5 см лигируют и пересекают правую желудочную артерию. Вскрывают брюшину над желудочно-поджелудочной связкой. Клетчатку с лимфатическими узлами сдвигают к желудку выделяя левые желудочные артерию и вены. Артерию и вену пересекают и лигируют с прошиванием у места отхождения. Отступя от пилорического жома на 4-5 см по малой кривизне с помощью аппаратов УО-60 вдоль большой кривизны формируют желудочную трубку шириной 3-4 см. Для получения достаточной длины желудочной трубки желудок перед наложением сшивающих аппаратов растягивают вдоль большой кривизны. Для герметизации трубки между отдельными фрагментами механического шва последнюю скобку предыдущего шага включают в начало последующего. Линия механического шва укрывают узловыми серозно-мышечными швами. Сформированную желудочную трубку (около 38 см) проводят в заранее сформированный предгрудинный канал с предварительной резекцией мечевидного отростка грудины и укрытия места резекции брюшиной. Канал дренируют двумя парастебельчатыми резиновыми активными дренажами. Желудочную трубку фиксируют к фасции у начала предгрудинного канала. При укладывании искусственного пищевода стараются чтобы верхний конец трубки заходил за нижний конец оставшейся части пищевода на 3-4 см с целью создания лучших условий для формирования шейного пищеводно-желудочного анастомоза в последствии. После проверки на гемостаз лапаротомную рану ушивают наглухо. Формирование шейного пищеводно-желудочного анастомоза. Мобилизуют конец собственного пищевода окаймляющим разрезом вокруг эзофагостомы на протяжении ок 3 см. Рассекают циркулярно вокруг стомы мышечную оболочку, затем отсекают слизистую. Рассекают по задне-правой стенке на уровне эзофагостомы стенку желудочной трубки на протяжении диаметра эзофагостомы до подслизистого слоя. Затем отдельными узловыми швами сшивают мышечные оболочки культи пищевода и желудочной трубки по задней губе формируемого анастомоза. Вскрывают просвет желудочной трубки и формируют второй ряд швов анастомоза внутрипросветными узловыми швами по передней и задней полуокружностям анастомоза. Затем формируют второй ряд серозно-мышечных швов на передней стенке анастомоза. Оптимальным является формирование анастомоза по типу «конец — в бок». Кожа над анастомозом зашивается до устья верхушки желудочной трубки где формируется отверстие гастростомы подшиванием слизистой к коже. В отверстие гастростомы вводят тонкий резиновый зонд для питания и декомпрессии. При отсутствии уверенности в качестве кровоснабжения искусственного пищевода анастомоз формируют спустя 1-3 мес. Техника формирования анастомоза может варьировать в зависимости от склонности хирурга к тому или иному техническому варианту. Одномоментная резекция и пластика пищевода. Целью операции является удаление пищевода с клетчаткой, лимфатическими узлами паратрахеальной, бифуркационной, задне-средостенной, левой и правой паракардиальной; малого сальника групп лимфатических узлов, а также лимфатических узлов по ходу левой желудочной артерии и малой кривизны желудка. Доступ-комбинированный: верхне-срединная лапаротомия и переднебоковая правосторонняя торакотомия. Операция начинается в положении больного на спине. Абдоминальный этап заканчивается ревизией. При отсутствии признаков отдаленного метастазирования накладывают провизорные швы на лапаротомную рану. Больного поворачивают на левый бок. Далее осуществляется ревизия и мобилизация пищевода как и при операции субтотальной резекции с той разницей, что пищевод пересекают только по проксимальной границе резекции после мобилизации его в области пищеводного отверстия диафрагмы. Пищевод с опухолью, лимфатическими узлами и клетчаткой перемещается в брюшную полость. Плевральную полость после проверки на гемостаз и дренирования по вышеописанной методике ушивают наглухо. В положении больного на спине выполняют шейный этап с выведением шейного отрезка пищевода в рану. Снимают провизорные швы с лапаротомной раны. Резецируют мечевидный отросток грудины, формируют и тампонируют подкожный канал. Далее мобилизуют желудок как при отсроченной пластике пищевода и формируют желудочную трубку. Препарат с клетчаткой средостения, малого сальника, паракардиальной и клетчаткой желудочно-поджелудочной связки вместе с расположенными в ней лимфатическими узлами, а также малой кривизной желудка удаляют. Желудочную трубку помещают в заранее сформированный и дренированный канал и фиксируют к фасции на уровне мечевидного отростка. Лапаротомную рану после проверки на гемостаз ушивают наглухо. Далее формируют шейные эзофагостому и гастростому. В случае хорошего кровоснабжения искусственного пищевода и культи собственного формируют шейный пищеводно-желудочный анастомоз по описанной выше методике. В противном случае-формируют отсроченный шейный пищеводно-желудочный анастомоз.
Поделиться ссылкой:
Паллиативные операции при раке пищевода
Операции также проводятся, чтобы остановить развитие метастазов. Главная цель такого хирургического вмешательства – облегчить состояние пациента, избавить его от проблем с глотанием, улучшить самочувствие и качество жизни.
Шунтирование
Данная процедура проводится, если невозможно поставить стент, а направление потока пищи или жидкости вокруг новообразования нужно изменить. Тогда желудок присоединяют к верхней части пищевода, минуя патологический очаг.
Эзофагэктомия
Делают только в том случае, если у врачей есть достаточная уверенность, что больной выживет после данной операции. Ведь в ходе хирургии вырезают почти весь пищевод, а оставшийся его сегмент соединяют с желудком.
Питательная трубка
Через нее пациент получает нужное количество питательных веществ, чтобы не потерять массу тела, и лекарства. Если есть метастазы и другие способы устранить блокировку, спровоцированную новообразованием, не помогают, то используют зонд. Его вставляют в желудок через нос (назогастральный зонд) или в тонкую кишку.
Часто задаваемые вопросы
Нужна ли специальная подготовка к операции при ахалазии кардии?
Хирургическое вмешательство проводится натощак, последний прием пищи, как минимум, за 8 часов до процедуры. Обо всех принимаемых медикаментах пациент должен заранее сообщить врачу, возможно, некоторые из них придется временно исключить.
Какие существуют виды операции при ахалазии кардии, помимо эзофагомиотомии?
Общепринятой методикой считается эндоскопическое бужирование пищевода, однако эффект от процедуры непродолжительный, а разрыв тканей и рубцы лишь ухудшают ситуацию. Однако этот метод может быть рекомендован пациентам старшего возраста с рецидивом ахалазии, в анамнезе у которых есть операция, а также тем, кому противопоказано хирургическое вмешательство. Кроме того, при лечении заболевания используется эндоскопическая интрасфинктерная инъекция ботулотоксина, рекомендованная пациентам, имеющим противопоказания к проведению операции. Однако эффект от этой методики длится всего лишь 2-3 месяца.
Какие осложнения возможны при операции по поводу ахалазии кардии?
Безусловно, теоретически существует вероятность развития интраоперационных осложнений, таких как перфорация пищевода, кровотечение, повреждение блуждающих нервов, раневая инфекция и др. Чтобы свести к минимуму вероятность их появления, лечение следует проводить в специализированной клинике, оснащенной современным оборудованием.
Особенности реабилитации после операции при ахалазии кардии?
Госпитализация длится, как правило, два дня, уже в день операции пациенту разрешается питье, со следующего дня — жидкая пища, рацион расширяется постепенно. Полное восстановление занимает обычно около 2 недель. Контрольный осмотр проводится через 2-3 недели после проведенной операции, в дальнейшем эндоскопическое исследование рекомендовано пройти через год после проведенного вмешательства с целью исключения диспластических изменений пищевода.
Отказ от операции — чем опасен?
Течение заболевания — медленно прогрессирующее, без операции ахалазия кардии способна привести к истончению стенок пищевода, что может вызвать развитие различных патологий, среди которых — варикозное расширение вен пищевода, дивертикулы, отслаивание подслизистого слоя и др. Кроме того, при отсутствии лечения возможно кровотечение, прободение стенки пищевода, общее истощение. Также возрастает риск развития злокачественной опухоли пищевода.
Теги: Общая хирургия Ахалазия кардии Грыжи ГПОД
Отзывы
16.11.2021
«Меня поразило, что врачи очень внимательны к пациентам, разъясняют все до мелочей»
В 2022 году 16 августа моя старшая сестра прилетела к нам Лобню, чтобы пройти обследование и, если нужно, лечение в онкоклинике НАКФФ.
Она живет в столице Кирг…
Читать весь отзыв
27.10.2021
В клинике, как дома
30.09.2021
Отзыв о лечении рака яичников в клинике НАКФФ
07.09.2021
Пациентка НАКФФ о лечении, быстрых обследованиях и внимательном отношении
Смотреть все отзывы
Стационар, госпитализация, скорая медицинская помощь – круглосуточно, без выходных
+7 (495) 259-44-44