Кровотечение прекращается самостоятельно приблизительно в 80% случаев. Продолжающееся кровотечение требует его остановки эндоскопическом способом в максимально короткие сроки. Если это невозможно, то прибегают к активной хирургической тактике. В отдельных случаях проводится эндоваскулярное вмешательство или консервативное лечение.
Основные задачи, возлагаемые на анестезиолога-реаниматолога при лечении больных с ЖКК:
- Проведение профилактики рецидива кровотечения после его остановки;
- Восстановление системной гемодинамики и других показателей гомеостаза. Естественно, что объем оказываемой помощи может варьироваться в широких пределах: от реанимационных мероприятий и до простого динамического наблюдения за больным;
- Оказание помощи при проведении эндоскопического вмешательства или хирургического вмешательства (если в этом возникла необходимость);
- Своевременное выявление рецидива кровотечения;
- В относительно редких случаях – проведение консервативного лечения кровотечения.
Последовательность оказания помощи
Если больной получал до возникновения кровотечения антикоагулянты, их, в большинстве случаев, следует отменить. Оценить по клиническим признакам тяжесть состояния и предполагаемый объем кровопотери. Рвота кровью, жидкий стул с кровью, мелена, изменение показателей гемодинамики – эти признаки говорят о продолжающемся кровотечении. Артериальная гипотония в положении лежа свидетельствует о большой кровопотере (более 20% ОЦК). Ортостатическая гипотония (снижение систолического АД выше 10 мм рт. ст. и увеличение ЧСС более 20 уд. мин при переходе в вертикальное положение) свидетельствует об умеренной кровопотере (10-20% ОЦК);
В наиболее тяжелых случаях может потребоваться интубация трахеи и проведение ИВЛ перед проведением эндоскопического вмешательства. Осуществить венозный доступ периферическим катетером достаточного диаметра (G14-18), в тяжелых случаях – установить второй периферический катетер или провести катетеризацию центральной вены.
Провести забор достаточного объема крови (обычно не менее 20 мл) для определения группы и Rh-фактора, совмещения крови и проведения лабораторных анализов: общего анализа крови, протромбинового и активированного частичного тромбопластинового времени, биохимических показателей.
Определение причины и оценка интенсивности кровотечения
Часто вероятную причину кровотечения можно определить по анамнезу.
Важно учитывать:
- симптомы диспепсии (особенно ночью);
- симптомы язвенной болезни желудка;
- побочные эффекты принимаемых лекарств, особенно ингибирующих свертывание крови, например, нестероидных противовоспалительных препаратов;
- вероятность злоупотребления алкоголем;
- наличие гепатита B или C — они могут указывать на цирроз печени и портальную гипертензию, как на возможные причины кровотечения.
Инфузионная терапия
Начать проведение инфузионной терапии с введения сбалансированных солевых растворов.
Важно! Если есть признаки продолжающегося кровотечения или достигнут нестойкий гемостаз – артериальное давление надо поддерживать на минимально приемлемом уровне (САД 80-100 мм рт. ст.), т.е. инфузионная терапия должна быть не слишком агрессивной. Гемотрансфузии проводятся, если проведением адекватной инфузионной те-рапии не удается стабилизировать гемодинамику у пациента (АД, ЧСС). Рассмотреть необходимость гемотрансфузии:
– при снижении уровня гемоглобина ниже 70 г/л. при остановившемся кровотечении;
– при продолжающемся кровотечении, когда гемоглобин ниже 90-110 г/л.
При массивной кровопотере (больше 50-100% ОЦК) трансфузионное лечение проводится в соответствии с принципами «Гемостатической реанимации» . Считается, что каждая доза эритроцитарной массы (250-300 мл) повышает уровень гемоглобина на 10 г/л. Свежезамороженную плазму назначают при клинически значимой коагулопатии, в том числе, и медикаментозно индуцированной (например, пациент получает варфарин). И в случае массивной кровопотери (>50% ОЦК). Если надежный гемостаз достигнут, нет необходимости во введении СЗП даже при значительной кровопотере (более 30% ОЦК). Декстраны (полиглюкин, реополиглюкин), растворы гидроксиэтилкрахмала (ГЭК) могут усилить кровоточивость, и их применение не рекомендуется.
Как ставят диагноз
Врач осматривает пациента, оценивая его внешнее состояние, оттенок кожного покрова, слизистых. Затем измеряет артериальное давление — зачастую оно сниженное.
В условиях клиники пациент проходит общий анализ крови. По нему можно быстро получить представление об уровне гемоглобина, объеме других кровяных клеток. Дополнительно диагноз ставят по биохимическому анализу, однако его обычно назначают спустя несколько суток после начала кровопотери, так как химический состав крови при этом меняется лишь со временем.
Основная же диагностика касается обнаружения самой причины нарушения целостности сосудов. Для этого врачи используют следующие аппаратные обследования.
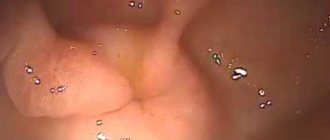
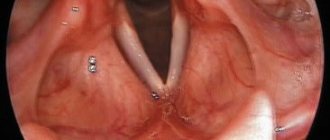
- Эндоскопия — изучение пищевода, желудка, 12-перстной кишки с помощью гибкой трубки с миниатюрной камерой позволяет оперативно обнаружить проблемное место;
- Контрастная рентгенография — эффективный метод обнаружения кровотечений в желудочно-кишечном тракте заключается во введении в орган безопасного контрастного раствора с последующим рентген-снимком;
- Магнитно-резонансная томография — современный метод, позволяющий получить исчерпывающие сведения о состоянии всех тканей того или иного органа ЖКТ.
Антисекреторная терапия
Оптимальные условия для реализации сосудисто-тромбоцитарного и гемокоагуляционного компонентов гемостаза создаются при рН > 4,0. В качестве антисекреторных препаратов используются ингибиторы протонной помпы и блока-торы H2-гистаминовых рецепторов.
Внимание! Одновременно назначать блокаторы H2-гистаминовых рецепторов и ингибиторы протонной помпы не целесообразно.
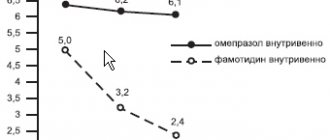
Лекарства обеих групп подавляют выработку соляной кислоты в желудке и тем самым создают условия для стойкого гемостаза кровоточащего сосуда. Но ингибиторы протонной помпы демонстрируют более стабильные результаты по снижению кислотности желудочного сока и значительно эффективнее снижают риск рецидива кровотечения. Антисекреторный эффект ингибиторов протонной помпы носит дозозависимый характер. Поэтому в настоящее время рекомендуют применение высоких доз препаратов, так что указанные ниже схемы назначения – это не описка автора.
Больным назначается в/в инфузия одного из перечисленных ниже ингибиторов протонной помпы:
- Омепразол (Лосек) в/в 80 мг в качестве нагрузочной дозы, с последующим введением 8 мг/час.
- Пантопразол (Контролок) в/в 80 мг в качестве нагрузочной дозы, с последующим введением 8 мг/час.
- Эзомепразол (Нексиум) в/в 80 мг в качестве нагрузочной дозы, с последующим введением 8 мг/час.
Нагрузочная доза препарата вводится приблизительно за полчаса. Внутривенное введение препарата продолжают в течение 48-72 часов, используя, в зависимости от возможностей, болюсный или непрерывный способ введения. В последующие дни переходят на пероральный прием препарата в суточной дозе 40 мг (для всех из перечисленных в этом абзаце ингибиторов протонной помпы). Ориентировочная длительность курса – 4 недели.
Внимание. Введение ингибиторов протонной помпы должно быть начато до проведения эндоскопического вмешательства, так как это уменьшает вероятность возникновения рецидива кровотечения.
При отсутствии ингибиторов протонной помпы, или их непереносимости больными, назначают в/в блокаторы H2-гистаминовых рецепторов:
- Ранитидин в/в по 50 мг через 6 часов или 50 мг в/в, затем 6,25 мг/час в/в. Через трое суток внутрь 150-300 мг 2-3 раза в сутки;
- Фамотидин в/в капельно по 20 мг через 12 часов. Внутрь с целью лечения применяют по 10-20 мг 2 раза/сут или по 40 мг 1 раз/сут.
Кто в зоне риска?
В основном, заболевания, которые приводят к кровяным истечениям, наблюдаются у взрослых. Причем, по статистике, у мужчин в 2 раза чаще, чем у женщин, диагностируют проблемы с органами желудочно-кишечного тракта — желудком, 12-перстной кишкой. Как мы уже отметили выше, первое место по количеству заболеваний удерживают язвенные патологии. Возрастной пик заболеваний — 40-45 лет.
Однако проблема встречается не только у взрослых. Диагноз, связанный с язвенными поражениями органов ЖКТ, зачастую ставят подросткам, которые бесконтрольно потребляют вредную пищу и напитки. Нередки и случаи образования кишечных полипов.
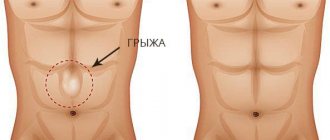
Желудочные и кишечные кровотечения все чаще обнаруживают даже у новорожденных детей. В основном, к ним приводит заворот кишок. У 3-летних детей истечение может быть вызвано образованием диафрагмальной грыжи, а также аномалиями в развитии органов нижнего отдела ЖКТ.
Подготовка к проведению гастроскопии
После относительной стабилизации состояния пациента (САД более 80-90 мм рт. ст.) требуется провести эндоскопический осмотр, и если возможно, определить источник и осуществить остановку кровотечения.
Облегчить проведение гастроскопии на фоне продолжающегося кровотечения, позволяет следующий прием. За 20 минут до проведения вмешательства, больному внутривенно путем быстрой инфузии вводят эритромицин (250-300 мг эритромицина растворяют в 50 мл 0,9% р-ра хлорида натрия и вводят за 5 минут). Эритромицин способствует быстрой эвакуации крови в кишечник, и тем самым облегчает нахождение источника кровотечения. При относительно стабильной гемодинамике с этими же целями используют в/в введение 10 мг метоклопрамида.
У пациентов с клапанной патологией сердца, перед выполнением гастроскопии рекомендуется проведение антибиотикопрофилактики. Иногда для удаления из желудка сгустков крови (для облегчения проведения эндоскопического обследования), требуется введение желудочного зонда большого диаметра (24 Fr или более). Промывание желудка рекомендуется осуществлять водой комнатной температуры. После окончания процедуры зонд извлекается.
Использовать желудочный зонд с целью диагностики и контроля за кровотечением (при наличии возможности проведения эндоскопического обследования), в большинстве случаев, считается нецелесообразным.
Лечение острого язвенного кровотечения
О статье
3919
0
Регулярные выпуски «РМЖ» №15 от 09.07.2010 стр. 933
Рубрика: Гастроэнтерология
Авторы: Gralnek I.M. , Barkun A.N. , Bardou M.
Для цитирования:
Gralnek I.M., Barkun A.N., Bardou M. Лечение острого язвенного кровотечения. РМЖ. 2010;15:933.
Острое кровотечение из верхних отделов желудочно–кишечного тракта (ЖКТ), определяемое как кровотечение, источник которого располагается проксимальнее связки Трейтца, является частым и клинически важным состоянием, оказывающим существенное влияние на расходы здравоохранения во всех странах мира. Среди негативных последствий этого явления следует назвать повторное кровотечение и смерть, которая во многих случаях связана с декомпенсацией существующих заболеваний, вызванной острым кровотечением [1]. В настоящем обзоре речь пойдет о лечении пациентов с острым язвенным кровотечением.
Острое кровотечение из верхних отделов желудочно–кишечного тракта (ЖКТ), определяемое как кровотечение, источник которого располагается проксимальнее связки Трейтца, является частым и клинически важным состоянием, оказывающим существенное влияние на расходы здравоохранения во всех странах мира. Среди негативных последствий этого явления следует назвать повторное кровотечение и смерть, которая во многих случаях связана с декомпенсацией существующих заболеваний, вызванной острым кровотечением [1]. В настоящем обзоре речь пойдет о лечении пациентов с острым язвенным кровотечением. Эпидемиология Ежегодно в Соединенных Штатах Америки происходит 160 госпитализаций в связи с острым желудочно–кишечным кровотечением (ЖКК) на 100 тыс. жителей, что соответствует более чем 400 тыс. госпитализаций в год [2]. Большая часть (80–90%) эпизодов острого кровотечения не связана с варикозным расширением вен пищевода и вызван язвами желудка и двенадцатиперстной кишки [3]. Хотя в нескольких работах было высказано предположение, что число язвенных кровотечений в мире может снижаться [4], недавно были опубликованы данные о том, что частота их встречаемости составляет 60 на 100 тыс. населения [5], при этом все большее число подобных кровотечений связано с приемом ацетилсалициновой кислоты и нестероидных противовоспалительных препаратов (НПВП). Кроме того, в большинстве случаев язвенные кровотечения развиваются у пожилых, так как 68% случаев составляют люди в возрасте старше 60 лет, а 27% – в возрасте старше 80 лет [6]. Смертность от язвенных кровотечений продолжает оставаться высокой, находясь в пределах от 5 до 10% [1,3]. По существующим оценкам, непосредственные расходы на стационарное лечение пациентов с язвенными кровотечениями в Соединенных Штатах Америки превышают 2 млрд долларов в год [7]. Клиническая картина Первичное ведение пациентов Рвота с кровью и мелена являются наиболее частыми первыми проявлениями острого язвенного кровотечения. Мелена в некоторых случаях имеет место у пациентов с кровотечениями из нижних отделов ЖКТ (т.е. дистальной тонкой и толстой кишки), а у пациентов с кровотечением из верхних отделов может иметь место примесь крови в кале [8]. Важна оценка состояния гемодинамики, включающая тщательное измерение пульса и артериального давления (АД), в том числе анализ ортостатических изменений для оценки объема внутрисосудистой жидкости и проведения реанимационных мероприятий. У пациентов с острым язвенным кровотечением и значительным снижением объема внутрисосудистой жидкости отмечается тахикардия в покое (пульс более или равен 100 уд./мин), гипотензия (систолическое артериальное давление менее 100 мм рт.ст.) или значительные ортостатические изменения (ускорение пульса на 20 и более уд./мин или снижение АД на 20 и более мм рт.ст. при вставании) [9,10]. Также должны быть оценены состояние слизистых, вен шеи и объем выделяемой мочи, так как они косвенно отражают состояние внутрисосудистого объема жидкости [9]. Первой задачей лечения является восстановление потерь жидкости и гемодинамической стабильности. Необходимо начать введение кристаллоидных растворов с применением крупных венозных катетеров (например, двух периферических катетров 16–18–го размера или центрального катетера при невозможности установки периферических). В целях поддержания адекватной способности крови к транспортировке кислорода, особенно у пожилых людей с сопутствующими сердечно–сосудистыми заболеваниями, следует рассмотреть возможность применения кислорода и переливания плазмы крови и эритроцитов при наличии тахикардии, гипотензии или снижения уровня гемоглобина ниже 10 г/дцл [9,11]. При наличии показаний также следует проводить коррекцию коагулопатии [12]. Введение назогастрального зонда может быть весьма полезным на первичном этапе обследования пациента (особенно для определения тяжести заболевания), хотя мнение о ценности данной процедуры продолжает оставаться противоречивым [10]. Было высказано предположение, что наличие алой крови в аспирате из назогастрального зонда является плохим прогностическим признаком, указывающим на необходимость срочного эндоскопического обследования [10,13]. В то же время отсутствие крови или материла, напоминающего кофейную гущу, не является гарантией отсутствия кровотечения, так как у 15% подобных пациентов при эндоскопическом обследовании были выявлены поражения высокого риска [10]. Применение орогастральных зондов большого диаметра для промывания желудка (водой комнатной температуры) улучшает визуализацию желудочного дна при эндоскопии, но не результаты лечения [14]. Внутривенное введение эритромицина, являющегося агонистом рецепторов мотилина, усиливает перистальтику желудка и значительно улучшает визуализацию его слизистой при первичной эндоскопии. Однако повышение диагностической ценности эндоскопии или улучшение результатов лечения в результате введения эритромицина доказаны не были (табл. 1) [18]. Сортировка пациентов и определение риска Разработаны критерии, основанные на клинических признаках (т.е. не на данных эндоскопии), которые позволяют ускорить сортировку пациентов с острым ЖКК, выявить нуждающихся в срочном вмешательстве, прогнозировать риск осложнений и определить оптимальный метод лечения [19,20]. Шкала Blatchford, общепризнанный метод классификации степени риска, основанный на клинических и лабораторных данных, используется для прогнозирования необходимости медицинского вмешательства у пациентов с кровотечением из верхних отделов ЖКТ (табл. 2) [16]. Данный показатель может находиться в пределах от 0 до 23, при этом более высокие значения указывают на больший риск. Шкала Rockall является, вероятнее всего, наиболее известной системой определения риска при кровотечениях из верхних отделов ЖКТ, и ее эффективность была доказана в различных условиях (табл. 2) [17]. Клинический показатель Rockall (т.е. рассчитываемый до эндоскопии) получают исключительно на основании клинических данных непосредственно при поступлении. Полный показатель Rockall включает как клинические, так и эндоскопические данные и позволяет прогнозировать риск повторного кровотечения и смерти, он варьирует от 0 до 11 баллов, при этом более высокие значения указывают на более высокий риск. Оба эти показателя (Rockall и Blatchford) полезны в определении прогноза пациентов, поступающих с острым кровотечением из верхних отделов ЖКТ, и имеют общие черты, включая данные о гемодинамическом состоянии и сопутствующих заболеваниях; применение этих шкал позволяет снизить число экстренных эндоскопических вмешательств среди пациентов, имеющих низкий риск [21]. Предложены и другие методы определения риска [20]. В настоящее время рекомендуется применение подобных шкал в качестве дополнения к клинической оценке состояния больных. Эндоскопическая картина кровоточащей язвы может быть использована для прогнозирования повторного кровотечения на основании классификации Forrest, в которой выделяют категории от IA до III. К числу изменений высокого риска относят язвы с видимым сильным (категория IA) или слабым кровотечением (категория IB), видимым сосудом, описываемым как пигментированный выступ, без кровотечения (категория IIA) и закрепленным тромбом (определяемым как красное или черное образование аморфной консистенции, которое невозможно сместить путем отсасывания или полива водой под давлением) (категория IIB) (рис. 1A–1D). Поражения низкого риска включают плоские, пигментированные пятна (категория IIC) и язвы с чистым дном (категория III) (рис. 1E и 1F) [8,22–24]. Зависимость правильности определения категории язвы от квалификации специалиста, выполняющего исследование, низка [25]. При первичном эндоскопическом исследовании изменения высокого риска выявляются примерно в диапазоне от одной трети до половины случаев [3], при этом частота повторных кровотечений из этих язв составляет от 22 до 55%, если их не пытались лечить эндоскопически [8,22,24]. Для подтверждения самостоятельной диагностической ценности эндоскопического доплеровского ультразвукового исследования области кровотечения до и после воздействия на нее с целью остановки кровотечения в отношении определения риска необходимы дополнительные исследования [26]. Подходы к лечению Рекомендуется совместное лечение различными специалистами со своевременным привлечением специально подготовленного эндоскописта [9,19,27]. Подобная тактика требует круглосуточной доступности подобных специалистов в связи с тем, что ранняя эндоскопия (выполненная в течение 24 ч после обращения пациента) является краеугольным камнем лечения пациентов с острым кровотечением из верхних отделов ЖКТ и может улучшать отдельные результаты лечения (количество перелитой крови и длительность госпитализации) в случае пациентов, отнесенных к группе высокого риска. Ранняя эндоскопия также позволяет определить показания к безопасной выписке пациентов, отнесенных к группе низкого риска, таким образом снижая расходы на их лечение [19,28]. Целями ранней эндоскопии являются определение источника кровотечения, прогноза и проведение эндоскопического лечения при наличии показаний. Рекомендации по лечению касаются прежде всего первых 72 ч после поступления и эндоскопического обследования и лечения, так как риск повторного кровотечения наиболее высок именно в этот период (табл. 1) [24,29]. Пациенты из группы высокого риска Пациенты с высоким риском должны быть госпитализированы, им следует провести эндоскопическое исследование и назначить лечение. Необходимо определить нуждаются ли они в помещении в отделение интенсивной терапии или достаточно усиленного наблюдения в течение первых 24 ч, при этом общая длительность госпитализации составляет как правило около 72 ч. Пациентам с кровоточащими язвами, отнесенными к группе высокого риска при эндоскопии (активное кровотечение или видимый кровеносный сосуд), должен быть выполнен эндоскопический гемостаз, который снижает риск повторного кровотечения, экстренного оперативного вмешательства и смерти [19,27,30]. К числу современных методов эндоскопического вмешательства относят инъекции (например, физиологического раствора, вазоконстрикторов, склерозирующих веществ, препаратов, склеивающих ткани, или их комбинаций), термальные воздействия (контактные, такие как многополярная электрокоагуляция, и бесконтактные, такие как коагуляция с применением аргоновой плазмы) или механические воздействия (прежде всего эндоскопическое клипирование). Все методы эндоскопических вмешательств доказанно превосходят отсутствие какого–либо вмешательства [19,27]. В то же время добавление второго метода гемостаза (инъекции, термального воздействия) к введению адреналина (в физиологическом растворе в разведении 1 к 10 000) в еще большей степени снижает вероятность повторного кровотечения, оперативных вмешательств и смерти [31] по сравнению с только введением адреналина, которого следует избегать [27,32]. Хотя эффективность введения только склерозирующего вещества считается сомнительной, оно редко приводит к повреждению тканей [33]. Существующие рекомендации считают более предпочтительным комбинированное лечение (введение адреналина с целью достижения местной вазоконстрикции и облегчения визуализации кровоточащего сосуда с последующим термальным воздействием) [19], однако преимущества комбинированного лечения перед только термальным воздействием доказаны не окончательно [32]. Возможность эндоскопического лечения среди пациентов с высоким риском, имеющих закрепленный тромб, остается дискуссионным вопросом (табл. 1) [15,19,34–36]. Применение методов механического воздействия, прежде всего эндоскопической установки клипс, считается весьма перспективным [19]. Точная роль этого метода окончательно не определена, существующие данные указывают на эффективность, аналогичную только термальному воздействию, комбинации инъекции и контактного термального воздействия, а также установке клипс в сочетании с инъекцией [32,37]. Этот вопрос требует дальнейшего изучения. Возможно, в будущем оптимальный метод лечения будет зависеть от расположения и внешнего вида язвы. В настоящее время эндоскопистам следует применять те методы гемостаза, которые они лучше знают, так как все эти методы достаточно эффективны. Однако применение только инъекции эпинефрина является неоправданным. Точная роль новых методов эндоскопического гемостаза, таких как криотерапия, ушивание и применение металлических клипс, должна быть установлена в будущих исследованиях. Различные клинические и эндоскопические факторы были предложены для прогнозирования эффективности эндоскопического лечения у пациентов с язвенным кровотечением. Они включают наличие язвенной болезни в анамнезе, наличие язвенных кровотечений в анамнезе, поступление в состоянии шока, активное кровотечение во время эндоскопического исследования, большой размер язвы (более 2 см в диаметре), большой размер сосуда, из которого происходит кровотечение (
Возможные осложнения
Кровотечения из верхнего отдела желудочно-кишечного тракта опасны аспирацией дыхательных путей. Это означает, что рвотные массы с кровью могут попасть в нос или трахею, что вызовет пневмонию с высоким риском летального исхода. Профилактика аспирации обычно сводится к установке эндотрахеальной трубки. Особенно это необходимо больным, находящимся без сознания.
Также желудочно-кишечные кровотечения чреваты общими осложнениями на фоне обильной кровопотери (гиповолемии). Если в организме циркулирует недостаточное количество крови, повышается риск сердечной, почечной и мозговой недостаточности. При потере более 20% общего объема крови развивается угрожающее жизни состояние — геморрагический шок. В этом случае нарушается клеточный обмен, наступают кислородное голодание и интоксикация тканей. Прогноз На здоровье самих органов пищеварительного тракта эпизод кровотечения не сказывается. Однако он указывает на необходимость более тщательного контроля течения заболевания, которое его спровоцировало. В первые несколько недель могут наблюдаться признаки постгеморрагической анемии. Это вызывается падением концентрации гемоглобина на фоне обильной потери эритроцитов. В следующие полгода пациенту необходимо принимать препараты железа. Негативный прогноз имеет место при неоказании своевременной помощи во время кровотечения из желудочно-кишечного тракта. Москва и другие мегаполисы с затрудненным трафиком часто не позволяют быстро доставить больного в стационар. Смерть наступает в 5-20% случаев (в зависимости от локализации повреждения и общего состояния пациента).
Эндоскопическое лечение поврежденных сосудов
При язвенной болезни обычно прибегают к эндоскопической коагуляции сосудов. Спайка поврежденных стенок может проводиться при помощи электрических токов или лазера. В случае кровотечения из расширенных вен желудочно-кишечного тракта проводят: • Инъекционную склеротерапию — введение во внутреннюю оболочку стенки вены склерозантов. Эти препараты разрушают поврежденный участок, который в итоге рассасывается. В дальнейшем вена склеивается и становится беспросветной. • Эндоскопическое лигирование — механическое пережатие поврежденного участка. • Наложение портосистемного шунта для перенаправления потоков крови и снижения портального давления на расширенные вены.
Срочность проведения эндоскопии зависит от состояния пациента. Если оно тяжелое, лечение должно начаться не позднее 24 часов с момента кровотечения из желудочно-кишечного тракта.
Как организм справляется с потерей крови?
Если кровопотеря составляет не более 10%, организм способен восстановиться сам. Достигается это за счет внутренних компенсаторных механизмов: • Выделения надпочечниками катехоламинов сразу после начала кровотечения из пищеварительного тракта. Под действием этих веществ сосуды спазмируются, а скорость кровотока адаптируется к новым условиям. Это предотвращает прекращение кровоснабжения органов. • Выхода тканевой жидкости в сосуды. На третий день организм начинает расходовать запасы эритроцитов из селезенки для восстановления нормального объема крови. Однако это происходит в ущерб клеточному метаболизму. • Восстановления состава крови костным мозгом. Он стабилизируется максимум за три недели. Однако это не означает, что лечение желудочно-кишечного кровотечения необязательно. На практике организму сложно справиться с последствиями подобной компенсации. Поэтому медикаментозная поддержка ему все же требуется.