- Что такое острая кишечная непроходимость?
- Классификация
- Почему развивается острая кишечная непроходимость?
- Признаки кишечной непроходимости
- Чем опасна кишечная непроходимость?
- Что необходимо предпринять, чтобы спасти человека при кишечной непроходимости?
- Всегда ли необходимо выведение стомы во время операции по поводу кишечной непроходимости?
- Что происходит с выведенной стомой?
- Возможно ли помочь больному без операции?
Своевременная диагностика и лечение острой кишечной непроходимости, в том числе профилактика непроходимости путем эндоскопической установки стентов, позволяет сохранить высокое качество жизни у пациентов с онкологическими заболеваниями органов брюшной полости, а в ряде случаев и спасти жизнь. [1]
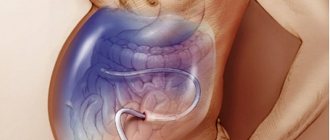
Что такое острая кишечная непроходимость?
Острая кишечная непроходимость – грозное, опасное для жизни осложнение многих заболеваний желудочно-кишечного тракта, в том числе опухолей собственно кишечника, а также опухолей других органов брюшной полости и забрюшинного пространства.[2]
Несмотря на успехи медицины, при неоказании своевременной медицинской помощи в первые 4-6 часов развития от острой кишечной непроходимости гибнет до 90% больных.
Пациентам с раком толстой и тонкой кишки, особенно на поздних стадиях заболевания, при наличии массивных метастазов в области ворот печени, важно знать первые признаки развития острой кишечной непроходимости, чтобы своевременно обратиться за медицинской помощью в лечебное учреждение.
Суть острой кишечной непроходимости состоит в быстром прекращении нормального физиологического прохождения (пассажа) пищи по пищеварительному тракту.
Кишечная непроходимость бывает полной или частичной. При частичной непроходимости пассаж пищи резко ограничен. Так, например, при стенозе (сдавлении) опухолевым конгломератом толстой кишки ее диаметр может уменьшиться до 1-3 мм. В результате через такое отверстие может проходить только небольшое количество пищи. Диагностируется такое поражение при проведении гастроскопии или колоноскопии, в зависимости от места развития сужения кишки.
Для прогноза лечения и исхода этого острого осложнения онкологического заболевания крайне важно знать, произошло ли нарушение пассажа пищи до или после связки Трейца, образованной складкой брюшины, подвешивающей двенадцатиперстную кишку. Соответственно поэтому выделяют высокую (тонкокишечную) и низкую (толстокишечную) непроходимость. [3]
Также прогноз лечения острой кишечной непроходимости определяется наличием или отсутствием механического препятствия. Если нет препятствия пассажу пищи в виде полного сдавления кишечной трубки, кишечная непроходимость называется динамической, которая в свою очередь бывает паралитической или спастической.
При наличии механического препятствия на пути пищи (чаще опухоли, отека прилежащих тканей, обусловленных опухолью, или спайки, в том числе возникшей вследствие ранее проведенных операций хирургического лечения рака), такая кишечная непроходимость называется механической (синоним — обтурационной).
При сдавлении брыжейки (складки брюшины, поддерживающей кишку, в которой проходят сосуды и нервы) кишечная непроходимость называется странгуляционной. [5,8]
При динамической кишечной непроходимости назначают консервативное лечение в условиях хирургического стационара. При механической и странгуляционной кишечной непроходимости лечение только хирургическое.
Каков прогноз?
В большинстве случаев кишечная непроходимость возникает при запущенных стадиях рака, поэтому вопрос стоит о том, как улучшить состояние пациента и продлить его жизнь, а не о том, как вылечить. Такое лечение называется паллиативным. Прогноз зависит от стадии опухоли и ряда других факторов.
Например, пятилетняя выживаемость на 4 стадии онкологических заболеваний, которые могут приводить к кишечной непроходимости, составляет:
- Рак ободочной кишки — 11%.
- Рак прямой кишки — 12%.
- Рак тонкой кишки — 10%.
- Рак желудка — 5%.
- Рак простаты — 29–100%.
- Рак матки — 15–17%.
- Рак яичников — 19%.
- Рак мочевого пузыря — 15%.
Классификация
Кишечная непроходимость не является самостоятельным заболеванием, а представляет собой симптом, в результате которого прекращается и нарушается прохождение содержимого по кишечнику. Согласно Международной классификации болезней 10 пересмотра (МКБ-10), данное состояние является осложнением других болезней, к которым относятся следующие нозологии: [7]
| Код | Нозология |
| K56 | Паралитический илеус и непроходимость кишечника без грыжи |
| K56.0 | Паралитический илеус |
| K56.1 | Инвагинация |
| K56.2 | Заворот кишок |
| K56.3 | Илеус, вызванный желчным камнем |
| K56.4 | Другой вид закрытия просвета кишечника |
| K56.5 | Кишечные сращения [спайки] с непроходимостью |
| K56.6 | Другая и неуточненная кишечная непроходимость |
| K56.7 | Илеус неуточненный |
Кроме того, кишечную непроходимость можно классифицировать по степени нарушения пассажа, по уровню непроходимости, по клиническому течению, по этиологии и степени компенсации.
По степени нарушения пассажа
- Полная. Пассаж кишечного содержимого полностью прекращен.
- Частичная. Пассаж кишечного содержимого частично сохранен.
По уровню непроходимости
- Высокая (при возникновении препятствия в правых отделах ободочной кишки).
- Низкая (препятствие возникает в левых отделах ободочной или в прямой кишке).
По клиническому течению
- Острая.
- Хроническая.
По этиологии возникновения
- Опухолевая. Опухоль может сдавливать кишечник снаружи, в таком случае говорят о функциональной обструкции. Если опухоль находится внутри кишечника – это механическая. Когда опухоль прорастает нервное сплетение, может возникать псевдонепроходимость.
- Неопухолевая. Причиной может быть снижение тонуса кишечника, запоры, каловые завалы, дивертикулит, инфаркт кишечной стенки, грыжи, спайки и т.д.
По степени компенсации
- Компенсированная. Возникает на фоне регулярных запоров с затруднением отхождения газов и задержкой стула.
- Субкомпенсированная. Задержка газов и стула не превышает 3 суток.
- Декомпенсированная. Задержка стула и газов превышает 3 суток, имеются рентгенологические признаки и тонко и толстокишечной непроходимости. [1,3,4]
Как проводится операция
Объем операции зависит от локализации и причины, вызвавшей кишечную непроходимость. Основной задачей хирурга является устранение этиологического фактора, исходя из этого возможно проведение нескольких видов операций:
- Рассечение спаек.
- Удаление части кишечника, в котором произошли непоправимые изменения. При благоприятных условиях два участка кишечника сшивают друг с другом. Если одномоментное восстановление кишечника не представляется возможным, то формируют стому (искусственный канал для опорожнения кишечника от каловых масс).
- Устранение заворотов, инвагинаций, узлообразований.
При возникновении непроходимости кишечника на фоне опухолевого процесса объем операции будет зависеть от локализации, стадии заболевания, осложнений, вызванных непроходимостью просвета кишечника.
Почему развивается острая кишечная непроходимость?
Среди факторов, предрасполагающих к механической кишечной непроходимости, наиболее часто встречаются:
- Спаечный процесс в брюшной полости (как следствие взаимодействия между опухолью и окружающими тканями, и как осложнение после операций по удалению первичного очага опухоли).
- Индивидуальные особенности строения кишечника (долихосигма, подвижная слепая кишка, дополнительные карманы и складки брюшины),
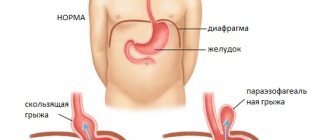
- Грыжи передней брюшной стенки и внутренние грыжи.
Механическая (обтурационная) кишечная непроходимость может возникнуть также вследствие сдавления кишечника опухолью извне или сужения просвета кишечника в результате воспаления. Важно знать, что механическая кишечная непродоходимость может развиться не только при опухолях кишечника, но и при раках других локализаций, например, раке почки, раке печени, раке мочевого пузыря, раке матки.
Паралитическая непроходимость может быть результатом травмы, перитонита, существенных нарушений обмена веществ, например, при низком уровне калия в крови. У онкологических больных паралитическая кишечная непроходимость может быть обусловлена декомпенсацией функции печени и почек, нарушением углеводного обмена при наличии таких сопутствующих заболеваний, как сахарный диабет и ряде других состояний.
Спастическая кишечная непроходимость развивается при поражениях головного или спинного мозга, отравления солями тяжёлых металлов (например, свинцом) и некоторых других состояниях. [9,10]
Подготовка и проведение операции
Перед началом операции пациенту необходимо пройти инструментальную диагностику и рентгенографию, сдать все необходимые анализы. При плановом поступлении за трое суток до хирургического вмешательства нужно исключить продукты, повышающие газообразование в организме. Запрещен прием пищи и употребление жидкости за 10 часов до проведения операции.
Первым этапом вмешательства является рассечение спаек между кишкой и брюшной стенкой. Таким способом освобождается необходимое место для хирургических манипуляций. Спаечные соединения между кишкой и брюшной стенкой рассекают острыми ножницами (холодный вид). Далее хирург после осмотра тонкой кишки восстанавливает проходимость на всем ее протяжении.
При завершении процесса устанавливают противоспаечные барьеры, которые снижают возможность образования повторных срастаний после операции спаечной болезни брюшной полости.
Признаки кишечной непроходимости
Ранний и обязательный симптом острой кишечной непроходимости — боль в животе. Боль может возникнуть внезапно без каких-либо предвестников, быть «схваткообразной», обычно она не зависит от приёма пищи. Приступы боли при острой кишечной непроходимости первое время повторяются примерно через равные промежутки времени и связаны с физиологическим волнообразным движением кишечника — перистальтикой. Спустя некоторое время боль в животе может стать постоянной.
При странгуляционной непроходимости боль сразу постоянная, с периодами усиления во время волны перистальтики. При этом стихание болей нужно расценивать как сигнал тревоги, поскольку говорит о прекращении перистальтической деятельности кишечника и возникновении пареза (паралича) кишечника.
При паралитической кишечной непроходимости боли в животе чаще тупые распирающие.
Симптомы разнятся в зависимости от высоты нарушения проходимости пищи – в области пищевода, желудка, двенадцатиперстной кишки или толстого кишечника. Задержка стула, включая его отсутствие с течение нескольких часов, отсутствие отхождения газов — это ранние симптомы низкой кишечной непроходимости.
При расположении механического сдавления, пареза или сужения в области верхних отделов кишечника, преимущественно в начале заболевания, при частичной проходимости кишечной трубки, под влиянием лечебных мероприятий, у пациента может быть стул за счёт опорожнения кишечника, расположенного ниже препятствия. Часто наблюдается тошнота и рвота, иногда многократная, неукротимая, усиливающаяся с нарастанием интоксикации.
Иногда отмечаются кровянистые выделения из заднего прохода.
При внимательном осмотре можно заметить существенное вздутие и выраженную асимметрию живота, видимую на глаз перистальтику кишок, которая затем постепенно угасает – «шум вначале, тишина в конце».
Общая интоксикация, слабость, снижение аппетита, апатия — эти симптомы наблюдаются у большинства больных с постепенным прогрессированием кишечной непроходимости от частичной до полной. [1,2]
Консервативное лечение
Иногда можно обойтись без операции. Обычно консервативное лечение кишечной непроходимости предполагает следующие меры:
- В желудок через нос вводят назогастральный зонд, чтобы обеспечить отток жидкости.
- Внутривенно вводят водно-солевые растворы.
- Назначают обезболивающие, противорвотные препараты, лекарства для улучшения работы кишечника и других внутренних органов.
- Состояние пациента постоянно контролируют.
Если эти меры не помогают, и состояние больного ухудшается, прибегают к хирургическому лечению. Консервативная терапия возможна лишь в определенных случаях, при определенных видах кишечной непроходимости. Чаще всего при онкологических заболеваниях необходима операция.
Чем опасна кишечная непроходимость?
Кишечная непроходимость приводит к обезвоживанию организма, выраженным сдвигам водно-электролитного и кислотно-щелочного баланса организма. В основе лежит нарушение поступления пищи, ее переваривания и всасывания, а также прекращения секреции желудочного и кишечного соков в просвет желудочно-кишечного тракта.
Поскольку ткани и клетки организма чувствительны к малейшим изменениям в химическом постоянстве внутренней среды, то такие сдвиги вызывают дисфункцию практически всех органов и систем. Наряду с жидкостью и электролитами при кишечной недостаточности за счёт голодания, рвоты, образования воспалительного экссудата теряется значительное количество белков (до 300 г/сут), особенно альбумина, играющего важную роль в гомеостазе. Наличие метастазов в области печени, которые угнетают белково-синтетическую функцию печени, дополнительно уменьшает уровень белка в крови, снижает онкотическое давление плазмы крови, что вызывает развитие стойких отеков.
Общая интоксикация организма при постепенном развитии кишечной непроходимости дополнительно ухудшается тем фактом, что в содержимом приводящего отдела кишечника начинаются процессы разложения и гниения, в содержимом просвета кишечника начинает размножаться патогенная микрофлора, накапливаются токсические продукты. При этом физиологические барьеры, в норме препятствующие всасыванию токсинов из кишечника, не работают и значительная часть токсических продуктов поступает в кровоток, усугубляя общую интоксикацию организма. В стенке кишки начинает развивается омертвение (некроз), итогом которого является гнойный перитонит из-за излития кишечного содержимого в брюшинную полость. При этом токсичные продукты распада тканей, микробные токсины, тяжелые метаболические сдвиги могут привести к сепсису и полиорганной недостаточности и гибели пациента. [5,11]
Что необходимо предпринять, чтобы спасти человека при кишечной непроходимости?
Развитие кишечной непроходимости – показание к срочной госпитализации в хирургический стационар, где безотлагательно производится:
- рентгенография брюшной полости,
- ультразвуковое исследование органов брюшной полости
- ирригография — рентгенологическое исследование с контрастной бариевой взвесью, вводимой в кишечник с помощью клизмы.
В нашей клинике мы часто используем жидкий контраст для лучшего контурирования кишечника и во избежание попадания бария в брюшинную полость во время последующей операции. При подтверждении диагноза и/или наличии выраженных клинических симптомов перитонита после очень короткой предоперационной подготовки проводится экстренное хирургическое вмешательство.
В отсутствие симптомов раздражения брюшины (перитонита) некоторое время (до суток) под наблюдением хирурга проводится консервативная терапия:
- регидратация,
- введение белковых растворов, электролитов,
- введение антибиотиков,
- освобождение верхних отделов пищеварительного тракта путем зондового промывания желудка,
- промывание кишечника,
- обезболивание и пр.
При отсутствии эффекта от консервативного лечения требуется выполнить операцию в плановом порядке. При возможности удалить причину непроходимости проводится диагностическая лапаротомия с резекцией кишечника. Во время операции обязательно проводится ревизия брюшной полости для уточнения причины развития острой кишечной непроходимости и определения общего объема операции. [2]
При обнаружении во время ревизии органов брюшной полости спаек, заворота, узлов петель, инвагинаций, производится их устранение. По возможности выполняется циторедуктивная операция по удалению первичного опухолевого очага, вызвавшего развитие острой кишечной непроходимости.
По существующим правилам удаление кишки при непроходимости должно проводиться на определенном расстоянии выше и ниже места непроходимости (обтурации). Если диаметр соединяемых отрезков ненамного отличается, выполняют анастомоз «конец в конец», при значительном различии диаметров приводящего и отводящего участков анастомоза – «бок в бок». В нашей клинике мы используем как классические методики ручного шва для формирования аностозов, так и современные сшивающие аппараты типа степлеров.
При тяжелом общем состоянии больного или невозможности формирования первичного анастомоза по другим причинам, например, из-за далеко зашедшего опухолевого процесса, формирования «опухолевого панциря», большой протяженности участка резецируемого кишечника, скопления большого объема жидкости в брюшной полости (асцита), на передней брюшной стенке формируется отверстие – колостома, в которую выводятся приводящий и отводящий отрезки кишки – «двухствольная стома».
В зависимости от участка кишки, из которого производится формирование колостомы данное оперативное вмешательство имеет различное наименование:
- наложение илеостомы – при выведении тонкой кишки,
- цекостома – слепой,
- асцендо-, десцендо- и трансверзостомы – соответственно восходящей, поперечный и нисходящий участки поперечноободочной кишки,
- при сигмостомии – из сигмовидной кишки.
При операции на сигмовидной кишке, называемой «операцией Гартмана» отводящий отрезок толстой кишки всегда ушивается наглухо и погружается в брюшную полость. [2,12]
Острая спаечная кишечная непроходимость является одним из наиболее грозных заболеваний органов брюшной полости, при этом операцию необходимо выполнить в течение 2 ч после того, как к ней были поставлены показания. Очень часто решение о необходимости экстренного вмешательства принимает дежурный хирург в ночное время или праздничные дни, когда рядом нет более опытных коллег. Вся ответственность за жизнь больного ложится на плечи порой молодого врача, который обязан самостоятельно произвести сложную операцию. Выйти с честью из такой ситуации можно, лишь неукоснительно соблюдая тактические установки и технические приемы, разработанные за многие годы врачами, занимающимися неотложной абдоминальной хирургией. Настоящая публикация содержит изложение основных приемов хирургической техники, позволяющих добиться неплохих результатов при лечении больных с острой спаечной кишечной непроходимостью.
Хирургический доступ.
В большинстве случаев при острой спаечной кишечной непроходимости операцию выполняют через широкий разрез передней брюшной стенки. По строгим показаниям при отсутствии множественных спаечных сращений операция может быть произведена лапароскопическим способом.
Перед операцией, если такая возможность имеется, следует провести ультразвуковое исследование для определения мест фиксации кишечных петель к передней брюшной стенке спайками. Лапароскопический вариант операции без предварительного ультразвукового исследования недопустим.
Оптимальным хирургическим доступом является средне-срединная лапаротомия. При необходимости доступ расширяют вверх или вниз. Если по средней линии имеется рубец от предшествующей операции, производят иссечение кожного рубца окаймляющими разрезами. В рубцовых тканях белой линии живота часто обнаруживают инкапсулированные лигатуры из нерассасывающего шовного материала, которые удаляют. Иногда в области лигатур бывают гранулемы, которые следует иссекать вместе с окружающей их грануляционной тканью, а ложе обрабатывать раствором антисептика.
Париетальная брюшина в области послеоперационного рубца брюшной стенки всегда имеет грубые сращения с апоневрозом белой линии живота. Более того, как правило, к париетальной брюшине фиксированы спайками большой сальник и петли кишечника. В связи с этим при рассечении единого блока тканей апоневроза белой линии живота и париетальной брюшины можно вскрыть просвет кишки, фиксированной к париетальной брюшине. Если перед операцией не удалось произвести ультразвуковое исследование и получить информацию о локализации висцеропариетальных сращений, для уменьшения опасности вскрытия просвета кишки используют следующий прием.
Лапаротомный разрез продлевают на 3—5 см выше или ниже старого операционного рубца. Брюшную полость вскрывают в самой верхней или нижней части разреза, вне зоны прежнего доступа, где вероятность плотной фиксации большого сальника и кишечника меньше.
После того, как удалось вскрыть брюшную полость, пусть даже на небольшом протяжении в углу раны, дальнейшее рассечение единого листка апоневроза и париетальной брюшины существенно облегчается. Приподнимая брюшную стенку крючком или наложенными на край апоневроза зажимами Микулича, фиксированные спайками органы отделяют от париетальной брюшины острым путем, освобождая место для последующего рассечения апоневроза с брюшиной. Таким образом поэтапно рассекают апоневроз и париетальную брюшину на всем протяжении лапаротомной раны. При наличии в брюшной полости выпота его обязательно забирают для микробиологического исследования.
Основным ориентиром места непроходимости является граница между перерастянутой содержимым приводящей частью кишечника и спавшимися кишечными петлями отводящей части. Если расширенные приводящие петли плавно переходят в нерасширенную часть, это свидетельствует об отсутствии механической кишечной непроходимости, т. е. хирург имеет дело с паралитическим илеусом.
Техника разделения спаечных сращений.
Разделение «рыхлых» спаек, с которыми чаще сталкиваются при ранней спаечной кишечной непроходимости, не представляет технических сложностей. Эти спайки можно разрушать пальцем, не прилагая при этом излишних усилий, приводящих к повреждению серозного покрова кишечника, или рассекать ножницами. При рассечении спаек ножницами используют прием «обратной работы» режущих частей инструмента. Для этого кончики сомкнутых браншей вводят между спаянными органами, после чего бранши разводят в стороны, что позволяет обозначить «слой» между фиксированными петлями кишки. За счет отсутствия васкуляризации сращений кровотечения при этом не бывает. Шнуровидные спайки, как правило, имеющие достаточную протяженность, рассекают ножницами или электроножом. Используя для разделения спаек электрокоагуляцию, следует строго следить за тем, чтобы не произошло ожога стенки кишки. Для этого зона термического воздействия должна отстоять не менее чем на 3—5 мм от кишечной стенки.
Наибольшие технические сложности возникают в случаях, когда кишечные петли плотно фиксированы друг к другу или к париетальной брюшине на значительной площади, образуя единый конгломерат. Бывают ситуации, в которых фиксация кишечных петель между собой столь плотная, что идентифицировать границу между ними или париетальной брюшиной невозможно. При плотном сращении стенки кишки с париетальной брюшиной самым безопасным способом является отделение кишки за счет иссечения прилежащей к ней брюшины.
Для разделения плотных плоскостных межкишечных сращений нужно прибегать к следующему приему. В месте наименее выраженных спаечных сращений создают канал в сторону задней брюшной стенки. В образовавшееся пространство вводят указательный палец правой руки и маятникообразными движениями без приложения излишних усилий разделяют спаечные сращения по задней поверхности кишечного конгломерата. Как правило, спаечные сращения и их плотность в этой области не столь выражены, за счет чего появляется возможность частично разделить кишечные петли по задней поверхности конгломерата. После достижения кишечными петлями некоторой мобильности их ротируют кпереди и в таком положении завершают разделение спаек. Если разделить кишечный конгломерат не представляется возможным, а уровень непроходимости приходится на эту часть кишечника, то возможно два варианта действий. При отсутствии признаков нарушения жизнеспособности деформированной части кишечника накладывают обходной межкишечный анастомоз. При нарушении кровообращения выполняют резекцию кишечного конгломерата.
При разделении спаечных сращений может произойти поверхностное повреждение кишечной стенки. Чаще повреждаются перерастянутые приводящие петли. В случаях, когда повреждение затрагивает не только серозный, но и мышечный слой (при этом через дефект стенки пролабирует неповрежденная слизистая оболочка кишки), необходимо наложить серозно-мышечные швы рассасывающимся шовным материалом на атравматической игле 4/0 или 5/0.Поверхностные щелевидные повреждения серозного покрова ушивать не следует, так как после опорожнения перерастянутой кишки края этих дефектов сопоставляются самостоятельно.
При вскрытии просвета кишки дефект стенки тотчас зажимают марлевым тампоном, чтобы прекратить выделение кишечного содержимого. Строгое соблюдение асептики является необходимой мерой, поскольку микрофлора, заселяющая просвет приводящей петли, всегда высоковирулентна и при контаминации брюшной полости имеется реальная угроза возникновения инфекционных послеоперационных осложнений.
Перед ушиванием дефекта стенки кишки поврежденная петля должна быть полностью выделена из спаечных сращений. Ушивание не мобилизованной из спаек кишки никогда не бывает успешным.
Мобилизованную поврежденную кишку изолируют от брюшной полости марлевыми тампонами. Выше и ниже повреждения на кишку накладывают мягкие кишечные жомы. Отнимают руку с тампоном, закрывавшим перфорационное отверстие. Отсосом аспирируют кишечное содержимое, оставшееся в просвете изолированной кишечными жомами петли кишки, обрабатывают зону перфорации и прилежащие ткани раствором антисептика. После этого ушивают отверстие в поперечном направлении в 2 ряда швов рассасывающимся шовным материалом на атравматической игле 4/0—5/0.
Выявив место непроходимости, пересекают спайку, сдавливающую просвет кишки и ее брыжейку при странгуляционной непроходимости, разделяют плоскостные сращения, деформирующие кишечные петли при обтурационной непроходимости.
После устранения кишечной непроходимости необходимо оценить жизнеспособность кишки. При странгуляционной непроходимости наибольшие нарушения кровообращения всегда бывают в области странгуляционной борозды. Абсолютным признаком некроза кишечной стенки является ее грязно-серый или черно-зеленый цвет в сочетании со значительным понижением тургора тканей (дряблость кишечной стенки с участками ее западения при спавшейся кишке или пролабирование отдельных участков при повышенном внутрикишечном давлении) и неприятным специфическим запахом. Сомнения в жизнеспособности кишки должны возникать, если пораженный участок не перистальтирует, имеет багрово-черный цвет, не определяется пульсация брыжеечных и прямых артерий кишечной стенки. В такой ситуации после рассечения спаек петлю кишки погружают в брюшную полость и оставляют на 15—20 мин. За это время осуществляют гемостаз, производят назоинтестинальную интубацию и аспирируют кишечное содержимое. Затем вновь осматривают компрометированную часть кишки.
Более агрессивным способом проверки жизнеспособности кишки является ее согревание марлевыми тампонами, смоченными горячим физиологическим раствором. Если указанные мероприятия не привели к изменению состояния кишечной стенки, кишку признают нежизнеспособной, что служит показанием к ее резекции. В свою очередь резекция кишки требует предварительного выполнения назоинтестинальной интубации.
Назоинтестинальная интубация
, обеспечивая декомпрессию тонкой кишки, способствует нормализации кровообращения кишечной стенки и быстрому восстановлению моторной активности. Соответственно показаниями к ней являются расширение просвета кишки до 5 см и более, утрата моторной активности (паралитическая кишечная непроходимость), а также необходимость выполнения резекции тонкой кишки.
Назоинтестинальную интубацию выполняют совместно с анестезиологом, который вводит через нос в желудок специальный многоперфорированный зонд длиной около 1,5 м. При проведении зонда через пищевод он может сворачиваться в последнем, не достигая желудка. В таком случае под контролем ларингоскопа в пищевод вводят интубационную трубку № 8 и через ее просвет проводят назоинтестинальный зонд, который после окончания интубациии изо рта переводят в носовой ход, как при задней тампонаде носа.
После того, как головка зонда оказывается в желудке, необходимо провести ее в двенадцатиперстную кишку. Для этого левой рукой хирург фиксирует привратник, правой рукой через его просвет проводит головку зонда в луковицу двенадцатиперстной кишки. Далее зонд продвигают через двенадцатиперстную кишку за счет смещения его через стенку желудка. При типичном расположении всех отделов двенадцатиперстной кишки это удается довольно просто и быстро. При наличии резких изгибов кишки для проведения зонда используют следующие приемы. Головку зонда левой рукой удерживают в луковице двенадцатиперстной кишки и смещают в вертикальную часть кишки, в то время как правой рукой под брыжейкой поперечной ободочной кишки направляют головку в нижнегоризонтальную часть двенадцатиперстной кишки. Проведенный в этот участок зонд, как правило, легко выходит за связку Трейтца в тощую кишку. При ощущении препятствия в области дуоденоеюнального перехода, что обусловлено наличием спаечной деформации в виде двустволки, правой рукой перемещают оливу зонда в нужном направлении или рассекают спайки, деформирующие кишку. Форсированное продвижение зонда при ощущаемом препятствии в области дуоденоеюнального перехода недопустимо ввиду опасности перфорации стенки кишки.
По прохождении головки зонда за связку Трейтца начинается наиболее легкий этап — проведение зонда по тонкой кишке. Интубация тонкой кишки ускоряется, если оперирующий хирург двумя руками продвигает зонд в ее начальном отделе, а ассистент направляет головку зонда и помогает его продвижению, расправляя кишечные петли. Процедура проведения зонда может затрудняться из-за образования избыточных петель зонда в желудке, что возникает, если поступление зонда в желудок опережает его продвижение по тонкой кишке, поэтому действия хирурга и анестезиолога, продвигающего зонд в желудок, должны быть синхронными. Интубацию завершают при достижении илеоцекального отдела кишечника. После этого производят аспирацию кишечного содержимого.
Заводить зонд в слепую кишку не следует во избежание заброса толстокишечного содержимого в тонкую кишку, что неизбежно приводит к дополнительной колонизации тонкой кишки фекальной микрофлорой. Аспирацию кишечного содержимого осуществляют только после завершения интубации, так как проведение зонда через раздутые петли менее травматично и занимает меньше времени.
Завершив интубацию тонкой кишки, контролируют расположение зонда. Он не должен иметь петель и деформаций. «Заламывание» зонда на каком-либо боковом отверстии сводит на нет эффективность декомпрессии в послеоперационном периоде.
Важной деталью правильного положения зонда в кишечнике является локализация последнего бокового отверстия, которое должно находиться в средней части желудка. Недопустимо смещение последнего отверстия в пищевод, так как это может привести в послеоперационном периоде к аспирации желудочного содержимого в дыхательные пути. Менее опасная ошибка — заведение последнего бокового отверстия в двенадцатиперстную кишку. В этом случае у больных может возникать рвота, поскольку полость желудка оказывается недренированной. Для облегчения определения расположения последнего отверстия в зонде на этом уровне создают колечко из узкой полоски пластыря. Пальпируя через стенку утолщение на зонде, точно ориентируются в правильности его расположения.
При необходимости выполнения резекции кишки назоинтестинальный зонд проводят дистальнее резецируемого участка, аспирируют кишечное содержимое. Затем зонд перемещают проксимальнее резецируемой части и лишь после этого приступают к резекции кишки, а выполнив последнюю, зонд вновь продвигают дистальнее межкишечного анастомоза.
Резекция некротизированной тонкой кишки должна быть выполнена в пределах жизнеспособных тканей так, чтобы нарушения кровообращения в области пересечения кишок были минимальны. Для достижения этого отступают от видимой зоны некроза на 20—30 см. Поскольку микроциркуляторные изменения в приводящей петле кишки всегда выражены больше, чем в отводящей, в оральном направлении приходится отступать на большее расстояние.
После резекции кишки анастомозирование культей может быть осуществлено как конец в конец, так и бок в бок. Последний вариант наложения анастомоза используют при выраженном несоответствии диаметров приводящей и отводящей культей кишки.
При анастомозировании конец в конец культи тонкой кишки, предварительно прошитые сшивающими аппаратами или перевязанные лигатурами, освобождают от жировой клетчатки в области брыжейки на протяжении не более 8—10 мм. На противоположные стороны культей кишок на уровне границы мобилизованной брыжейки накладывают серозно-мышечные швы-держалки. Натяжением в противоположные стороны за эти швы кишку растягивают до диаметра эктазированной культи приводящей петли. Рассасывающимся шовным материалом на атравматических иглах накладывают первый ряд узловых серозно-мышечных швов, которыми формируют заднюю губу анастомоза. При этом должен остаться свободный край стенки длиной 6—8 мм для наложения внутреннего ряда швов монофиламентной рассасывающейся нитью 3/0 или 4/0. Последними прошивают стенку кишки без захвата слизистой оболочки — выкол иглы делают через подслизистый слой. Передний ряд швов накладывают с соблюдением тех же технических правил. Узловыми швами ушивают дефект брыжейки под анастомозом. При этом швы накладывают поверхностно, чтобы в них не попали сосуды брыжейки.
При выраженном несоответствии диаметров приводящей и отводящей петель кишки анастомоз приходится накладывать бок в бок. Культи кишок, прошитые сшивающими аппаратами, перитонизируют за счет наложения кисетных или узловых швов. Узловые швы используют при резкой инфильтрации стенки кишки или ее большом диаметре. Первый ряд узловых атравматических серозно-мышечных швов накладывают вдоль брыжеечного края кишок на протяжении 3—4 см. При этом длина «слепых» карманов в области культей не должна превышать 1—2 см. Электрокоагулятором рассекают стенку кишок, отступая 6—8 мм от первого ряда швов. Длина разреза должна быть не более 2—2,5 см. Просвет кишок обрабатывают антисептическим раствором. Накладывают внутренний ряд монофиламентных рассасывающихся швов без захвата слизистой оболочки на заднюю губу анастомоза. Затем аналогичным способом формируют переднюю губу анастомоза.
Независимо от способа анастомозирования назоинтестинальный зонд проводят за анастомоз на 30—50 см.
Завершая операцию, аспирируют транссудат, образовавшийся в брюшной полости за время операции, кровь, выделившуюся из рассеченных спаек. При необходимости производят дополнительный гемостаз. Брюшную полость дренируют через контрапертуру трубкой, которую устанавливают в полость малого таза.
Лапаротомную рану ушивают послойно наглухо с использованием рассасывающегося шовного материала.
Лапароскопические операции при острой спаечной кишечной непроходимости
Лапароскопический вариант операции правомочен только в том случае, если хирург в совершенстве владеет необходимыми техническими навыками лапароскопической хирургии (опыт самостоятельных операций — холецистэктомия, аппендэктомия, фундопликация — должен превышать более 100 вмешательств). Разрешающая способность лапароскопической техники оперирования ограничена степенью выраженности спаечных сращений. Лапароскопический адгезиолизис возможен лишь в случае, если у больного ранее не было многократных операций и по результатам ультразвукового исследования отсутствуют множественные спайки. Завышение показаний к лапароскопическому выполнению операции таит в себе опасность тяжелых осложнений.
Иглу Veress для наложения пневмоперитонеума и первый троакар вводят в брюшную полость в проекции «акустического окна» (участка передней брюшной стенки, свободного от фиксированных спайками петель кишечника), установленного при ультразвуковом исследовании. Стилет троакара меняют на лапароскоп. Осуществляют диагностическую лапароскопию, при которой оценивают распространенность спаек, состояние кишечника. Уже на этом этапе часто удается выявить кишку, сдавленную спайкой. Если пораженный участок кишки недоступен прямому осмотру, поиск следует осуществлять за счет перемещения спавшихся петель кишок зажимом Бебкокка. Нарушение этого правила — смещение инструментами перерастянутых петель, расположенных выше места непроходимости, — более травматично и может привести к вскрытию просвета кишки. Детали техники адгезиолизиса идентичны таковым при традиционном варианте операции. Если произошло вскрытие просвета кишки (а оно бывает практически всегда выше уровня препятствия), в брюшную полость поступает значительное количество кишечного содержимого с высоковирулентной микрофлорой. Лапароскопическая санация брюшной полости в такой ситуации не может быть адекватной, поэтому следует тотчас выполнять лапаротомию.
Изложенное эссе основано на личном опыте 40-летней хирургической практики и не претендует на истину в последней инстанции. Однако, наблюдая за хирургами, придерживающимися изложенных рекомендаций, мы имели возможность убедиться в их правомочности. Предлагаемые «мелкие» детали техники часто позволяют избежать больших проблем.
Всегда ли необходимо выведение стомы во время операции по поводу кишечной непроходимости?
Помимо наложения стомы, альтернативным способом восстановления прохождения пищи по кишечнику является создание обходного межкишечного анастомоза. Операции называются по названию соединяемых отделов кишечника, например:
- Операция на правых отделах толстого кишечника называется наложением обходного илеотрансверзоанастомоза.
- Наложение анастомоза между начальным отделом тонкой и конечным отделом тощей кишок называется наложением обходного илеоеюноанастоза.
Каждое из этих вмешательств может быть временным, производимым для подготовки больного к последующим этапам или окончательным при невозможности проведения радикальной операции.
Основной задачей, решаемой во время хирургического лечения острой кишечной непроходимости, является спасение жизни пациента от угрозы прорыва кишечного содержимого в брюшинную полость с развитием острого перитонита и смертью пациента.[3,6]
Что происходит с выведенной стомой?
В течение 2-3-х недель после выполненной операции по поводу острой кишечной непроходимости при условии улучшении общего состояния, ликвидации последствий интоксикации организма может быть выполнена повторная операция по восстановлению естественного пассажа пищи. В таких случаях выполняется наложение кишечного анастомоза, который погружается внутрь брюшной полости.
В остальных случаях к колостоме присоединяется калоприемник для сбора кишечного содержимого. Современные разновидности калоприемников позволяют поддерживать приемлемое качество жизни даже при их использовании в течение нескольких месяцев. [2,6]
Послеоперационный период и возможные осложнения
Обычно больные, которые перенесли операцию по поводу кишечной непроходимости, могут вернуться к нормальному приему пищи через несколько дней. В первые дни питание осуществляется внутривенно, разрешено лишь смачивать губы влажным кусочком ткани. Многих беспокоят сильные послеоперационные боли, поэтому важно назначить адекватное обезболивание.
Риск осложнений зависит от объема операции, общего состояния здоровья пациента и других факторов:
- Несостоятельность кишечных швов — опасное для жизни осложнение, оно требует немедленной повторной операции. Если швы плохо справляются со своей функцией, кишечное содержимое попадает в брюшную полость, развивается перитонит.
- Сильные кровотечения также опасны и требуют хирургического вмешательства.
- Распространенное осложнение — образование тромбов в сосудах ног. Чтобы его предотвратить, назначают препараты, которые уменьшают свертываемость крови, на ноги накладывают эластичные бинты, больного стараются как можно быстрее вернуть к активным движениям.
- Для профилактики инфекции назначают антибиотики внутривенно, через дренажные трубки, которые оставляют в брюшной полости после операции.
- Если во время операции врач сделал большой разрез, швы могут плохо заживать, расходиться. Риск этого осложнения выше у пожилых, ослабленных, страдающих сопутствующими заболеваниями пациентов.
- Любая операция — травма для организма. После нее в животе могут сформироваться спайки, и они способны вновь привести к кишечной непроходимости.
Возможно ли помочь больному без операции?
Часто в тяжелых случаях и при неоперабельных опухолях у больных в тяжелом состоянии с частичной кишечной непроходимостью декомпрессия желудочно-кишечного тракта достигается путем эндоскопической установкой стента в толстую кишку. В этом случае хирургическая операция выполняется через естественный просвет кишечника – под контролем колоноскопа в просвет толстой кишки per rectum вводится первоначально баллон, расширяющий суженный (стенозированный) участок, а затем устанавливается стент.
Своевременная профилактическая установка стента в просвет кишечника позволяет продлить жизнь и существенно повысить ее качество за счет уменьшения интоксикации, а также избежать вероятного оперативного вмешательства у больных при 4 стадии ракового процесса. Аналогичным образом может выполняться стентирование участков двенадцатиперстной кишки. [9,11]
Мы устанавливаем стенты в толстый кишечник у больных раковым поражением кишечника и с высоким классом анестезиологического риска из-за наличия сопутствующих заболеваний, в том числе ишемической болезни сердца, сахарного диабета и ряда других. Это позволит длительно поддерживать проходимость кишечника и избежать оперативного вмешательства.
Запись на консультацию круглосуточно
+7+7+78
Список литературы:
- Клинические рекомендации: Острая кишечная непроходимость опухолевой этиологии. — Москва, 2014.
- Клинические рекомендации: Острая кишечная непроходимость опухолевой этиологии у взрослых. — Министерство здравоохранения РФ. — 2022.
- Кишечная непроходимость : учебно-методическое пособие / П. С. Неверов К46 [и др.]. – Минск : БГМУ, 2022. – 42 с.
- Хирургические болезни. Учебно — методическое пособие/ Под редакцией Чернядьев С.А. – Екатеринбург,2019. –29с.
- Б. О. Кабешев, С. Л. Зыблев. Острая кишечная непроходимость. — Практическое пособие для врачей. — Гомель, 2022.
- М.Ю. Кабанов, И.А. Соловьёв, О.В. Балюра. — Результаты комплексного лечения больных с острой кишечной непроходимостью карциноматозного генеза. — Вестник Российской военно-медицинской академии, 1(37)-2012.
- Международная классификация болезней 10-го пересмотра (МКБ-10) https://mkb-10.com/.
- Barnett A, Cedar A, Siddiqui F, et al. Colorectal cancer emergencies. J Gastrointest Cancer 2013;44(2):132–42.
- Национальные клинические рекомендации «острая неопухолевая кишечная непроходимость». — Российское общество хирургов. — 2015.
- Karakaş DÖ, Yeşiltaş M, Gökçek M, Eğin S, Hot S. Etiology, management, and survival of acute mechanical bowel obstruction: Five-year results of a training and research hospital in Turkey. Ulus Travma Acil Cerrahi Derg 2019;25:268-280.
- Colorectal cancer (update): evidence review for effectiveness of stenting compared with emergency surgery for acute large bowel obstruction. Developed by the National Guideline Alliance part of the Royal College of Obstetricians and Gynaecologists. FINAL (January 2020).
- Subramaniyan Ramanathan, Vijayanadh Ojili, Ravi Vassa, and Arpit Nagar. Large Bowel Obstruction in the Emergency Department: Imaging Spectrum of Common and Uncommon Causes. J Clin Imaging Sci. 2017; 7: 15. doi: 10.4103/jcis.JCIS_6_17