Введение
Нормальная микрофлора (микробиота) желудочно-кишечного тракта (ЖКТ) представляет собой сложную экосистему, включающую более 500 видов микроорганизмов [1]. Суммарный вес микробиоты составляет около 3 кг. Микробиота ЖКТ поддерживает значительное количество биохимических процессов и по значимости сравнивается с печенью. Некоторые исследователи даже называют микробиоту специальным “микробным органом”, т. к. микробиота участвует в иммуностимуляции, синтезе витаминов группы В и витамина К, регулировании моторики и других функций ЖКТ, синтезе короткоцепочечных жирных кислот (КЦЖК) и множестве других процессов [2].
Характерные изменения профиля микрофлоры играют существенную роль не только в патогенезе заболеваний ЖКТ, но и заболеваний других органов и систем [3]. Количественный и качественный состав микрофлоры толстой кишки служит чувствительным индикатором здоровья человека и является “доклиническим” маркером нарушений гомеостаза [4].
В отраслевом стандарте “Протокол ведения больных. Дисбактериоз кишечника” (ОСТ 91500.11.0004 от 09.06.2003) нормофлора определена как качественное и количественное соотношение в отдельных органах и системах разнообразных популяций микробов, поддерживающих биохимическое, метаболическое и иммунное равновесие макроорганизма, необходимое для сохранения здоровья. Дисбактериоз кишечника в свою очередь определен как клинико-лабораторный синдром, характеризущийся изменением качественного и/или количественного состава нормофлоры кишечника, транслокацией ее представителей в несвойственные биотопы, метаболическими и иммунными нарушениями, сопровождающимися клиническими симптомами у части пациентов [5].
Микрофлора ЖКТ весьма чувствительна к воздействию таких внешних факторов, как прием антибиотиков, алкоголя, психологические и физические нагрузки, радиация, макро- и микроэлементный состав пищи [6]. К негативным последствиям воздействия антибиотиков относятся снижение синтеза КЦЖК, снижение печеночного кровотока, уменьшение всасывания кальция и повреждение слизистой оболочки ЖКТ [7].
Диетические факторы, негативно влияющие на микрофлору ЖКТ,включают: • соединения серы (сульфаты, сульфиты и т. д.), которые часто используются в качестве консервантов для сухофруктов, овощей, яблок, упакованных соков, муки, большинства алкогольных продуктов и многих лекарств [8]; • диету с высоким содержанием белка (непереваренный белок является источником таких токсичных метаболитов, как аммиак, амины, фенолы, сульфиды, индолы) [9]; • высокоуглеводную диету с избытком простых сахаров, которая способствует увеличению ферментативной деятельности бактерий и повышению концентрации желчных кислот, что приводит к замедлению времени прохождения через кишечник [10].
Лечение дисбактериоза может проводиться пробиотиками, т. е. непосредственной “подсадкой” пациенту живой, активной флоры. Молочнокислые бактерии и бифидобактерии являются наиболее распространенными пробиотиками (WHO Expert Consultation, 2001) [11].
Следует отметить, что принимаемые конкретным пациентом штаммы бифидо- и лактофлоры, как правило, не соответствуют уникальному врожденному профилю штаммов этого пациента. Последнее делает необходимым персонализированное назначение конкретных штаммов микрофлоры пациенту, что практически крайне сложно осуществить. В результате отсутствия генетической совместимости между вводимыми штаммами и штаммами организма пациента развиваются побочные эффекты (напри- мер, у детей может возникать сепсис) или же эффективность терапии пробиотиками чрезвычайно снижается и терапия не имеет долговременных эффектов.
Вторым важным направлением терапии дисбактериоза кишечника является учет того, что для питания позитивной и патогенной флоры необходимы различные наборы питательных веществ. Пребиотики – это вещества натурального или синтетического происхождения, селективно стимулирующие рост и/или ферментативную активность одного или нескольких видов нормофлоры. К пребиотикам, как правило, относят пищевые волокна, олигосахариды (инулин), лактулозу. Прием пребиотиков создает питательную среду для роста позитивной флоры [12].
В настоящей работе вкратце представлены результаты метаболомного моделирования одного из таких препаратов (Хилак форте, Teva Pharmaceutical Industries Ltd., Израиль), для которого имеется значительный опыт эффективного клинического применения.
В представленном систематическом анализе последовательно рассмотрены следующие вопросы: • особенности симбиотической и патогенной микрофлоры; • изменения профиля микрофлоры, связанные с дисбактериозом; • молекулярные факторы, влияющие на выживание микрофлоры; • связь между гормонами стресса и образованием биопленок; • сравнительный метаболомный анализ позитивной и негативной флоры ЖКТ, указывающий на основы молекулярного действия препарата Хилак форте; • опыт клинического применения препарата Хилак форте.
Симбиотическая и патогенная микрофлора
В кишечнике человека содержится по меньшей мере 500 видов микроорганизмов. Принято различать постоянную (облигатную) микрофлору, преобладающую по численности колонийобразующих единиц (КОЕ) и ограниченную по видовому составу, и транзиторную (условно-патогенную) микрофлору, отличающуюся разнообразием, но уступающую облигатной флоре по количественному составу.
В облигатной микрофлоре двенадцатиперстной и тощей кишки доминируют стрептококки, лактобациллы и вейлонеллы; в микрофлоре повздошной кишки – кишечная палочка и анаэробные бактерии. Толстая кишка отличается высокой степенью обсемененности, которая определяется ассоциациями анаэробных и факультативно анаэробных микроорганизмов: бифидобактерий (108–109 КОЕ/г содержимого толстой кишки), лактобацилл (106 – 108 КОЕ/г), эшерихий (106–108 КОЕ/г) и энтерококков (105–106 КОЕ/г) [14].
Нормомикрофлора участвует в формировании колонизационной резистентности, т. е. обеспечивает предотвращение заселения ЖКТ агрессивными условно-патогенными микроорганизмами (например, Clostridium difficile и Candida albicans, гемолизирующей кишечной палочкой, лактозонегативными энтеробактериями и т. д.). Здоровая микрофлора участвует в процессах детоксикации ксенобиотиков, в т. ч. синтетических фармацевтических препаратов. Принципиальным отличием метаболизма, протекающего в кишечнике, является то, что в нем доминируют процессы гидролиза и восстановления, тогда как в печени –процессы окисления.
Изменения профиля микробиоты, связанные с дисбактериозом
Для выбора оптимального курса терапии дисбактериоза необходима диагностика стадии этого заболевания.
Согласно бактериологической классификации И.Б. Куваевой и К.С. Ладодо (1991), выделяют четыре фазы дисбактериоза:
I – латентную фазу дисбактериоза [4]. Клинических проявлений дисбактериоза не отмечается. Наблюдается снижение количества позитивной микрофлоры (бифидобактерий, лактобацилл, симбиотических кишечных палочек) в несколько раз по сравнению с нормой.
II – пусковую фазу дисбактериоза. Функциональные расстройства пищеварения включают запор или, наоборот, спорадический жидкий стул зеленоватого цвета с неприятным запахом и со сдвигом рН в щелочную сторону. Происходит размножение плазмокоагулирующих стафилококков, протеев, грибов рода Candida.
III – фазу агрессии аэробной флоры. Дисфункции кишечника с расстройствами моторики, секреции ферментов и всасывания, отмечается учащенный разжиженный стул (часто зеленого цвета), снижение аппетита, ухудшение самочувствия. Происходит характерное увеличение содержания агрессивных микроорганизмов (золотистые стафилококки и протеи – до 108, гемолитические знтерококки, наблюдается замещение полноценных Escherichia coli бактериями родов Klebsiella, Enterobacter, Citrobacter и др.).
IV – фазу ассоциативного дисбактериоза. Расстройства пищеварительной системы, дефицит массы тела, бледность кожных покровов, снижение аппетита, частый зеленоватый стул с резким запахом и примесью слизи (иногда крови). Характерно вегетирование энтеропатогенных серотипов кишечной палочки, сальмонелл, шигелл и других возбудителей острых кишечных инфекций, возможно размножение клостридий. Начиная со второй стадии происходит активный рост колоний патогенных микроорганизмов.
Молекулярные факторы, влияющие на выживание микрофлоры
Систематических исследований по различиям в метаболизме позитивной и патогенной микрофлоры ЖКТ не проводилось. В ходе бактериологических исследований были установлены различные молекулярные факторы, которые могут влиять на выживание позитивной флоры. К этим факторам относятся, в частности, содержание в питательной среде бактерий пирофосфата, устойчивость микроорганизмов к желчным кислотам, влияние таких эндогенных регуляторов, как гистамин и катехоламины, и влияние продуктов жизнедеятельности определенного рода бактерий.
Экзогенный пирофосфат (входящий в состав препарата Хилак форте) вызывает увеличение роста E. coli (на 25–35 %) даже при низких уровнях глюкозы в питательной среде in vitro и in vivo. Повышение уровней пирофосфата в питательной среде кишечной палочки приводит к модуляции синтеза более 20 белков бактериальных механизмов реакции на стресс. Эти процессы улучшают способность E. coli к использованию углерод-содержащих питательных веществ и выживаемости в кишечнике [15].
Желчные кислоты в значительной степени регулируют выживание микрофлоры ЖКТ. Например, анализ чувствительности к желчи 195 энтеробактерий в культуре показал, что сопротивляемость бактерий к желчи уменьшается в следующем ряду: Shigella > Salmonella > Klebsiella > Providencia. Уровень чувствительности к желчи определяет способность энтеробактерий колонизировать желчные пути и проксимальные участки пищеварительного тракта [16].
Гистамин, известный нейромедиатор и регулятор воспаления, вносит определенный вклад во взаимодействие “бактерии–хозяин” посредством т. н. двухкомпонентных систем сигнализации, регулирующих метаболизм КЦЖК и хемотаксис бактерий [17]. В эксперименте антагонисты гистамина также способствовали снижению численности колоний E. coli [18]. Данный результат весьма важен с практической точки зрения. Традиционно считается, что часто применяемые антигистаминные препараты не влияют на состояние микрофлоры кишечника. Поэтому при приеме антигистаминных препаратов следует оказывать дополнительную поддержку микробиоты пребиотическими препаратами (инулин, Хилак форте и др.).
. Двухкомпонентные системы бактериальной сигнализации осуществляют воздействие гистамина, глюкозы и других метаболитов на жизнедеятельность кишечной микрофлоры (на примере E. coli) [18].
Помимо гистамина посредством двухкомпонентных систем бактериальной сигнализации на жизнедеятельность бактерий влияют также такие молекулы, как ацетоацетат, полиамины, липиды и глюкоза (рис. 1). Ацетоацетат или спермидин инициирует активацию белка AtoS гистидинкиназы (“первый компонент”), который активирует “второй компонент” AtoC фосфорилированием аминокислотных остатков Asp55 и His73. Гистамин и кальций оказывают регулирующее воздействие на этот процесс, регулируя транспорт питательных веществ через мембрану и тем самым поддерживая выживание позитивных штаммов E. coli [18].
Гормоны стресса – катехоламины и образование биопленок микрофлорой ЖКТ
Важно отметить, что микрофлора ЖКТ реагирует на изменения уровней гормонов стресса – адреналина и норадреналина. Переживание острого стресса у пациентов (F45.0) снижает уровень лактобацилл и бифидобактерий в течение нескольких дней (р < 0,001) [19]. В то же время норадреналин, адреналин и дофамин стимулируют деление типичной кишечной палочки [20].
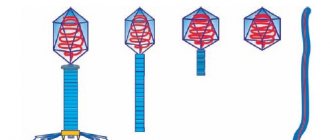
Эффекты воздействия гормонов стресса на кишечную микрофлору связаны с важнейшей особенностью выживания бактерий – образованием т. н. бактериальных пленок (англ. biofilms). Бактериальные пленки – колонии бактерий, выживаемость которых чрезвычайно усилена за счет активной кооперации между отдельными микроорганизмами (т. н. кворумная сигнализация). В биопленке бактерии взаимодействуют друг с другом и с поверхностью эпителия ЖКТ. Эти “слипшиеся” клетки бактерий часто окружают себя т. н. матрицей из внеклеточных полимерных веществ – ДНК, белков, полисахаридов [21].
Бактерии, способные формировать биопленки, имеют рецепторы к специфическим сигнальным молекулам кворумной сигнализации. Особый интерес представляют сигнальные молекулы N-ацилгомосерин лактонов и аутоиндуктор-2, производимые микрофлорой ЖКТ. N-ацилгомосерин лактоны (иногда также называемые аутоиндукторами 1-го типа – АИ-1) отличаются длиной боковой цепи R-группы, содержащей цепи длиной 4–18 атомов углерода. Биологически активными являются N-ацилгомосерин лактоны с длинной R-цепи более 4 атомов углерода, причем более длинная R-цепь соответствует более стабильной сигнальной молекуле и более высокому сродству сигнальной молекулы к соответствующему рецептору [22, 23]. Связывая N-ацилгомосерин лактоны, белок-рецептор SdiA активирует транскрипцию генов, ускоряющих процессы клеточного деления бактерий для формирования биопленки [24].
Известно, что в состав Хилак форте включены продукты жизнедеятельности типичных E. coli, которые имеют механизмы реагирования на N-ацилгомосерин лактоны (включая специальный транспортный белок), в то время как, например, C. difficile, Staphylococcus aureus, C. albicans не имеют таких механизмов. Более того, определенные N-ацилгомосерин лактоны не только способствуют выживанию типичных E. coli, но и тормозят рост патогенной флоры. Например, 3-оксо-12-гомосерин лактон уменьша-ет вирулентность S. aureus посредством снижения секреции экзотоксина и экспрессии вирулентных генов sarA и agr [25]. Определенные гомосерин лактоны также тормозят развитие грибов рода Candida [26].
Аутоиндуктор-2 (АИ-2) – фуранозилборатный эфир, также является одной из основных молекул кворумной сигнализации у различных видов бактерий [27]. В целом молекулярный механизм воздействия АИ-2 можно описать следующим образом. Молекула АИ-2 специфически связывается с транспортным белком типа Lsr и транспортируется внутрь бактериальных клеток, где претерпевает фосфорилирование белком киназы LsrK. Затем фосфо-АИ-2 связывается с рецептором – транскрипционным репрессором LSRR, который отделяется от промотера lsr-оперона (группы генов), что приводит к инициации транскрипции генов lsr. Эти гены включают ген luxS, кодирующий одноименный белок, который в свою очередь играет важную роль в переработке S-аденозил-L-метионина с образованием АИ-2 как побочного продукта [28].
Микроорганизмы флоры кишечника различаются по наличию у них систем кворумной сигнализации, опосредованной сигнальной молекулой АИ-2. Например, основной ген данной сигнальной системы, ген luxS, был найден в геномах позитивной флоры E. coli, Lactobacillus acidophilus, но не найден в геномах Streptococcus faecalis и дрожжеподобных грибов C. albicans. Поэтому АИ-2 будет способствовать выживанию и росту E. coli, L. acidophilus и не окажет воздействия на выживание S. faecalis или C. albicans.
Повышенные уровни катехоламинов воспринимаются как факторы стресса и человеком и его микробиотой. Катехоламины непосредственно стимулируют формирование биопленок. Норадреналин отличается наиболее интенсивным воздействием на микробиоту и приводит к выработке бактерией E. coli молекулы АИ-2 [29]. Другими факторами среды, которые влияют на образование биопленок, являются триптофан в высокой концентрации (высокие уровни триптофана, наоборот, предотвращают формирование биопленок E. coli [30] и определенные, в настоящее время еще не идентифицированные секретируемые бактериями пептиды. Так как обработка среды роста бактерий протеиназой К значительно снижала степень агрегации бактерий в биопленки, это указывает на важную роль белковых компонентов в формировании биопленок микробиоты [31].
Таким образом, анализ геномов исследованных представителей микробиоты ЖКТ показал, что гены, отвечающие за синтез и клеточный ответ микроорганизмов на стимуляторы роста биопленок (АИ 1-го и 2-го типов), присутствуют в таких представителях микробиоты, как E. coli и L. acidophilus. Поэтому можно предположить, что аутоиндукторы, способствующие выживанию бактериальных пленок микробиоты, присутствуют в беззародышевых экстрактах продуктов жизнедеятельности этих микроорганизмов.
Сравнительный метаболомный анализ позитивной и негативной кишечной флоры и основы молекулярного действия препарата Хилак форте
Известно, что экстракты продуктов жизнедеятельности определенного вида бактерий являются стимулятором роста определенных бактерий. При проведении сравнения 9 культур бифидобактерий и 18 условно-патогенных микроорганизмов in vitro, выделенных у пациентов с дисбактериозом кишечника, было показано, что бифидофлора снижала уровни факторов роста, антилизоцимовую активность и формирование биопленок Klebsiella pneumoniae, Staphylococcus aureus, C. albicans [32].
Проведены отдельные исследования молекулярных компонентов, входящих в состав экстрактов продуктов жизнедеятельности ряда бактерий. Жидкостная и гель-хроматография низкомолекулярных экзометаболитов культуральной жидкости E. coli штамма М-17 показала, что стимулирующая активность экстракта отчасти обусловлена глутаминовой и янтарной кислотами [33]. Однако систематического анализа состава такого рода экстрактов жизнедеятельности бактерий не проводилось.
В настоящем разделе представлены результаты анализа, проведенного нами на основе моделей метаболома нескольких типичных представителей микрофлоры ЖКТ. Заметим, что термины “геном”, “протеом”, “метаболом” означают совокупности всех молекул определенного вида, найденных внутри того или иного организма. Геном – это совокупность всех генов организма. Процессы экспрессии генов генома приводят к образованию совокупности всех соответствующих белков (протеом). Ферменты-белки поддерживают определенные химические реакции, в результате протекания которых образуются различные метаболиты, образующие метаболом организма.
Таким образом, метаболомом называется весь массив метаболитов или т. н. малых молекул биологической системы. Очевидно, что если известен геном определенного организма, становится возможным установить его протеом. Далее, установление функций (т. н. аннотация) белков протео- ма позволяет моделировать метаболом организма. Данные такого рода приведены в многочисленных биоинформационных базах данных, среди которых следует особо отметить базы KEGG [34], MetaCyc/BioCyc [35] и Reactome [36].
Данные о метаболомах различных организмов являются чрезвычайно важной информацией для разработки и анализа молекулярных эффектов воздействия лекарственных средств [37]. В настоящем исследовании метод сравнительного метаболомного анализа [37] был применен к различным представителям кишечной микробиоты с целью установления спектра возможных механизмов молекулярного воздействия препарата Хилак форте. Очевидно, что эффективный и безопасный пребиотический препарат должен поддерживать выживание позитивной кишечной флоры и тормозить (или по крайней мере не поддерживать) рост негативной флоры. Так как Хилак форте содержит часть метаболома бактерий, соответствующих позитивной микрофлоре, сравнение метаболомов этих микроорганизмов с метаболомами бактерий негативной флоры указывает на наиболее вероятные молекулярные пути, посредством которых осуществляется терапевтическое воздействие препарата. Суммарная информация по исследованным метаболомам представлена в табл. 1.
Как видно из данных, представленных в табл. 1, метаболомы различных видов бактерий имеют значительное число общих метаболитов. Например, из 1230 метаболитов, найденный в 4 моделях метаболомов позитивной флоры, 396 молекул входили в каждый из 4 метаболомов. В случае патогенной флоры из 970 молекул 3 метаболомов 350 входили в каждый из исследованных метаболомов.
Кишечная палочка (E. coli) – грамотрицательная палочковидная бактерия, компонент нормальной флоры кишечника. E. coli синтезирует витамин К [38] и предотвращает рост патогенных микроорганизмов в кишечнике [39]. Болезнетворные штаммы E. coli (например, серотип O157:H7 и др.) не типичны для микробиоты. Энтерококк фекальный (Enterococcus faecalis, S. faecalis) входит в состав микробиоты, играя важную роль в обеспечении колонизационной резистентности слизистой оболочки ЖКТ. Не типичные для микробиоты болезнетворные штаммы E. faecalis являются возбудителем различных инфекций, в т. ч. внутрибольничных инфекций. L. acidophilus и L. helveticus — разновидности бактерий рода Lactobacillus, ферментирующих лактозу до молочной кислоты и выживающих в пищеварительном тракте при более низком значении рН (pH = 4,5 и менее), т. е. в более кислых средах. Ацидофильные лактобактерии применяются в качестве пробиотиков, действие которых во многом обусловлено продуцируемой ими молочной кислотой. Молочная кислота обеспечивает высокую кислотность среды и создает неблагоприятные условия для жизнедеятельности многих патогенных и условно-патогенных бактерий (стафилококков, протеев, энтеропатогенных кишечных палочек), оптимум роста которых находится в более щелочной области значений рН (рН = 6,7 и более). Интересно отметить, что роль метаболома бактерий Lactobacillus выходит за пределы ЖКТ. В частности, L. helveticus секретирует трипептиды, которые снижают повышенное давление через ингибирование ангиотензинпревращающего фермента [40].
В результате сравнительного метаболомного анализа описанных выше бактерий с метаболомами C. difficile, S. aureus и C. albicans было установлено более 90 метаболитов, найденных в представителях исследованной позитивной флоры (т. е. E. coli, S. faecalis, L. acidophilus, L. helveticus) и в то же время отсутствующих у исследованных представителей C. difficile, S. aureus, C. albicans. Основные группы этих метаболитов приведены в табл. 2.
Таким образом, сравнительный метаболомный анализ показал, что позитивная микрофлора содержит метаболиты, необходимые для синтеза и переработки витаминов (витаминов В6, В2, K), поддерживает реакции переработки желчных кислот, обезвреживания определенных метаболитов (переработка оксалатов, преобразование аминов в мочевину, синтез глутатиона), синтез янтарной кислоты и биосинтез КЦЖК. Метаболомы этих представителей микробиоты содержат ряд специфических сахаров (например, пребиотик мелибиозу, т. е. дисахарид галактозы и глюкозы). Наличие этих молекул в экстрактах продуктов жизнедеятельности будет ускорять рост позитивной флоры, не стимулируя при этом рост патогенной флоры.
Например, связанные с биосинтезом витамина В6 метаболиты (производные пиридоксаля и др.) производят витамин В6 не столько для нужд организма хозяина, сколько для поддержания метаболической активности самой микробиоты. По данным настоящего анализа, такие производные витамина В6, как пиридоксаль фосфат, входят в состав более 70 таких важных для E. coli ферментов, как глутамат декарбоксилаза, триптофаназа, серин гидроксиметилсинтетаза, цистеин десульфураза, аланин рацемаза (метаболизм аминокислот), порфиринобилиноген деаминаза (метаболизм желчных кислот), аденилосукцинат синтаза, 4-аминобутират синтаза (метаболизм КЦЖК), и разбираемого ниже фермента гомеостаза селена – Se-цистеин синтетазы. Являясь кофактором белка, вовлеченного в транспорт и переработку мальтозы, пиридоксаль фосфат напрямую определяет способность E. coli перерабатывать мальтозу и, следовательно, необходим для выживания этой и других бактерий микробиоты [41].
. Результаты сравнительного метаболомного анализа исследованных микроорганизмов микрофлоры кишечника (Подчеркнем, что данные метаболиты входят в состав метаболомов позитивной флоры и отсутствуют в метаболомах C. difficile, S. aureus, C. albicans).
Важно отметить, что полученные нами данные (табл. 2) наглядно иллюстрируют правильность рассмотрения микробиоты как специфического “микробного органа”, участвующего в регуляции обмена витаминов В6, В2, К организма хозяина. Более того, встречаемые иногда в литературе сравнения этого “микробного органа” с печенью также весьма оправданны: к примеру, позитивная флора в значительной степени способствует переработке желчных кислот, тем самым дополняя одну из важнейших функций печени.
Крайне интересным результатом настоящего исследования является установление взаимосвязи метаболома важнейших представителей микробиоты и метаболизма оксалатов. Известно, что избыток оксалатов в организме приводит к таким заболеваниям, как мочекаменная болезнь, артриты, и потенцирует развитие атеросклероза вследствие поддержания хронического воспаления эндотелия кровеносных сосудов. В то же время оксалат анион является весьма приемлемым источником пищевого углерода для бактерий микробиоты [42], которые трансформируют токсичный для организма хозяина избыток оксалата в углекислый газ.
В бактериях позитивной флоры данный процесс осуществляется ферментом формил-коэнзим А трансферазой и Mg2+-зависимым ферментом оксалилкоэнзим А декарбоксилазой. Данный процесс зависит по меньшей мере от трех микронутриентов: пантотеновой кислоты (витамина В5, необходимого для синтеза коэнзима А), тиамин-дифосфата (витамина В1) и магния. Поскольку трансформации оксалата являются одним из важных источников углерода для бактерий позитивной флоры, выживание микробиоты в значительной степени зависит от нутрициальной обеспеченности организма витаминами В1, В5 и магнием.
По данным настоящего анализа (табл. 2), важным отличием метаболомов микробиоты от метаболомов патогенной микрофлоры является наличие метаболитов, связанных с биотрансформациями неорганического селена. Любой микроорганизм нуждается в аминокислоте селеноцистеине, необходимой для синтеза более 10 селенобелков. Однако из рассмотренных в настоящем исследовании микроорганизмов только представители позитивной микрофлоры способны синтезировать селеноцистеин из неорганического селена.
Биосинтез селеноцистеина поддерживается двумя ферментами – селенид-водной дикиназой и селеноцистеин синтетазой. Селенид-водная дикиназа – магний-зависимый фермент, который синтезирует из неорганического селенида (Se-2), АТФ и воды важный промежуточный продукт – молекулу селенофосфата (HO3PSe). Витамин-В6-зависимый фермент селеноцистеин синтетаза трансформирует селенофосфат и серин в селеноцистеин. Полученный в результате реакции селеноцистеин встраивается в такие селенобелки бактерий, как ydfZ, selA, selB и др. Благодаря этим ферментам E. coli и другие представители микробиоты могут использовать неорганический селенид непосредственно из окружающей среды.
Проведенный сравнительный анализ метаболомов также позволяет формулировать перспективные направления исследований состава препарата Хилак форте. Например, присутствие в метаболомах E. coli, S. faecalis, L. acidophilus, L. helveticus иона селенида и других производных селена позволяет предполагать достаточно высокое содержание селена в препарате Хилак форте. Поэтому весьма перспективно исследовать содержание селена и других микроэлементов в данном препарате посредством адсорбционной масс-спектрометрии. Наличие в метаболомах этих микроорганизмов продуктов биотрансформаций различных витаминов (В1, В2, В6, К, каротиноидов) позволяет предположить важность исследования витаминного профиля препарата.
Клинический опыт применения препарата Хилак форте как подтверждение результатов метаболомного анализа
Данный препарат для терапии дисбактериоза основан на экстракте продуктов метаболизма таких представителей микробиоты, как E. coli DSM, S. faecalis DSM, L. acidophilus DSM, L. helveticus DSM. Препарат содержит КЦЖК, обеспечивающие восстановление пораженной микрофлоры кишечника [43]. Кроме того, препарат содержит значительные количества фосфорной, лимонной и молочной кислот, способствующие нормализации рН и росту позитивной микрофлоры ЖКТ. Препарат способствует быстрому восстановлению позитивной микрофлоры кишечника, нарушенной во время применения антибиотиков или облучения, и показан при диспепсии, запорах, диарее, метеоризме, гастроэнтерите, аллергических кожных заболеваниях и острых кишечных инфекциях.
Проводимые российскими и зарубежными исследователями клинические работы показали высокую эффективность и безопасность использования препарата в клинической практике. Препарат Хилак форте используется в профилактике дисбактериоза после антибиотикотерапии [44], является эффективным средством для поддержания микробиоценоза и профилактики развития дисбактериоза [45], эффективен как адаптоген при острых респираторных инфекциях у детей [46], успешно используется пациентами с синдромом раздраженного кишечника [47–49]). При применении Хилака форте отмечена нормализация уровней и соотношений КЦЖК [50], он способствует ускорению выздоровления при острой кишечной инфекции [51, 52]. Применение Хилака форте также эффективно для пациентов с синдромом раздраженного кишечника: уже через 2 недели приема препарата наблюдались частичный или полный регресс субъективных жалоб, нормализация рН и микробного спектра фекалий [53, 54].
Особо следует отметить результаты комплексного рандомизированного исследования эффективности препарата [55] в группе 84 пациентов (36–74 лет) с функциональными запорами продолжительностью 1,5–27,0 лет (в среднем 8 лет). Пациенты 1-й группы (основной, n = 32) получали Хилак форте (40–50 капель 3 раза в сутки 4 недели) в составе комплексной терапии. Помимо значительного улучшения клинической симптоматики проведенное в данной работе бактериологическое исследование фекалий пациентов со II степенью дисбиоза кишечника выявило положительную динамику при приеме Хилака форте: в процессе лечения исчезали грибы рода Candida, протей, снижалось количество гемолизирующей формы E. coli. Терапия Хилаком форте приводит к определенным изменениям в профиле короткоцепочечных кислот: доля уксусной кислоты достоверно снижается (р < 0,001), увеличиваются доли масляной и пропионовой кислот (р < 0,01) [55]. В целом клинические исследования показали, что Хилак форте действительно оказывает дифференцированное влияние на выживаемость позитивной и патогенной микрофлоры, т. е. способствует выживанию позитивной микрофлоры кишечника и элиминации патогенной флоры, оказывая отчетливое оздоравливающее влияние на метаболом “микробного органа”.
Молекулярные механизмы воздействия компонентов беззародышевых экстрактов микробиоты.
Показания к применению препарата Хилак и хилак форте
Нарушение физиологической флоры тонкого и толстого кишечника (во время и после лечения антибиотиками или сульфаниламидными препаратами, лучевой терапии), хронические заболевания ЖКТ; синдром мальдигестии, диспепсии; диарея, метеоризм, запор; гастроэнтероколит, колит; нарушения функций ЖКТ, вызванные изменением климатичесого пояса; гипо- и антацидные состояния, в том числе в период беременности; аллергические заболевания кожи, крапивница (эндогенно обусловленная и хроническая экзема); после перенесенных острых кишечных инфекций (сальмонеллез и др.), в том числе у детей грудного возраста.
Применение препарата Хилак и хилак форте
Капли принимают внутрь до или во время приема пищи в достаточном количестве жидкости (за исключением молока) 3 раза в сутки: взрослые и дети в возрасте старше 12 лет — по 40–60 капель на прием; дети в возрасте старше 2 лет — по 20–40 капель на прием; дети в возрасте до 2 лет — по 15–30 капель на прием. После улучшения состояния суточная доза может быть снижена вдвое. Длительность лечения обычно составляет 2–4 нед. Необходимость более длительного применения определяет врач.
Особые указания
Во время лечения следует придерживаться ряда рекомендаций:
- Не запивать Хилак Форте молоком, молочными или кисломолочными продуктами
- Не принимать антацидные препараты, так как они нейтрализуют кислоты, входящие в состав «Хилак Форте»
- Открытый флакон следует хранить не более 1,5 месяца
- Лекарственное средство не требует специальных условий для хранения. Достаточно придерживаться температурного режима – от +4 до +25 градусов Цельсия.