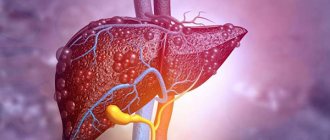
- Признаки и симптомы опухолей печени
- Диагностика опухолей печени
- Определение стадии злокачественных опухолей печени
- Лечение опухолей печени
- Результаты лечения злокачественных опухолей печени
- Что происходит после окончания лечения?
Злокачественные опухоли печени составляют 1-2% от числа всех опухолей детского возраста.
Мальчики болеют почти в 2 раза чаще девочек.
Среди опухолей печени у детей чаще всего диагностируется гепатобластома и гепатоцеллюлярный рак. К другим очень редким злокачественным опухолям относятся: эмбриональная саркома, рабдоидная опухоль и ангиосаркома.
В Западных странах гепатобластома встречается в 2 раза чаще гепатоцеллюлярного рака. Средний возраст детей на момент диагностики гепатобластомы — 1 год. После 5 лет эта форма опухоли печени выявляется очень редко. Средний возраст обнаружения гепатоцеллюлярного рака составляет 12 лет.
Доброкачественные опухоли печени являются еще более редкими и представлены гемангиомами, гамартомами и узловой гиперплазией.
Из факторов риска, повышающих вероятность возникновения злокачественных опухолей печени, следует отметить врожденные пороки развития, цирроз печени, полипоз толстого кишечника, глистные инвазии, вирусный гепатит В, обменные нарушения, афлатоксины, нитрозамины и некоторые другие.
Признаки и симптомы опухолей печени
Наиболее частым проявлением опухолей печени у детей является увеличение размеров живота и определяемое уплотнение. Из других симптомов следует отметить потерю аппетита и похудение. Жидкий стул или запоры встречаются редко.
Малокровие (анемия), повышение температуры, рвота и желтуха обычно появляются при далеко зашедшем опухолевом процессе, причем чаще у больных гепатоцеллюлярным раком.
В редких случаях у больных гепатобластомой отмечается преждевременное половое созревание за счет выработки опухолью гормона — человеческого хорионического гонадотропина.
1.Общие сведения
В сравнении с такими опасными, распространенными и широко обсуждаемыми заболеваниями печени, как цирроз, рак или вирусные гепатиты, проблема доброкачественных опухолей выглядит не столь острой. Вместе с тем, доброкачественные неоплазии в гепатологии все же не являются спорадической редкостью, – и по ряду причин (неспецифичность и слабая выраженность симптоматики, обоснованная настороженность врачей в отношении любых опухолевых процессов, недоступность объективного исследования в силу локализации и т.д.) зачастую становятся источником диагностических сомнений, затруднений или ошибок.
Названия доброкачественных опухолей традиционно производятся от названия той ткани, в которой начинается неопластический процесс. Среди доброкачественных опухолей печени абсолютным лидером являются опухоли, растущие из ткани сосудистых стенок, т.е. гемангиомы (до 90%); на втором месте по частоте встречаемости – опухоли железистой ткани, или аденомы (гепатоцеллюлярная аденома растет из паренхиматозных клеток печени, или гепатоцитов). Прочие разновидности (липомы, фибромы, гамартомы и т.д.) встречаются гораздо реже.
Обязательно для ознакомления! Помощь в лечении и госпитализации!
Диагностика опухолей печени
При ощупывании живота можно определить один или несколько опухолевых узлов в правом подреберье. Расширенная венозная сеть на передней брюшной стенке и асцит (жидкость) в животе может указывать на поражение печеночных вен и нижней полой вены.
Наиболее необходимым лабораторным методом диагностики злокачественных опухолей печени является определение в крови уровня особого белка — альфа-фетопротеина (АФП). Уровень его повышен у большинства пациентов с гепатобластомой и у 50% детей с гепатоцеллюлярным раком.
Увеличение количества тромбоцитов (тромбоцитоз) периферической крови является одним из признаков гепатобластомы.
Биопсия (взятие кусочка опухоли для микроскопического изучения) при помощи пункции или во время операции выполняется в тех случаях, когда данные проведенного всестороннего обследования сомнительны.
Рентгенография грудной клетки дает возможность обнаружить метастатическое поражение легочной ткани, которое встречается в 20% случаев на момент диагностики основной опухоли.
Рентгенография брюшной полости позволяет выявить кальцификаты (обызвествления) в опухолях печени и исключить другие опухолевые заболевания, например, метастазы нейробластомы.
Ультразвуковое исследование (УЗИ) помогает подтвердить происхождение опухоли из печени, уточнить ее расположение и распространение в органе, выявить поражение печеночных сосудов.
Компьютерная томография (КТ) с контрастированием, магнитно-резонансная томография (МРТ), радиоизотопное сканирование печени, ангиография (контрастное исследование сосудов) применяются для получения дополнительной информации, необходимой при планировании объема операции.
3.Симптомы и диагностика
Подавляющее большинство доброкачественных неоплазий печени являются бессимптомными, – точнее сказать, остаются таковыми длительное время, пока медленное увеличение в размерах не начнет сказываться на состоянии окружающих тканей и структур. В латентном, субклиническом периоде такие новообразования обнаруживаются лишь случайно. На этапе клинической выраженности чаще всего пациент ощущает тяжесть в подреберье, характерную практически для всех заболеваний печени, и боли ноющего или тянущего характера, не зависящие от приема пищи и обусловленные механическим давлением опухоли на смежные ткани. Иногда возникают симптомы диспепсии, очень редко формируются симптомокомплексы портальной гипертензии, нарушений оттока желчи, осложнения со стороны сердца и т.п.
Дифференциальную диагностику в подобных случаях облегчает доброкачественный характер опухоли, т.е. отсутствие метастазов, прорастания в другие органы, симптомов интоксикации, онкомаркеров в лабораторных анализах.
Решающей диагностической информативностью обладает пункционная биопсия, производимая под контролем УЗИ. Для уточнения габаритов, локализации, морфологических особенностей и других характеристик опухоли назначают КТ или МРТ; для исследования гемодинамических изменений, обусловленных крупной гемангиомой печени, применяют рентген-контрастную ангиографию и/или допплерографию.
О нашей клинике м. Чистые пруды Страница Мединтерком!
Определение стадии (распространенности) злокачественных опухолей печени
После всестороннего обследования уточняется стадия заболевания, которая важна для планирование лечения и оценки прогноза (исхода) болезни.
I стадия — опухоль полностью удалима
II стадия — после удаления опухоли остаются отдельные опухолевые клетки.
III стадия — разрыв опухоли во время операции, наличие пораженных лимфатических узлов или лишь частичное удаление опухоли.
IV стадия — наличие отдаленных метастазов
Симптомы рака печени
Рак печени может долгое время протекать бессимптомно. У многих пациентов его обнаруживают при проведении контрольных обследований или случайно, при обследовании по поводу другой патологии. Описаны случаи, когда у пациента была опухоль размером 15 см, а никаких клинических признаков при этом не было.
Уже на распространенных стадиях присоединяются следующие симптомы:
- Тяжесть и тупая боль в правом боку.
- Нарастающая слабость, быстрая утомляемость.
- Нарушение аппетита, тошнота, рвота.
- Увеличение объема живота из-за скапливающейся в брюшной полости жидкости (асцита).
- Расширение вен в области стенки живота.
- Пожелтение кожи и склер.
- Боль. Боль тем сильнее, чем больше растянута капсула печени. В ряде случаев она может отсутствовать.
Из клинических признаков присутствуют следующие:
- Увеличение размеров печени.
- Увеличение уровня билирубина. Он может быть повышен и на фоне цирроза.
- Увеличение размеров селезенки.
- Лихорадка, устойчивая к действию антибиотиков и противовоспалительной терапии.
- Желудочно-пищеводные кровотечения из варикозно-расширенных вен пищевода.
Стадии рака печени
Около 10-15% пациентов имеют признаки паранеопластического синдрома:
- Гипогликемия.
- Кожный зуд без желтухи.
- Остеопороз.
- Нарушение работы щитовидной и паращитовидной желез.
В ряде случаев первичные признаки со стороны печени отсутствуют, а симптомы появляются при развитии отдаленных метастазов, например, в легких, костях или головном мозге.
Лечение опухолей печени
Основным методом лечения опухолей печени является операция. Прогноз (исход) заболевания в основном зависит от того, насколько радикально (полностью) удалена опухоль.
Оперативное вмешательство у детей с гепатоцеллюлярным раком затруднено в связи с тем, что обычно имеются множественные опухолевые узлы внутри печеночной ткани.
Предоперационная химиотерапия с использованием винкристина, платины, адриамицина (доксорубицина), вепезида позволяет в ряде случаев уменьшить размеры гепатобластомы, что дает возможность в дальнейшем выполнить полное удаление опухоли.
В послеоперационном периоде химиотерапия назначается для уничтожения оставшихся опухолевых клеток. У больных с гепатоцеллюлярным раком химиотерапия малоэффективна.
Лучевая терапия может быть применена лишь с паллиативной целью для снятия боли и уменьшения проявлений желтухи.
Виды аденом печени
Аденома печени, как правило, локализуется в правой доли печени, имеет неоднородную структуру и находится вдали от кровеносных сосудов. Диаметр аденомы может составлять от нескольких мм до 20 сантиметров. В процессе пальпации данное образование является малочувствительным или болезненным узлом с однородной поверхностью. Аденомы печени могут быть как солитарными (одиночными), так и множественными. Ученые выделяют несколько видов аденом печени:
- холангиоаденома. Это доброкачественное новообразование состоит из клеток желчевыводящих протоков или из эпителия желчных протоков. Присуще больше женщинам, чем мужчинам;
- цистаденома. Является подвидом холангиоаденомы. Имеет злокачественный характер, представляет собой пузырь, заполненный прозрачной жидкостью с примесями холестерина, билирубина и др.;
- гепатоцеллюлярная аденома – опухоль, главным составляющим которой являются клетки печени гепатоциты.
Осложнения
Несмотря на то, что гемангиома не превращается в раковую, осложнения ее весьма серьезные. Наиболее частые из них:
- Происходит разрыв и начинается внутреннее кровотечение;
- Развивается тромбоз и опухоль уплотняется;
- При значительных размерах опухоли происходит сдавливание близрасположенных органов и сосудов.
На развитие опухоли во многом влияет содержание в крови эстрогенов, поэтому необходимо отслеживать ее развитие в период беременности либо в процессе применения контрацепции гормонального характера.
Введение
По определению патологоанатомов, фокальная нодулярная гиперплазия печени — это доброкачественное образование, относящееся к гамартомам, которое проявляется очаговой гиперплазией печеночных клеток, формирующих узелки паренхимы, окруженные фиброзными прослойками [1]. По международной классификации болезней (МКБ-10), это заболевание включено в рубрику «Другие уточненные болезни печени», К 76.8. В международной гистогенетической классификации опухолей печени и внутрипеченочных желчных протоков она фигурирует как «очаговая узловая гиперплазия». В литературе встречаются синонимы названия этого заболевания: «фибронодулярная гиперплазия» и «фокальный цирроз печени». По нашему мнению, термины «фокальная нодулярная гиперплазия» и «фокальный цирроз» не совсем удачны. Словосочетание «фокальная нодулярная» является по сути тавтологией, так как практически означает одно и то же (от лат. focus — очаг, nodulus — узел). Термин «фокальный цирроз» точно отражает морфологическую суть заболевания, но в сознании большинства клиницистов цирроз прочно ассоциируется с диффузным поражением печени. С нашей точки зрения, именно «фибронодулярная гиперплазия» (ФНГ) является вполне приемлемым с семантической точки зрения термином, поскольку наиболее четко соответствует морфологическому субстрату болезни — узел гиперплазии гепатоцитов с фиброзом.
Еще сравнительно недавно ФНГ относили к числу редких (3%) объемных поражений печени (ОПП) [2, 5, 6]. В настоящее время вследствие активного применения современных методов визуализации печени количество выявленных больных с ФНГ (как и очаговых заболеваний печени в целом) возросло [3, 12]. По данным литературы, ФНГ в структуре очаговых заболеваний печени занимает третье место среди доброкачественных ОПП после гемангиомы и аденомы [4, 8]. Этиология и патогенез ФНГ остаются неясными [11]. Теория об участии в развитии ФНГ гормональных контрацептивов не получила подтверждения, и в настоящее время большинство исследователей считают, что ФНГ является итогом прогрессирования врожденных или приобретенных сосудистых мальформаций, приводящих к гиперплазии гепатоцитов [8, 9, 14]. Макроскопически ФНГ чаще всего определяется в виде хорошо отграниченного от ткани печени, мягкоэластического образования, иногда плотного, желтого, вишневого, белесоватого, светло-коричневого или розоватого цвета, дольчатой структуры с наличием фиброзных прослоек, отходящих, как правило, от центрально расположенного рубца.
ФНГ — образование, визуально и пальпаторно зачастую малоотличимое от злокачественной опухоли. Макроскопическая картина определяется соотношением паренхиматозного, фиброзного и сосудистого компонентов, которое бывает различным, поэтому с полной уверенностью диагноз ФНГ может быть установлен только после гистологического исследования всего удаленного препарата. ФНГ может наблюдаться в виде одного или множества фокусов.
Микроскопическая картина схожа с таковой при истинном крупноузловом циррозе печени. Отмечается гиперплазия печеночной паренхимы, разделенной на узлы фиброзными прослойками; последние образуют рубцы звездчатой формы. Гепатоциты содержат избыточное количество гликогена и жира. В фиброзных прослойках имеются мелкие желчные протоки, иногда определяется воспалительная инфильтрация. Наблюдаются аномальные сосуды с утолщенными стенками. Процесс имеет очаговый характер, ткань печени вне очага выглядит неизмененной [8, 11].
Заболевание нередко протекает бессимптомно и является случайной находкой при УЗИ печени, выполненном по другому поводу. Клинические проявления (дискомфорт, чувство тяжести) обусловлены «масс-эффектом» и мало отличаются от таковых при иных ОПП. Специфическая лабораторная симптоматика отсутствует. ФНГ не озлокачествляется и крайне редко вызывает осложнения в виде внутрибрюшного кровотечения [13]. Описаны случаи регрессии опухоли вплоть до полного ее исчезновения [10]. При подтверждении диагноза ФНГ и отсутствии осложнений ряд авторов рекомендуют динамическое наблюдение, хотя подобная тактика дискутабельна [7, 9, 10]. Лечебная тактика при ФНГ остается спорной и, кроме того, в доступной литературе нами не обнаружено сообщений о попытках проследить «естественное» течение заболевания при отказе от операции. Это побудило нас поделиться собственным опытом лечения этого заболевания.
Цель исследования — ретроспективно проанализировать частоту ФНГ среди ОПП и лечебно-диагностическую тактику при ФНГ за два временных периода: с 1996 по 2005 г. и с 2006 г. по настоящее время.
Материал и методы
За последние 17 лет в стационаре лечено 1425 больных с ОПП. Наблюдали 53 больных с ФНГ, что составило 3,6% всех больных с ОПП и 11,06% больных с доброкачественными опухолями. Возраст больных с ФНГ варьировал от 12 до 77 лет, преобладали женщины — 44 (83,2%). 47% больных обращались с характерными для ОПП на ранней стадии развития жалобами — чувство тяжести, абдоминальный дискомфорт, в основе которых лежит растяжение глиссоновой капсулы печени растущей опухолью, в остальных наблюдениях образование случайно обнаруживали при УЗИ, реже при КТ («инциденталома»). Заключительный диагноз ФНГ являлся итогом применения комплексного диагностического алгоритма ведения больных с ОПП солидной структуры [6], включающего УЗИ как метод первичного выявления и мониторинга, СКТ и МРТ как методы уточняющей диагностики, по показаниям лапароскопию, биопсию, ангиографию, лапаротомию как окончательный этап диагностики. В наших наблюдениях опухолевые узлы чаще были одиночными, и лишь у одной больной отмечено наличие двух очагов в обеих долях печени. Диаметр образований в наибольшем измерении варьировал от 3,5 до 20 см. 40 из 53 больных с ФНГ оперированы. Объем операции определялся размерами и локализацией опухоли. Расширенная левосторонняя гемигепатэктомия выполнена в 1 наблюдении, левосторонняя — в 2, правосторонняя — в 1, бисегментэктомия — в 8, атипичная резекция печени — в 16, энуклеация опухоли — в 8 наблюдениях. Эксплоративная лапаротомия произведена 3 больным, лапароскопическая холецистэктомия по поводу калькулезного холецистита с биопсией обнаруженной опухоли — 1 больному. Летальных исходов и осложнений, связанных непосредственно с операцией на печени, не было. У больной У.
, 18 лет, с врожденным сахарным диабетом на 10-е сутки после левосторонней гемигепатэктомии отмечена декомпенсация диабета с последующим развитием синдрома полиорганной недостаточности. У другой больной 24 лет латентно протекающая порфирия манифестировала на 8-е сутки после правосторонней гемигепатэктомии развитием тяжелой полинейропатии. Летального исхода у обоих больных удалось избежать, но потребовалось длительное интенсивное лечение в условиях реанимационного отделения. Не оперированы и находятся под наблюдением с регулярным УЗИ 12 больных. Сроки наблюдения за больными с ФНГ составили от 1 года до 13 лет.
Результаты и обсуждение
Ретроспективный анализ историй болезни с 1996 г. позволил выделить два периода, на протяжении которых тактические подходы к ведению больных с ФНГ претерпели некоторые изменения. Период с 1996 по 2005 г. характеризовался преимущественным применением УЗИ в качестве основного средства диагностики очагового заболевания печени, при этом ФНГ фигурировала в качестве «редкого» заболевания печени. Эхосемиотика ФНГ была разработана слабо, «осознанной» диагностической и лечебной тактики не было. В этих условиях сам факт обнаружения ОПП неясной этиологии определял показания к оперативному лечению, а точный морфологический диагноз ФНГ устанавливали после операции. В этот период оперированы 22 больных, причем в 3 наблюдениях выполнена эксплоративная лапаротомия. Показания к оперативному лечению выставляли довольно широко, но от удаления опухоли при подтверждении ее доброкачественного характера при предполагаемом вмешательстве большого объема воздерживались. Это дало возможность проследить «естественное» течение ФНГ. Выяснилось, что тезис о «безобидности» течения ФНГ сомнителен. Подтверждением служат два наших наблюдения, опубликованные в журнале «Хирургия» за 2005 г. [7].
По мере накопления опыта в течение второго периода, с 2006 по 2013 г., стало очевидно, что ФНГ встречается чаще, чем предполагалось. В диагностике ФНГ главное место заняли СКТ и МРТ. Стали чаще ставить показания к динамическому наблюдению больных с ФНГ (при уверенности в отсутствии злокачественной опухоли). Мы располагаем опытом наблюдения «естественного» течения ФНГ, не потребовавшего оперативного лечения, у 12 больных. При этом в 11 наблюдениях диагноз ФНГ установлен по данным неинвазивных методов диагностики (УЗИ, СКТ, МРТ), в 1 — после лапароскопической холецистэктомии с биопсией опухоли. Размер образования у этих больных был небольшим (до 5 см в диаметре), клиническая симптоматика отсутствовала. Мониторинг с регулярным УЗИ в сроки от 1 года до 7 лет выявил незначительный рост образования лишь у 3 больных, что пока исключало необходимость операции. Кроме того, анализ течения заболевания у радикально оперированных за оба периода больных позволил убедиться в том, что после хирургического лечения при контрольном обследовании, включавшем УЗИ, СКТ, признаков рецидива ФНГ не выявлено ни в одном наблюдении. В связи с этим основной задачей второго периода (с 2006 г. по настоящее время) становится определение четких показаний как к оперативному лечению, так и к динамическому наблюдению лиц с ФНГ. Примером успешной активной лечебной тактики может служить следующее наблюдение.
У больного Л.
, 18 лет, при УЗИ и МРТ в IV и V сегментах печени обнаружено объемное образование диаметром до 15 см. Какие-либо специфические жалобы отсутствовали, однако, учитывая молодой возраст больного, размер образования, невозможность исключения его злокачественного характера, также предыдущий «отрицательный» опыт наблюдения, мы приняли решение об операции. 12.08.10 больной оперирован. При ревизии в IV (передний сектор) и V сегментах печени имеется большое бугристое образование диаметром 15 см, выступающее над диафрагмальной и висцеральной поверхностями, мягкоэластической консистенции, темно-вишневого цвета, с белесоватыми прожилками, распространяющееся на ложе желчного пузыря, большая часть опухоли находится в левой доле
(рис. 1)
.
Рисунок 1. Интраоперационная фотография. Фибронодулярная гиперплазия IV, V сегментов печени. а — диафрагмальная поверхность печени; б — висцеральная поверхность печени.
Выполнена левосторонняя расширенная гемигепатэктомия, холецистэктомия. Гистологическое заключение: фибронодулярная гиперплазия печени (рис. 2)
.
Рисунок 2. Микрофотография. Фибринодулярная гиперплазия. Окраска гематоксилином и эозином. Ув. 100. Послеоперационный период протекал без осложнений. За время наблюдения в течение 3 лет признаков рецидива заболевания нет. Полная социальная адаптация.
В практике хирургов-гепатологов ФНГ встречается не так редко. Следует заметить, что хирурги других специальностей, а также врачи-«визуалисты» недостаточно хорошо знакомы с этим заболеванием. На этапе амбулаторного обследования диагноз ФНГ был установлен только в 16 (30,7%) наблюдениях, что отражает как недостаточную осведомленность врачей-«визуалистов» об этом заболевании, так и объективные трудности диагностики, обусловленные вариабельностью соотношения в узле стромального, паренхиматозного и сосудистого компонентов. Чаще всего образование в печени на дооперационном этапе трактовали как гемангиому, рак печени, «объемное поражение печени неясного генеза». Исключить злокачественный характер патологического очага без операции далеко не всегда возможно, поэтому целесообразность лапаротомии как завершающего этапа диагностики в ряде наблюдений не вызывает сомнений. Целесообразность выполнения у всех больных предоперационной пункционной биопсии под контролем УЗИ или КТ представляется спорной. Часто приходится дифференцировать ФНГ со злокачественной опухолью печени, в частности гепатоцеллюлярным раком. Пункционная биопсия очага далеко не всегда информативна (репрезентативность биоптата) и окончательность гистологического заключения в таких ситуациях сомнительна. Кроме того, биопсия при раке чревата опасностью диссеминации либо имплантационного метастазирования. Мы согласны с мнением авторов, призывающих не выполнять предоперационную биопсию при подозрении на рак, поскольку этот фактор ухудшает прогноз заболевания [15]. При подозрении на гемангиому такая манипуляция в принципе противопоказана из-за угрозы внутрибрюшного кровотечения.
Исходя из нашего опыта, в настоящее время к длительному динамическому наблюдению больных даже с установленным и подтвержденным гистологически диагнозом ФНГ относимся с осторожностью. Обязательными условиями для этого следует считать возможность регулярного УЗ-мониторинга (1 раз в 6-8 мес) и достаточного комплайенса со стороны больного. Как и при большинстве ОПП, «выход» очага за пределы легкой операбельности чреват интраоперационными проблемами и тяжелым течением послеоперационного периода [6].
Таким образом, ФНГ — заболевание с неясным этиопатогенезом, неуправляемым течением и весьма неопределенным индивидуальным прогнозом. Рост опухоли может вести к смертельным осложнениям. В настоящее время представляется оптимальной следующая тактика при этом заболевании: оперативное вмешательство показано при «симптоматической» и быстрорастущей ФНГ, размерах очага свыше 5 см, невозможности исключения при полноценном обследовании его злокачественного характера. Динамическое наблюдение целесообразно при уверенности в диагнозе, небольших (менее 5 см) размерах очага, а также при общеизвестных факторах операционного риска (возраст, сопутствующие заболевания), так как опасность операции не должна превышать опасности самой болезни.
Комментарий от редколлегии
Широкое распространение и доступность современных неинвазивных методов диагностики (КТ, МРТ), а также увеличение их разрешающей способности привели к возрастанию частоты выявления бессимптомных очаговых образований печени. Подавляющее большинство из них являются доброкачественными, тем не менее перед врачом нередко встает вопрос о тактике ведения таких пациентов. Статья, посвященная фокальной нодулярной гиперплазии, одной из наиболее частых доброкачественных опухолей печени, безусловно, будет интересна хирургам-гепатологам, тем более, что русскоязычные публикации на эту тему единичны.
Для начала необходимо определиться с терминологией. В начале статьи авторы предлагают использовать термин «фибронодулярная гиперплазия». С этим можно соглашаться или нет, но для того, чтобы избежать путаницы и непонимания, лучше придерживаться международной терминологии, предложенной исследовательской группой в 1995 г. (Terminology of Nodular Hepatocellular Lesions. International Working Party. Hepatology, 1995), в которой данное образование определено как фокальная нодулярная гиперплазия (focal nodular hyperplasia) и предложены критерии, по которым его можно отличить от других регенераторных образований.
Неинвазивные методы играют главенствующую роль в диагностике ФНГ. МРТ и КТ обладают высокой чувствительностью и специфичностью, однако у ряда пациентов диагноз может оставаться сомнительным, и в этом случае оправдано выполнение биопсии, тем более, что предложены «большие» и «малые» критерии для интерпретации полученного при биопсии материала (A. Fabre и соавт., 2002). Авторы настороженно относятся к биопсии, опасаясь осложнений и имплантационного метастазирования в случае злокачественной опухоли, однако мы считаем, что для установления диагноза необходимо использовать весь арсенал имеющихся средств, и только при остающихся сомнениях прибегать к лапаротомии и резекции образования. Риски биопсии при соблюдении ряда правил считаем преувеличенными.
Мы придерживаемся сдержанной тактики ведения ФНГ, так как прогноз благоприятный: не зафиксировано случаев малигнизации, осложнения редки (описано всего несколько наблюдений разрыва опухоли с кровотечением), большинство опухолей бессимптомны, а размеры остаются стабильными в течение длительных сроков.
В связи с этим мы поддерживаем приведенные в статье показания для хирургического лечения: симптомная опухоль, ее рост, невозможность исключить злокачественное образование после всестороннего обследования. Важно отметить также, что симптомы ФНГ неспецифичны, поэтому исключение сопутствующей патологии органов брюшной полости, которая может обусловливать клиническую картину, является необходимым. Что касается рекомендации удалять образования, размер которых превышает 5 см, с этим можно не согласиться, так как на наличие симптомов влияет не только размер образования, но и его локализация и соседство окружающих органов. Кроме того, имеют значения размеры самого пациента и его органов. Например, ФНГ размером 10 см у крупного человека, расположенная интрапаренхиматозно, может никак себя не проявлять, в связи с чем необходимость резекции печени у него будет сомнительна.
Таким образом, при выборе тактики ведения у конкретного пациента следует ориентироваться на комплекс факторов, не подвергая его необоснованному риску хирургического вмешательства, так как летальность в группе пациентов с доброкачественными образованиями печени недопустима.
Современные методы лечения
Некоторые гемангиомы диагностируются при рождении или в раннем детстве (до 5 — 10% годовалых детей). Гемангиома обычно со временем уменьшается и в некоторых случаях может исчезнуть. Если она небольшая, стабильная и не вызывает никаких симптомов, ее можно контролировать с помощью визуальных исследований каждые 6 — 12 месяцев.
Лекарственных средств для лечения гемангиомы печени не существует. Для удаления опухоли может потребоваться операция – если она быстро растет или вызывает значительный дискомфорт или боль. Техника, называемая сосудистой эмболизацией, при которой перекрываются кровеносные сосуды, питающие гемангиому, может замедлить или обратить вспять ее рост.
Лечение доброкачественных новообразований
Из-за их доброкачественной природы и отсутствия известного злокачественного потенциала печеночные гемангиомы обычно не требуют лечения. Для больших, симптоматических гемангиом, которые влияют на качество жизни пациента или когда диагноз сомнительный, используется хирургическая резекция.
После постановки диагноза пациентам с аденомой печени следует прекратить применение КОК или любых анаболических стероидов. Разрыв аденомы может потребовать неотложного вмешательства для контроля внутреннего кровотечения. Хирургическая резекция классически показана для симптоматических аденом или образований размером более 5 см.
При узловых гиперплазиях в большинстве случаев нет показаний к хирургическому вмешательству, и лечение включает консервативное клиническое наблюдение у бессимптомных пациентов. Хирургическое вмешательство обычно назначается только при большой симптоматической опухоли или при сомнении диагноза. Некоторые авторы рекомендуют хирургическую резекцию опухолей, которые демонстрируют прогрессивный рост, или опухолей размером более 10 см.
Осложнения, прогноз и профилактика
С целью профилактики патологии необходимо вести здоровый образ жизни.
Прогноз в целом благоприятный при своевременно начатом лечении.
При поздней диагностике возможно массивное кровотечение с развитием анемии, разрыв опухоли, переход в злокачественную форму.
С целью профилактики необходимо вести здоровый образ жизни: бросить вредные привычки, правильно питаться, заниматься физическими упражнениями (ходьба, плавание, бег, фитнес). По возможности отказаться от использования гормональных препаратов, если их прием не является необходимым для лечения основного заболевания.
Профилактика рака печени
Учитывая то, что рак печени в основном развивается на фоне цирроза, всем таким пациентам показано регулярное обследование. Проводится анализ на определение уровня онкомаркера альфа-фетопротеина и выполнение УЗИ печени.
Пациентам не из группы риска, т. е. у которых нет цирроза и сопутствующих заболеваний, можно предложить следующие мероприятия:
- Вакцинация против гепатита В.
- Регулярное обследование на определение маркеров вирусных гепатитов, и при постановке диагноза проведение своевременной антивирусной терапии.
- Отказ от употребления алкоголя.
- Соблюдение принципов рационального питания.
- Контроль веса и диабета.
- Контроль метаболического синдрома.
Факторы риска рака печени
Основным фактором риска развития рака печени является цирроз самой разной этиологии. По сути цирроз является исходом хронического заболевания печени, которое в ряде случаев может длиться годами. Основными причинами развития цирроза являются:
- Хронические гепатиты В и С.
- Алкоголизм. При длительном и обильном употреблении алкоголя может развиться острый гепатит с трансформацией в хронический.
- Некоторые паразитарные инвазии.
- Гемохроматоз.
- Аутоиммунные гепатиты.
- Токсическое отравление афлотоксинами или винилхлоридом.
- Инсулинрезистентный сахарный диабет.
Только у 10% пациентов с раком печени опухоль развивается на фоне здоровой печеночной ткани.
Популярные вопросы и ответы
На вопросы о гемангиоме печени мы попросили ответить рентгенэндоваскулярного хирурга Александра Ширяева.
Какие могут быть осложнения при гемангиоме печени?
Гемангиома печени может привести к разрыву тканей, внутреннему кровотечению и геморрагическому шоку. Есть вероятность, что из-за больших размеров образования могут быть сдавлены близлежащие органы, сосуды и нервы.
Когда нужна операция при гемангиоме печени?
Выбор тактики лечения гемангиомы во многом зависит от ее размеров и формы. Опухоли размером 4 — 6 см (в объеме) не требуют оперативных действий. В этом случае за состоянием пациента просто наблюдают, через 3 месяца с момента обнаружения делают УЗ-контроль, а в дальнейшем его повторяют каждые 6 — 12 месяцев.
В более сложной ситуации специалист подберет гормональную терапию, лучевую терапию или хирургическое вмешательство.