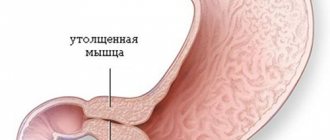
Пилоростеноз (высокая желудочно-кишечная непроходимость)
Главная угроза – полная невозможность прохождения пищи из желудка в нижележащие отделы ЖКТ и развитие истощения.
- Механизм развития
Постъязвенный рубцовый стеноз привратника (пилоростеноз) или двенадцатиперстной кишки – осложнение язвенной болезни выходного отдела желудка (пилорического отдела) или луковицы двенадцатиперстной кишки. На месте зажившей язвы образуется рубец, ткань в области рубца стягивается, прохождение пищи из желудка в двенадцатиперстную кишку затрудняется. Это место постоянно травмируется пищевыми массами, на него воздействует соляная кислота. Возникает хроническое воспаление, зона сужения прогрессирует, проход становится ещё уже. Затем развивается декомпенсация: пища проходит с большим трудом, желудок расширяется и теряет свою перистальтическую функцию. У пациентов с признаками декомпенсированной дуоденальной непроходимости желудок может достигать огромных размеров, пища перестает проходить дальше в кишку, процесс пищеварения останавливается. Возникает истощение.
- Симптомы
Язва проявляется болями в брюшной полости. Это могут быть голодные боли или боли после еды. Сужение выходного отдела желудка проявляет себя тошнотой и чувством переполнения желудка после приёма пищи. В норме человек должен просыпаться утром с чувством голода, но пациент с высокой непроходимостью просыпается с чувством переполнения желудка. Декомпенсация стеноза характеризуется рвотой пищей, съеденной за 2-3 часа до этого. Декомпенсация – угрожающее жизни состояние, следует незамедлительно обратиться к врачу.
- Диагностика
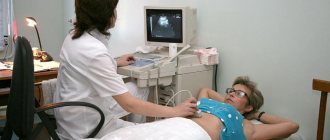
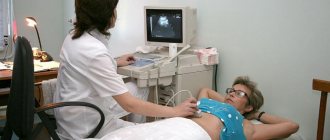
Для того, чтобы диагностировать постъязвенный рубцовый стеноз выходного отдела желудка, применяются компьютерная томография с водорастворимым контрастом и рентгенологическое исследование с водорастворимым контрастом или с барием. Чтобы понять, через какое время у пациента происходит эвакуация содержимого желудка в нижележащие отделы ЖКТ, врач даёт пациенту барий, делает рентгеновский снимок, и видит, куда барий распространился. Затем снимки делаются через 3, 6, 12 часов – это позволяет оценить динамику прохождения контраста и степень стеноза. В Ильинской больнице пациентам с подозрением на высокую кишечную непроходимость всегда выполняется эндоскопическая диагностика: с помощью эндоскопа врач точно локализует место стриктуры и определяет объем хирургической помощи.
Пилоростеноз
Источник изображения: Designua / Shutterstock
- Баллонная дилатация зоны рубцовой стриктуры
Если пациент обратился в Ильинскую больницу на ранней стадии заболевания, и у него диагностирован компенсированный рубцовый язвенный стеноз выходного отдела желудка, то пациенту можно предложить эндоскопический метод лечения — баллонную дилатацию зоны рубцовой стриктуры. Через рот в зону сужения проводится тонкий эндоскоп. Под одновременным контролем эндоскопа и рентгена через инструментальный канал эндоскопа в зону сужения доставляется специальный баллон. Баллон раздувается, зона стеноза растягивается, непроходимость разрешается. Давление в баллоне контролируется манометром, что исключает повреждение и разрыв тканей желудка. Рентген-эндоскопически ассистированная баллонная дилатация зоны рубцово-язвенного сужения выходного отдела желудка или луковицы двенадцатиперстной кишки — деликатная, но действенная операция.
- Лапароскопическая пилоропластика
Если степень желудочно-кишечной непроходимости не позволяет провести баллонную дилатацию, но серьёзной формы декомпенсации еще нет – хирурги Ильинской больницы выполняют пациенту лапароскопическую операцию – пилоропластику. Через небольшие разрезы на брюшной стенке (размером около 10 мм) в брюшную полость вводятся лапароскоп и хирургические манипуляторы. Одновременно через рот в просвет желудка вводится эндоскоп. С помощью лапароскопических инструментов хирург рассекает суженную зону двенадцатиперстной кишки и выходного отдела желудка в продольном направлении, а сшивает в поперечном, тем самым значительно расширяя место сужения и разрешая непроходимость. Второй хирург ассистирует ему из просвета желудка с помощью эндоскопа, обеспечивая максимальную безопасность манипуляций. Это малотравматичная операция, дающая устойчивый положительный эффект.
- Лапароскопическая субтотальная резекция желудка
Если у пациента диагностирована выраженная декомпенсированная стадия желудочно-кишечной непроходимости, то вышеперечисленные операции не эффективны. В этом случае хирурги Ильинской больницы выполняют лапароскопическую субтотальную резекцию желудка. Желудок у пациента сильно увеличен, его перистальтика нарушена, в желудке скапливается пища. Поэтому хирургу необходимо резецировать большую часть этого растянутого и потерявшего свои функции желудка. Операция выполняется лапароскопически через четыре небольших разреза. Оставшаяся часть желудка подсоединяется к петле тощей кишки — формируется анастомоз. На следующий день после такой операции пациент уже может пить воду. Через день ему проводят рентгенологическое исследование с водорастворимым контрастом для контроля состоятельности анастомоза. Если всё в порядке, то пациенту сразу разрешают есть жидкую пищу.
Симптоматика острого и хронического дуоденита
Если говорить о заболевании в целом, то воспалительный процесс обычно протекает вяло, проявляя себя нарушениями аппетита и общего самочувствия и некоторыми диспепсическими симптомами (например, урчанием в животе, метеоризмом). Больные часто словно погружены в себя, раздраженные. Дети обычно «худосочные», плохо растут. Но клиническая картина дуоденита может развиваться и весьма бурно, особенно при сопутствующем заражении лямблиями.
Острый дуоденит. Внезапно и, как правило, после обильного переедания может возникнуть приступ сильной боли в животе, от которой пациенты буквально корчатся. Боль не купируется никакими препаратами. Лицо больного покрывается капельками пота. Многократная рвота может поначалу навести на мысль об остром панкреатите, однако сухой и обложенный белым налетом язык ясно свидетельствует о раздражении брюшины, лейкоцитозе и субфебрилитете. Вся эта симптоматика не оставляет врачам выбора: единственный выход – хирургическое вмешательство. Так, на операционном столе и ставится порой точный диагноз – острый дуоденит.
К симптомам острого дуоденита относятся также боли и чувство распирания в районе желудка (так называемой эпигастральной области), обильное слюнотечение, тошнота и рвота, снижение аппетита. Нередко повышается температура тела. Приступ может сопровождаться головными болями, слабостью и артериальной гипотензией.
Хронический дуоденит. Это течение заболевания отличается многообразием клинических проявлений, которые затрудняют постановку диагноза: хронический дуоденит нередко принимают за другие болезни органов пищеварительной системы. Так, чаще всего он «симулирует» язву двенадцатиперстной кишки, но с меньшими болями и с меньшей выраженностью сезонных обострений. Когда же на первый план выступают нарушения нормальной деятельности желудка (диспепсические расстройства), то болезнь поначалу неправильно диагностируют как гастрит.
Существуют формы этого «многоликого» недуга, которые проявляют себя как хронический холецистит или панкреатит: возникают боли в правом подреберье либо опоясывающие боли в верхней части живота, непременно усиливающиеся после приема жирной пищи.
У молодых женщин чаще встречается нервно-вегетативная форма дуоденита. Здесь обычно преобладают вегетативные расстройства: повышенная утомляемость или, напротив, возбудимость; слабость, головные боли и т.д. При смешанных проявлениях хронического дуоденита сочетаются симптомы самых разных клинических форм. Но нередко, особенно у пожилых людей, болезнь протекает в скрытой форме, то есть бессимптомно.
Отдельно следует сказать о флегмонозном дуодените. Он встречается редко, но, как говорится, «бьет метко». Это острое гнойное воспаление, которое поражает стенку двенадцатиперстной кишки. Может возникать как первичный фактор вследствие проникновения вредных микробов (стафилококков, стрептококков и др.) через слизистую в глубинные слои стенки кишки (такое происходит при глубоких язвах, распадающихся опухолях и механическом повреждении слизистой оболочки). Вторичный же флегмонозный дуоденит обычно развивается в результате распространения патогенных микроорганизмов из каких-либо первичных очагов (например, при фурункулезе или абсцессах различной локализации).
Диагностика заболеваний двенадцатиперстной кишки
Основные методы, используемые в диагностике дуоденита, следующие:
- Гастродуоденоскопия – наиболее информативный метод, который помогает определить или исключить заболевание. Такая эндоскопическая процедура определяет, есть ли воспалительные процессы на слизистой, развились ли эрозии, язвы двенадцатиперстной кишки, дуодено-гастральный рефлюкс. Исследование проводится на голодный желудок с возможной предварительной седацией пациента.
- Исследование биопсийного материала либо дыхательного уреазного теста помогает определить наличие инфекции хеликобактер.
- Рентгенологические исследования (проводятся реже).
При обращении в клинику для диагностики необходимо помнить о том, что большинство предлагаемых процедур проводится на голодный желудок. Предварительная консультация гастроэнтеролога позволит вам правильно подготовиться к тестам, что значительно увеличит их информативность.
Введение
Постбульбарные язвы двенадцатиперстной кишки (ДПК) в диагностическом и тактико-техническом плане относятся к «трудным» дуоденальным язвам. По данным литературы, они встречаются в 0,9-25% общего числа наблюдений язвенной болезни ДПК [1, 3, 7, 10, 12, 15].
По клиническому течению постбульбарные язвы отличаются от язв двенадцатиперстной кишки обычной локализации «агрессивностью», более высокими показателями кислотопродукции в желудке, резистентностью к противоязвенной терапии, высокой частотой развития осложнений, особенно пенетрации язвы в соседние органы, и острым кровотечением. Пенетрация постбульбарных язв, по материалам литературы, составляет от 25,3 до 90% и создает значительные технические трудности при выполнении оперативных вмешательств [7, 9, 10].
Частота стенозирования ДПК при постбульбарных язвах колеблется от 45,l до 65,5% [7, 10, 15].
При хирургическом лечении постбульбарных язв и стенозов многие хирурги отдают предпочтение резекции желудка, в том числе «на выключение» язвы. Результаты этой операции нельзя считать удовлетворительными вследствие высокой летальности и значительного числа осложнений. Основной причиной смерти является несостоятельность швов дуоденальной культи, которая чаще всего наблюдается у больных, оперированных по поводу так называемых трудных язв [9, 12].
Ряд хирургов при постбульбарных стенозах альтернативой резекции желудка считают селективную проксимальную ваготомию (СПВ) с дуоденопластикой, которая сохраняет анатомическую и функциональную целостность пилорического сфинктера [5, 13, 16].
Время показало, что резекция желудка при постбульбарных стенозах не может оставаться альтернативой в арсенале способов оперативных вмешательств из-за высокой частоты послеоперационных осложнений и летальности. Однако нельзя категорически высказываться против резекции желудка, в том числе «на выключение» язвы, как метода хирургического лечения осложненных дуоденальных язв, так как хирургическая ситуация порой диктует свои условия.
Материал и методы
Наши выводы основаны на данных многолетних наблюдений за 214 больными, которым в плановом порядке были выполнены различные оперативные вмешательства по поводу постбульбарных дуоденостенозов. Среди них мужчин было 169 (78,9%), женщин — 45 (21,1%), их соотношение составляет 3,8:1. Возраст больных варьирует от 16 до 66 лет.
В фазе обострения язвенной болезни поступили 182 (85,1%) больных. Рубцовый стеноз диагностирован у 85 (39,7%), рубцово-язвенный — у 129 (60,3%) больных. Пенетрация язвы в соседние органы или образования имелась у 184 (85,9%) больных, в том числе с периульцерозным воспалительным инфильтратом у 85 (68,5%).
Дуоденостеноз в стадии компенсации диагностирован у 24 (11,2%) больных, в стадии субкомпенсации — у 75 (35,1%), декомпенсации — у 115 (59,7%) больных.
С целью диагностики постбульбарных стенозов нами применялись все методы, используемые для диагностики язвенной болезни ДПК. Рентгенологически порой трудно установить локализацию стеноза из-за выраженного нарушения эвакуаторной функции желудка. Рентгенологически диагноз постбульбарного стеноза установлен лишь у трети (33,8%) больных. При гастродуоденоскопии из-за анатомических нарушений в пилородуоденальной зоне нередко наблюдается гипердиагностика постбульбарного стеноза, поэтому основным способом точной диагностики локализации постбульбарных стенозов остается интраоперационная ревизия после мобилизации ДПК по Кохеру.
Результаты и обсуждение
При выполнении операции важное значение имеет правильная тактика хирурга у каждого конкретного больного с постбульбарным стенозом ДПК. Характер хирургических вмешательств при постбульбарных дуоденостенозах представлен в таблице.
Не оправдано стремление обязательно произвести радикальную операцию с удалением язвы, которую рекомендуют ряд хирургов [2, 5, 6, 8]. Такая тактика приводит к возникновению непоправимых интраоперационных и послеоперационных осложнений: повреждению элементов гепатодуоденальной связки, послеоперационному панкреатиту, несостоятельности швов культи ДПК и др. Во избежание этих осложнений необходимо в каждом конкретном наблюдении, учитывая характер и распространенность патологического процесса, избрать индивидуальную тактику и произвести адекватное оперативное вмешательство.
Радикальное удаление стенозирующей язвы показано лишь при отсутствии периульцерозного воспаления и пенетрации, т.е. при рубцовом стенозе. Однако такая радикализация не всегда оправдана, так как связана с риском повреждения гепатикохоледоха, поджелудочной железы, вскрытия просвета ДПК. Нередко при этом искусственно создается «трудная» дуоденальная культя, обработка которой производится в условиях дефицита ткани кишки. Последний всегда имеет место и наиболее выражен при пенетрирующих дуоденальных язвах.
Резекция желудка с радикальным иссечением язвы применена в 63 (29,4%) наблюдениях, в том числе в 6 в сочетании с селективной ваготомией. В 39 наблюдениях она завершена формированием гастроэнтероанастомоза по Гофмейстеру-Финстереру, в 23 — по Ру, в 1 — по Бальфуру. Однако, если при этом имелась реальная опасность повреждения элементов гепатодуоденальной связки или образования «трудной» дуоденальной культи в силу обширного рубцово-спаечного процесса или периульцерозного воспалительного инфильтрата, мы отказывались от такого вмешательства в пользу резекции желудка «на выключение» или СПВ с дренирующими или дуоденопластическими операциями.
Ретроспективный анализ показал, что при резекции желудка с радикальным иссечением язвы технические трудности выделения и ушивания культи ДПК наблюдались почти у каждого второго (32) больного. В 17 (24,6%) наблюдениях отмечалось прорезывание швов и вскрытие просвета кишки, что вынуждало прибегнуть к «открытой» обработке культи ДПК. В раннем послеоперационном периоде несостоятельность швов дуоденальной культи наблюдалась у 3 (4,3%) больных, которым было выполнено радикальное иссечение постбульбарной язвы.
При стенозирующих пенетрирующих в соседние органы постбульбарных язвах с периульцерозным воспалительным инфильтратом в 39 (18,2%) наблюдениях была применена резекция желудка «на выключение» язвы, из них в 8 в сочетании с селективной ваготомией. Гастроеюноанастомоз по Ру применен в 14 из них, по Гофмейстеру-Финстереру — в 25 наблюдениях.
При выполнении резекции желудка «на выключение» язвы некоторые авторы отдают предпочтение подпривратниковому варианту [11], который, на наш взгляд, менее надежен, создает технические трудности при ушивании культи ДПК, так как формировать ее приходится в условиях дефицита и воспалительных изменений тканей. Последние всегда имеют место и более выражены при пенетрирующих язвах ДПК.
При выполнении надпривратникового варианта резекции желудка для выключения язвы мы, как и другие авторы, выделяем ряд обязательных этапов операции. Среди них важнейшими являются демукозация, сохранение хорошего питания оставшейся части преддверия, тщательный гемостаз при формировании серозно-мышечной манжетки, соблюдение асептики.
Всем этим требованиям в большей мере отвечает усовершенствованный Г.П. Рычаговым [14] способ укрытия дуоденальной культи при резекции желудка для выключения язвы по Вильмансу-Кекало.
Решение о выполнении резекции «на выключение» следует принимать заблаговременно, так как мобилизация антрального отдела с перевязкой сосудов может привести в последующем к некрозу культи.
Суть метода заключается в том, что отступя на 4 см выше привратника и от правой желудочной и желудочно-сальниковой артерии еще на 2 см кверху циркулярно рассекаем серозно-мышечный слой стенки преддверия и отпрепарируем его от слизистой. Сосуды, идущие в подслизистом слое, захватываем изогнутыми по оси зажимами «москит», пересекаем и лигируем. Такой способ обработки сосудов обеспечивает идеальный гемостаз, сухое операционное поле и минимальную травму серозно-мышечной манжетки. Мобилизацию слизистой продолжаем ниже привратника на 0,5-1 см и на этом уровне уже на слизистую ДПК накладываем аппарат УО-40, прошиваем скрепочным швом и выше линии прошивания слизистую пересекаем. Серозно-мышечную манжетку, образовавшуюся в результате демукозации преддверия, ушиваем двухрядным швом. Первым рядом швов подшиваем переднюю губу манжетки к мышце привратника, вторым фиксируем заднюю губу к передней.
В раннем послеоперационном периоде несостоятельности швов дуоденальной культи не наблюдалось ни разу.
В отдаленные сроки после резекции желудка «на выключение» пептическая язва соустья наблюдалась у 1 (2,1%) больного. Она была обусловлена сохраненной непрерывной кислотопродукцией в желудке вследствие экономной резекции желудка без ваготомии. По этой же причине возник рецидив язвенной болезни у 1 (1,4%) больного после резекции желудка с радикальным иссечением язвы.
Селективная ваготомия с антрумэктомией применена в 14 (1,3%) наблюдениях. При этом 8 больным выполнена резекция желудка «на выключение» язвы, 6 — с радикальным удалением язвы. Показанием к выполнению ваготомии в сочетании с экономной резекцией считаем чрезмерно высокие показатели кислотопродукции в гуморальную фазу желудочной секреции.
Отдельно следует рассматривать вопрос о применении органосохраняющих операций при постбульбарных стенозах.
Альтернативой резекции желудка при постбульбарных стенозирующих и пенетрирующих язвах является СПВ с дуоденопластикой. Однако выбор такого варианта операции имеет особенности. При этом необходимо учитывать следующие факторы: уровень кислотопродукции в гуморальную фазу желудочной секреции, степень сохранности резервных возможностей моторно-эвакуаторной функции желудка, наличие и выраженность периульцерозного воспалительного процесса в зоне стеноза и хроническое нарушение дуоденальной проходимости.
Ваготомия выполнялась при вагусном и смешанном типе желудочной секреции. При смешанном типе желудочной секреции, если уровень кислотопродукции в гуморальную фазу превышал 35 мекв/ч, отдавали предпочтение экономной резекции (антрумэктомии) в сочетании с селективной ваготомией.
Поскольку более 2/3 больных имели декомпенсированный стеноз, вопрос о применении СПВ в сочетании с дуоденопластикой или другим видом дренирующей операции решался на основании изучения резервных возможностей моторно-эвакуаторной функции (МЭФ) желудка. Для определения последней нами разработаны критерии, получаемые с помощью рентгенопланиметрии на фоне стимуляции МЭФ желудка церукалом (10 мг внутривенно).
В зависимости от степени сохранности резервных возможностей МЭФ желудка при декомпенсированном стенозе мы выделяем три уровня: хорошие, удовлетворительные, неудовлетворительные. Эти критерии позволяют прогнозировать риск развития постваготомического гастростаза (ПВГ) и определить возможность применения ваготомии у больных с декомпенсированным дуоденостенозом. Как показала наша практика, при хороших резервных возможностях МЭФ желудка риск развития ПВГ минимален, при удовлетворительных — не исключено развитие гастростаза I-II степени, хорошо поддающегося консервативному лечению. При неудовлетворительных резервных возможностях МЭФ желудка имеется риск развития ПВГ III степени или гастроплегии.
Исходя из этого, СПВ с дуоденопластикой или дренирующими операциями в случае декомпенсированного дуоденостеноза применяли только при хороших и удовлетворительных резервных возможностях МЭФ желудка. При неудовлетворительных резервных возможностях МЭФ желудка отдавали предпочтение резекции желудка с формированием гастроеюнального анастомоза по Ру.
Наличие нарушения МЭФ ДПК является препятствием для применения ваготомии с дуоденопластикой, так как значительно ухудшает результаты операции. Его необходимо диагностировать до операции с помощью рентгенологического исследования ДПК или заподозрить на основании косвенных признаков (дуоденогастральный рефлюкс высокой степени). При невозможности рентгенологической диагностики дуоденостаза существуют интраоперационные признаки хронического нарушения дуоденальной проходимости: расширение просвета нисходящей и особенно нижнегоризонтальной ветвей ДПК более 3,5 см, видимое преобладание диаметра ДПК над диаметром начального отдела тощей кишки, изменение тонуса ДПК, уменьшение диаметра ДПК в ответ на механическое раздражение более чем на 1/2 или менее чем на 1/3 первоначальной величины [12].
Ряд хирургов при выполнении дуоденопластики производят иссечение измененного рубцами участка кишки вместе с язвой [4, 5, 13]. При выполнении плановых операций больным с дуоденостенозом, на наш взгляд, такая тактика приводит к возникновению непоправимых осложнений. Попытка иссечения язвы при дуоденопластике значительно усложняет операцию и лишает ее одного из важнейших качеств — безопасности.
СПВ с дуоденопластикой (69 больных) или поперечным гастродуоденоанастомозом (7) при компенсированном постбульбарном дуоденостенозе применена в 10 наблюдениях, при субкомпенсированном — в 44, декомпенсированном — в 22 наблюдениях.
Интраоперационных осложнений, связанных с выполнением ваготомии и дренирующих желудок операций, мы не наблюдали. В раннем послеоперационном периоде развитие ПВГ у больных с субкомпенсированным и декомпенсированным стенозом является обычным из-за исходного нарушения МЭФ желудка. Явления ПВГ легко поддаются консервативному лечению и ликвидируются в течение 2-3 нед.
Постваготомический гастростаз III степени наблюдался у 3 (4%) больных: после дуоденопластики — у 1, после формирования поперечного гастродуоденоанастомоза — у 2. Эти явления ликвидированы консервативными мероприятиями.
В отдаленные сроки результаты органосохраняющих операций с ваготомией были наиболее благоприятными. Рецидив язвенной болезни наблюдался лишь у 2 (2,6%) больных. Демпинг-синдром легкой степени отмечен у одного больного после поперечной гастродуоденостомии. У одной больной после СПВ с дуоденопластикой имел место щелочной рефлюкс-гастрит вследствие некорригированного хронического нарушения дуоденальной проходимости функционального генеза.
Больным с высоким операционно-анестезиологическим риском вследствие сопутствующих заболеваний или тяжести алиментарно-дистрофических нарушений при крайне выраженной стадии стеноза, а также детям в возрасте до 16 лет при неудовлетворительных резервных возможностях МЭФ желудка стремились выполнять органосохраняющие операции без ваготомии, т.е. восстанавливали проходимость ДПК путем изолированной дуоденопластики, которая применена в 22 (10,3%) наблюдениях. Результаты этих операций у всех больных были благоприятными. В отдаленном периоде МЭФ и размеры желудка полностью восстановились, кислотопродуцирующая функция желудка по сравнению с дооперационными показателями снизилась на 30-40% за счет ликвидации гастростаза и восстановления антродуоденального механизма «кислотного тормоза». Превентивное применение антисекреторных препаратов снижает риск рецидива язвы у данной категории больных.
Как критерий эффективности методов хирургического лечения постбульбарных язв, осложненных дуоденостенозом, в отдаленные сроки после операции использовали результаты изучения качества жизни пациентов. При этом руководствовались рекомендациями Европейской ассоциации гастроэнтерологов, модифицированной Н.Н. Крыловым [6].
Максимальное число баллов, а значит более высокое качество жизни, было отмечено после СПВ с дуоденопластикой (129,3) и после СПВ с дренирующими желудок операциями (128,4). Далее по степени восстановления качества жизни пациентов стоит резекция желудка по Py (126,1). Эти показатели достоверно не отличались от таковых у здоровых лиц (130,1). Достоверно худшие результаты получены после резекции желудка по Гофмейстеру-Финстереру (112,7). Таким образом, органосохраняющие операции и резекции желудка более адекватно восстанавливают утраченное за время заболевания качество жизни пациентов. Измерение уровня качества жизни является важным критерием для оценки эффективности методов хирургического лечения больных язвенной болезнью.
Таким образом, постбульбарные дуоденостенозы относятся к категории «трудных» дуоденальных язв в тактико-техническом плане. Хирургическое лечение этой категории больных должно быть индивидуализированным. Операцией выбора при постбульбарных дуоденостенозах является селективная проксимальная ваготомия с дуоденопластикой. Расширение показаний к такой операции во многих наблюдениях позволяет избежать проблемы «трудной» дуоденальной культи. Однако в зависимости от конкретной клинической ситуации оправдано применение как резекции желудка «на выключение», так и с радикальным иссечением язвы. Однако при восстановлении непрерывности желудочно-кишечного тракта целесообразно отдавать предпочтение гастроеюноанастомозу по Ру. У больных с высоким операционно-анестезиологическим риском или в случае если резекция желудка нежелательна по другим соображениям, возможно применение дуоденопластики или дренирующей операции без ваготомии.
Симптомы заболеваний двенадцатиперстной кишки
Патологии отделов тонкого кишечника обычно проявляются следующим образом:
- Боли в эпигастральной области, которые возникают чаще через несколько часов после еды, ночью.
- Тошнота.
- Отсутствие аппетита.
- Тяжесть после еды
- Белый налет на языке.
Также заболевания дуодена могут сопровождаться симптомами, которые характерны для поражений поджелудочной железы, желчного пузыря и других органов. Это свидетельствует о значительном распространении патологического процесса.