Введение
В Российской Федерации октреотид считается обязательным препаратом в лечении острого панкреатита [1, 3]. В протоколах лечения панкреатита Японии, Великобритании, Международной ассоциации панкреатологов и Американской ассоциации панкреатологов его не рекомендуют применять [7, 10—12]. Это обосновывается результатами рандомизированных исследований, не выявивших улучшения результатов лечения больных при использовании препарата [5, 6, 8, 9]. Наиболее значимым и самым крупным (302 больных) из таких исследований было мультицентровое (32 центра в Европе), рандомизированное двойное слепое исследование, выполненное W. Uhl и соавт. [9].
Однако в исследовании есть ряд недостатков, позволяющих считать представленные авторами результаты не вполне адекватными. Во-первых, анализ проводился на общей совокупности больных, крайне разнородных по тяжести своего состояния. Такой подход к исследованию мог не выявить дифференцированной реакции отдельных групп пациентов на применение препарата. Во-вторых, некорректным выглядит сравнение результатов лечения группы, получавшей октреотид в дозе 100 и 200 мкг 3 раза в сут, так как тяжесть состояния больных в последней была на 2 балла по APACE II выше (7 баллов и 9 баллов соответственно). В-третьих, наиболее существенным недочетом явился статистический анализ полученных в ходе исследования данных. Он основывался на одномерном подходе без учета действия на исход заболевания других (помимо октреотида) потенциальных предикторов (факторов тяжести состояния и лечебных факторов). Все эти недостатки самого важного исследования по изучаемой проблеме позволяют утверждать, что оценка эффективности октреотида при лечении больных панкреонекрозом остается актуальной.
Нами проведено исследование, целью которого являлась оценка влияния октреотида на динамику летальности и распространенность некроза поджелудочной железы и парапанкреатической клетчатки при изначально тяжелом течении деструктивного панкреатита (9 и более баллов по шкале APACHE II).
Выбор категории пациентов для исследования основывался на высокой частоте их неблагоприятных исходов заболевания.
Побочные эффекты препарата Октреотид
Возможны боль, ощущение зуда или жжения, краснота и припухлость в месте инъекции, анорексия, тошнота, рвота, спастическая боль в животе, вздутие живота, метеоризм, жидкий стул, диарея и стеаторея, явления, напоминающие острую кишечную непроходимость (прогрессирующее вздутие живота, выраженная боль в эпигастральной области, мышечная защита), образование камней в желчном пузыре (при длительном использовании у 10–20% больных), острый панкреатит, выпадения волос, нарушения функции печени, в том числе острый гепатит без холестаза, гипербилирубинемия, сопровождающиеся повышением показателей щелочной фосфатазы, γ-глутамилтрансферазы и в меньшей степени трансаминаз, снижение толерантности к глюкозе, стойкая гипергликемия или гипогликемия (при длительном применении).
Материал и методы
В мультицентровое исследование включены 204 больных с тяжелым течением панкреонекроза, лечившихся в хирургических отделениях Ярославской областной клинической больницы (с 1996 по 2011 г.), городской больницы № 1 Вологды (с 2005 по 2010 г.), городской больницы № 2 Костромы (с 2008 по 2009 г.) и городской больницы № 1 Рыбинска (с 2008 по 2009 г.).
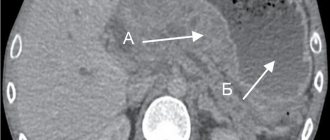
Критерии включения пациентов в исследование были следующие: 1) обнаружение некроза поджелудочной железы и парапанкреатической клетчатки в ходе операции; 2) наличие некроза поджелудочной железы и парапанкреатической клетчатки на вскрытии трупов умерших неоперированных больных; 3) наличие у неоперированных больных жидкостного образования с секвестрами по результатам ультразвукового исследования, компьютерной томографии и магнитно-резонансной томографии; 4) тяжесть состояния при поступлении 9 и более баллов по шкале APACHE II.
Критериями исключения пациентов из исследования являлись: 1) наличие злокачественного новообразования; 2) отсутствие некрозов поджелудочной железы во время операции, при вскрытии трупов умерших, при ультразвуковом исследовании, МРТ, КТ; 3) тяжесть состояния при поступлении менее 9 баллов по шкале APACHE II.
Важным условием проведения исследования была полная выборка пациентов с тяжелым течением панкреонекроза за весь календарный год в каждом из указанных стационаров, что фактически позволило считать его проспективным по принципу состояния на момент времени в прошлом [2].
В ходе проведения исследования пользовались международной классификацией острого панкреатита, в соответствии с которой определяли прогнозируемую тяжесть течения заболевания [4].
В начале исследования использовали традиционный подход к анализу, аналогичный применявшемуся W. Uhl и соавт. [9]. Больные были разбиты на две группы: основную (n
=114), в которой применяли октреотид в стандартных дозах (100 мкг 3 раза в сутки подкожно и внутримышечно), и контрольную (
n
=90), в которой препарат не применяли. Методами одномерной статистики сравнивали показатели летальности и распространенности некроза в основной и контрольной группах. Для корректной интерпретации полученных результатов группы дополнительно (в отличие от исследования W. Uhl и соавт.) сравнивали еще и по другим потенциальным предикторам (факторам тяжести состояния при поступлении в стационар и лечебным факторам), которые также могли влиять на исход заболевания.
Распространенным считали некроз, захватывающий один из отделов поджелудочной железы или существенный объем парапанкреатической клетчатки. Распространенность некроза устанавливали во время оперативного вмешательства или (у неоперированных больных) по результатам вскрытия. Кроме того, очаговым считали панкреонекроз у больных, для излечения которых не требовалось оперативное вмешательство.
Факторами тяжести состояния являлись возраст (количество лет), пол (1 — мужской, 0 — женский), тяжесть органных дисфункций по шкале APACHE II (в баллах), величина температуры тела (°С), частота пульса (в 1 мин), значение среднего артериального давления (в мм рт.ст.), частота дыхания (в 1 мин), уровень сознания по шкале Глазго (в баллах), количество лейкоцитов крови (тыс. ·109/л), палочкоядерных нейтрофилов (в %), уровень в крови креатинина (в мг/дл), калия (в ммоль/л), натрия (в ммоль/л), глюкозы (в ммоль/л), парциальное напряжение кислорода крови (в мм рт.ст.), значения pH крови. Эти параметры оценивали при поступлении.
Из лечебных предикторов оценивали и сравнивали методики антибактериальной профилактики (аминогликозиды, пенициллины и цефалоспорины первого поколения — код 1; цефалоспорины третьего и четвертого поколения — код 2; фторхинолоны и карбопенемы — код 3), частоту применения кваматела (1 — применяли, 0 — не применяли), антиферментной терапии (1 — применяли, 0 — не применяли), ранней нутритивной поддержки (1 — применяли, 0 — не применяли), нутритивной поддержки при гнойных осложнениях (1 — применяли, 0 — не применяли).
Сравнивали результаты лечения больных основной и контрольной групп только в случае отсутствия достоверных различий этих групп по указанным выше факторам тяжести состояния и лечебным факторам. Достоверными считали различия, если значение p
для используемого критерия было ниже 0,05. Использовали
t
-критерий Стьюдента при нормальном распределении значения признака,
U
-критерий Манна—Уитни при сравнении групп с отличным от нормального распределения значения признака, критерий χ2 при сравнении групп по качественному признаку.
На втором этапе исследования применяли альтернативный вариант анализа, не требующий формирования групп сравнения и их рандомизации, как в исследовании W. Uhl и соавт., — определение совокупного влияния факторов на исход лечения. Результатом его являлась модель прогноза вероятности наступления события (изменения результата лечения) по имеющимся факторам тяжести состояния при поступлении в стационар и факторам проводимого лечения.
Для оценки динамики летальности использовали модель пропорциональных рисков Кокса. Ее особенностью являлась оценка влияния этих параметров при каждом случае законченного наблюдения за временем жизни больных, т. е. до момента смерти.
Совокупное влияние факторов на распространенность некроза оценивали методом логистической регрессии.
При отборе переменных в модели для регрессионного анализа использовали метод обратного исключения [2].
Влияние вошедших в модель предикторов и точность всей модели в целом считали достоверными, если значения p
критерия χ2 были меньше критического значения (0,05) для всех вошедших факторов и в целом для модели.
Степень влияния предиктора определяли по величине регрессионного коэффициента. Большие его числовые значения свидетельствовали о большей силе влияния. Направленность влияния оценивали по знаку коэффициента. При отрицательном значении регрессионного коэффициента считали влияние параметра тяжести состояния или лечения обратнозависимым, т. е. его увеличение снижало вероятность летального исхода, при положительном значении коэффициента увеличение действия фактора указывало на увеличение вероятности летального исхода.
Статистическую обработку материала проводили с помощью программы StatSoft, Inc. (2007), Statistica version 8.0 и MedCalc, версия 10.5.0.0.
Особые указания по применению препарата Октреотид
При опухоли гипофиза, секретирующей гормон роста, необходим строгий контроль врача за больными, получающими октреоид, так как возможно увеличение размера опухолей с развитием такого серьезного осложнения, как сужение полей зрения. При лечении эндокринных опухолей пищеварительного тракта и поджелудочной железы октреотидом в редких случаях может наступить внезапный рецидив заболевания. У больных с инсулиномой на фоне лечения октреоидом может отмечаться увеличение выраженности и продолжительности гипогликемии. У больных сахарным диабетом, получающих инсулин, октреоид может снижать потребность в инсулине. Опыт применения октреоида в период беременности и кормления грудью отсутствует, в этот период препарат назначают только по абсолютным показаниям.
Результаты и обсуждение
Уже на этапе одномерного анализа, т. е. при простом сравнении групп, выявлена достоверно меньшая летальность в группе больных, получавшей октреотид, по сравнению с группой, его не получавшей (52% против 72%; критерий χ2; p
=0,003). При сравнении групп по распространенности некроза поджелудочной железы и парапанкреатической клетчатки также установлено, что в основной группе распространенный некроз встречался достоверно реже, чем в контрольной (64% против 77%; критерий χ2;
p
=0,051). Таким образом, оценка эффективности октреотида методом одномерного статистического анализа, применяемого только у больных с прогностически тяжелым течением заболевания, а не на общем числе больных панкреатитом, как в исследовании W. Uhl и соавт., показала уменьшение летальности и распространенности некроза.
Для адекватной интерпретации этого результата и исключения возможности опосредованной корреляции было проведено сравнение групп по остальным потенциальным предикторам, которые тоже могли влиять на летальность и распространенность некроза. Анализ тяжести состояния пациентов обеих групп при поступлении практически не выявил их различий (табл. 1). Интегральный показатель органных дисфункций (по шкале APACHE II) в обеих группах не различался (12,0±3,3 балла в основной против 12,0±3,3 балла в контрольной; t
-тест;
p
=0,959) (см. рисунок).
Таблица 1. Различия факторов тяжести состояния больных в основной и контрольной группах
Тяжесть состояния пациентов при поступлении у больных с изначально тяжелым течением заболевания.
Однако различия по лечебным факторам были существенны. Исключить тот факт, что выявленное снижение летальности и распространенности некроза в группе пациентов, получавших октреотид, было обусловлено более частым применением на ранней стадии заболевания нутритивной поддержки (критерий χ2; p
=0,000) и панкреотропных антибиотиков (
U
-тест;
p
=0,000) (табл. 2), а не использованием октреотида, оказалось невозможным. В связи с этим для установления совокупного с другими факторами влияния октреотида на летальность был использован способ статистического анализа — модель пропорциональных рисков Кокса.
Таблица 2. Различия лечебных факторов в основной и контрольной группах
Анализ Кокса (табл. 3) позволил построить значимую модель факторов лечения и тяжести состояния, влияющих на летальность (р
=0,000). Октреотид входил в состав модели предикторов (
р
=0,000).
Таблица 3. Результаты регрессии Кокса
Более того, регрессионный коэффициент у октреотида оказался наибольшим из числа всех предикторов, входящих в модель (β= –0,8). Это означало, что сила его влияния на изменение летальности являлась наибольшей среди всех факторов, входящих в модель. Знак регрессионного коэффициента «–» указывал на то, что факт законченности наблюдения за временем жизни пациента (соответствие факту летального исхода) и назначение октреотида находятся в обратной зависимости, т. е. назначение октреотида уменьшало вероятность летального исхода у больных деструктивным панкреатитом.
Для определения влияния назначения октреотида на распространенность некроза поджелудочной железы и парапанкреатической клетчатки использовали логистический регрессионный анализ (табл. 4), который позволил построить значимую модель взаимного влияния факторов (p
=0,0001). В эту модель наряду с другими предикторами, взаимно влияющими на развитие распространенного некроза, вошел октреотид (
p
=0,033) как фактор с самым сильным влиянием, регрессионный коэффициент составил –0,875. Знак регрессионного коэффициента «–» указывал на то, что изменение распространенности некроза поджелудочной железы и назначение октреотида находятся в обратной зависимости, т. е. назначение октреотида уменьшало вероятность распространенности некроза у пациентов с деструктивным панкреатитом.
Таблица 4. Результаты логистической регрессии по распространенности некроза
Таким образом, при использовании модели пропорциональных рисков Кокса выявлена закономерность, которая заключалась в том, что применение октреотида оказывает очень сильное влияние на снижение летальности при изначально тяжелых формах панкреонекроза. При использовании логистической регрессии установлено, что октреотид является самым значимым фактором, влияющим на уменьшение распространенности некроза поджелудочной железы и парапанкреатической клетчатки у больных с тяжелым течением панкреонекроза.
Данные проведенного исследования позволяют рекомендовать назначение октреотида больным с изначально тяжелым течением панкреонекроза.
Показания к применению препарата Октреотид
Акромегалия (контроль основных проявлений заболевания и снижения уровня гормона роста и соматомедина С в плазме крови в тех случаях, когда эффект хирургического лечения, лучевой терапии и лечения агонистами допамина не достаточен); облегчение симптомов эндокринных опухолей пищеварительного тракта и поджелудочной железы: карциноидные опухоли с наличием карциноидного синдрома; ВИПомы; глюкагономы; гастриномы/синдром Золлингера — Эллисона (обычно в комбинации с блокаторами Н2-гистаминовых рецепторов); инсулиномы (для контроля гипогликемии в предоперационный период, а также для поддерживающей терапии); соматолибериномы; рефрактерная диарея у больных СПИДом; профилактика осложнений после операций на поджелудочной железе; остановка кровотечения и профилактика повторного кровотечения из варикозно расширенных вен пищевода у больных с циррозом печени (в комбинации со специфическими лечебными мероприятиями, например, эндоскопической склерозирующей терапией).