Классификация
Основными характеристиками ЯК, согласно классификации, принято считать форму заболевания (тип течения), протяженность воспаления в толстой кишке, активность воспаления и тяжесть течения.
В соответствии с этими категориями определяют следующие клинические варианты ЯК [1, 4]:
• острая форма – первая атака болезни длительностью до 6 месяцев; может проявляться в двух вариантах: в фульминантной форме, характеризующейся быстрым нарастанием клинических симптомов и тяжелым течением, и в форме с постепенным началом и неярко выраженной клинической картиной;
• рецидивирующая форма с циклическим интермиттирующим течением со сменой обострений и ремиссий;
• непрерывная форма с упорным, как правило, вялотекущим течением, умеренной активностью воспаления в слизистой оболочке и отсутствием эндоскопической ремиссии в течение 6–8 месяцев при условии адекватной терапии.
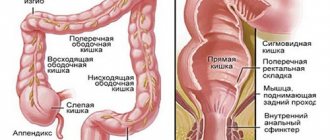
По протяженности воспалительного процесса в толстой кишке при ЯК в соответствии с Монреальской классификацией выделяют [5]:
• дистальный ограниченный колит – проктит;
• левосторонний колит – включает проктосигмоидит или более обширное диффузное поражение толстой кишки от ануса до селезеночного угла;
• распространенный колит – поражение толстой кишки, протяженное более чем до селезеночного угла, включая тотальный ЯК.
Клиническая картина
В мировой практике тяжесть атаки (обострения) ЯК оценивают с помощью индекса активности этого заболевания. Существует несколько индексов активности ЯК (Рахмилевича, Мэйо, оксфордский индекс, шведский индекс, система оценки тяжести по Truelov и Witts, Монреальская классификация). Среди специалистов нет единого мнения относительно предпочтительности применения какого-то конкретного индекса, т. к. все они недостаточно валидированы. В настоящее время есть тенденция дополнительно использовать уровень С-реактивного белка (СРБ) для оценки активности, что нашло отражение в Европейском консенсусе (ЕССО-консенсусе) по диагностике и лечению ЯК. В этом документе обсуждаются все индексы, причем эксперты делают следующий вывод: в настоящее время для оценки тяжести ЯК необходимо учитывать все параметры заболевания – клинические, лабораторные, инструментальные и гистологические [4]. Экспертный совет Российской группы по изучению воспалительных заболеваний кишечника (ВЗК) предлагает комплекс критериев, включающий легкоопределяемые параметры обострения ЯК, в т. ч. уровень СРБ. Этот комплекс шире обычно используемого при оценке индексов активности, поэтому более информативен. Набор оцениваемых параметров заболевания в большей степени, чем любые индексы (раздел 2.2.2.), соответствует экспертной оценке ЕССО-консенсуса, учитывает и клинические, и лабораторные проявления заболевания. Эта система оценки представляет собой расширенную модификацию критериев тяжести ЯК, предложенных Truelov и Witts [6]. В соответствии с выраженностью клинико-лабораторных симптомов выделяют легкое, среднетяжелое и тяжелое течение ЯК (см. таблицу).
Клиническая картина ЯК включает несколько групп симптомов [1]:
• кишечные (кровь в стуле, диарея, тенезмы);
• системные внекишечные аутоиммунные проявления (артропатии, поражения кожи, афтозный стоматит, поражения глаз, первичный склерозирующий холангит и др.);
• синдром эндотоксемии (общая интоксикация, фебрильная лихорадка, тахикардия, анемия, увеличение СОЭ, лейкоцитоз со сдвигом лейкоцитарной формулы до незрелых форм, токсическая зернистость нейтрофилов, повышение уровня острофазных белков – СРБ, серомукоида, фибриногена);
• метаболические расстройства (потеря массы тела, обезвоживание, гипопротеинемия, гипоальбуминемия, гипокалиемия и другие электролитные нарушения).
Выбор тактики лечения при разных клинических вариантах болезни Крона
В клинической картине БК с поражением кишечника присутствуют четыре основных синдрома: кишечный синдром, эндотоксемия, внекишечные проявления и синдром мальабсорбции. Кишечные симптомы в активную фазу заболевания включают диарею и боль в животе. Диарея, наиболее типичный симптом, встречается в 70–80% случаев БК тонкой, подвздошной или толстой кишки. Выделение крови с калом при этом необязательно. Этот симптом появляется только при левосторонней и дистальной локализации процесса в толстой кишке. Несмотря на отсутствие видимой примеси крови в стуле, для БК характерна прогрессирующая железодефицитная анемия. Боль в животе постоянного или приступообразного характера обычно соответствует месту поражения и формирования абдоминального инфильтрата, но может быть и разлитой, не локализованной. В ряде случаев острые приступы боли могут быть единственным симптомом на протяжении нескольких лет. Причина боли часто не устанавливается. В конечном счете, больных оперируют с подозрением на острый аппендицит. При лапаротомии обнаруживаются явления терминального илеита или тифлита. Приступы боли обычно сопровождаются подъемом температуры до 38–39°С. Лихорадка, показатели периферической крови (лейкоцитоз, увеличение СОЭ, токсигенная зернистость нейтрофилов), увеличение в крови С–реактивного белка, серомукоида и фибриногена свидетельствуют об остром воспалении и отражают синдром эндотоксемии в период атаки заболевания [2]. Возможны эпизоды лихорадки без абдоминальной боли на протяжении нескольких лет до появления первых кишечных симптомов. Упорная диарея, воспалительный процесс с экссудацией белка в просвет кишки и повышенный катаболизм белков приводят к значительной потере веса, метаболическим расстройствам (обезвоживание, гипокалиемия, гипонатриемия, гипопротеинемия и др.) и развитию синдрома мальабсорбции. БК часто сопровождается внекишечным системным поражением органов, что отражает аутоиммунный компонент в патогенезе заболевания. Для БК характерны такие внекишечные проявления, как узловатая эритема, гангренозная пиодермия, афтозный стоматит, различные артропатии, в том числе HLA В27 ассоциированный ревматоидный артрит и анкилозирующий спондилоартрит и сакроилеит (болезнь Бехтерева), витилиго, псориаз. Частота разных системных проявлений болезни находится в интервале 5–20%. По нашим данным, общая их частота составляет 62%, из них почти у 25% больных отмечаются артропатии. Ревматоидный артрит и болезнь Бехтерева встречаются в равных долях с частотой 8% [2,3]. Характер гистологических изменений и глубина поражения кишечной стенки при трансмуральном воспалении определяют спектр осложнений БК. Наиболее типичные и часто встречающиеся осложнения: воспалительные стриктуры с последующим развитием кишечной непроходимости, абдоминальные инфильтраты и абсцессы, межкишечные и наружные (кишечно–кожные) свищи. При поражении аноректальной области формируются парапроктиты, перианальные и ректовагинальные свищи и глубокие анальные трещины. При оценке тяжести БК учитывается характер и выраженность клинических симптомов и осложнений. Принято оценивать тяжесть болезни по «индексу активности БК» – СDАI (Crohn’s disease activity index), называемому также индексом Беста [3,5]. Этот индекс включает ряд клинических признаков, каждый из которых в зависимости от их присутствия или выраженности оценивается определенным количеством баллов. Расчет индекса проводится по специальной формуле. Индекс активности БК включает следующие критерии: частота жидкого стула за неделю, наличие болей в животе и их интенсивность, общее самочувствие (хорошее, удовлетворительное, плохое, очень плохое), системные проявления и/или анальные проявления (трещины, свищи, абсцессы) (есть, нет), использование опиатных антидиарейных средств (лоперамид), лихорадка (> 37,5°С), гематокрит, степень потери массы тела, наличие пальпируемого инфильтрата в брюшной полости. Принято, что индекс менее 150 расценивается, как ремиссия БК, индекс 150–220 соответствует низкой активности и легкому течению заболевания, 221–450 характеризует среднюю тяжесть БК, выше 450 баллов соответствует высокой активности воспаления и тяжелому течению [1]. Лечение больных БК представляет весьма трудную проблему, т.к даже при адекватной терапии у большинства пациентов заболевание имеет прогрессирующий характер с развитием осложнений или формированием непрерывных форм заболевания. Лечение должно проводиться дифференцированно с учетом локализации и протяженности воспалительного процесса, вида и характера осложнений и тяжести заболевания. Задачей лечения БК является купирование обострения, достижение и поддержание ремиссии. Базисная патогенетическая терапия БК включает три группы лекарственных препаратов: кортикостероидные гормоны, препараты 5–аминосалициловой кислоты (5–АСК) и иммуносупрессоры [1,2]. В настоящее время терапию, направленную на индукцию ремиссии у больных с легким или среднетяжелым течением БК, традиционно начинают с назначения препаратов 5–АСК – месалазина или сульфасалазина. В случае недостаточной эффективности аминосалицилатов назначают метронидазол и/или ципрофлоксацин. При отсутствии адекватного терапевтического ответа применяют кортикостероиды. При тяжелом течении используют стероидные гормоны, как терапию первой линии, а в случае рефрактерности к стероидам (стероидорезистентности или стероидозависимости) используют препараты резерва – иммуносупрессоры. Такие установившиеся подходы не являются дифференцированными и не учитывают накопленные на сегодняшний день данные доказательной медицины, позволяющие взвесить соотношение между эффективностью, безопасностью и переносимостью лекарственных средств и разработать оптимальные подходы к лечению при разном течении и разных формах заболевания. Аминосалицилаты Сульфасалазин и месалазин являются высоко эффективными базисными препаратами для лечения язвенного колита легкой и средней степени тяжести. Это позволило предположить, что препараты могут быть столь же эффективны при БК. На сегодняшний день они прочно вошли в лечебные схемы БК. Однако результаты контролируемых испытаний опровергают целесообразность подобного подхода. Изучению эффективности и безопасности сульфасалазина при БК было посвящено несколько плацебоконтролирумых клинических исследований, а также сравнительных исследований с глюкокортикоидами [5–8]. Результаты этих исследований свидетельствуют, что хотя эффективность сульфасалазина была выше, чем плацебо, но тем не менее уступала даже низким дозам системных кортикостероидов (0,25 мг/кг/сут.). В отличие от язвенного колита даже при легком течении БК сульфасалазин проявляет низкую активность. Положительный результат лечения сульфасалазином был получен лишь у больных с преимущественным поражением толстой кишки, что объясняется его непосредственной активацией ферментами толстокишечной флоры, и только при легком течении заболевания [9]. На терапию сульфасалазином отвечали лишь пациенты, не получавшие предварительную гормональную терапию, в то время как у получавших кортикостероиды препарат был не эффективен [7]. Все вышесказанное позволяет утверждать, что сульфасалазин имеет ограниченные возможности применения у больных только с легким течением БК с преимущественной локализацией в толстой кишке. Хорошо известные побочные эффекты сульфасалазина, возникающие у 10–30% больных, также ограничивают возможности его применения [9,10]. Таким образом, доказанная низкая эффективность сульфасалазина в сочетании с широким спектром побочных реакций не позволяют рекомендовать его для терапии больных БК с терминальным илеитом или илеоколитом, ограниченные показания имеются при лечении БК толстой кишки легкого течения. Месалазин лишен побочных эффектов сульфасалазина и не уступает ему по эффективности. Препараты таблетированного месалазина, производимые в разных странах, сходны по действию и эффективности и представляют собой 5–АСК в защитном покрытии. Они различаются характером энтеросолюбильного покрытия (эудрагитное, акриловое или этилцеллюлозное) и, соответственно, местом и скоростью освобождения 5–АСК в кишечнике [2]. Клиническая эффективность месалазина коррелирует с внутрипросветной концентрацией 5–АСК, поэтому локализация поражения обязательно должна учитываться при его назначении. Месалазин в качестве терапии первой линии у пациентов с легкой и умеренной БК используют 75% врачей [11]. Результаты клинических испытаний, однако, противоречивы. Месалазин в различных дозах был изучен в нескольких двойных слепых плацебо–контролируемых исследованиях [12,13,15]. В некоторых из них по способности вызывать ремиссию у пациентов с БК препарат в дозе 2–4 г в сутки не превосходил плацебо. Однако при анализе обобщенных данных 3 исследований с применением относительно высокой дозы месалазина (4–4,5 г/сут.) было выявлено статистически достоверное отличие от плацебо [11]. Месалазин в дозе 2 г в сутки значительно уступает стероидам (преднизолону, метилпреднизолону и будесониду), повышение дозы до 4,5 г дает сравнимые результаты [20,23,24,25]. В сравнительном исследовании с будесонидом (9 мг/сут.) месалазин (4 г/сут.) уступал глюкортикоиду по способности индуцировать ремиссию у пациентов с легкой и среднетяжелой формой БК [16]. Побочные эффекты при применении месалазина развиваются достаточно редко. Таким образом, не все результаты исследований в равной мере позитивны в отношении месалазина. Минимальная эффективная доза при БК с легким течением составляет 4 г в сутки, хотя в некоторых исследованиях количество больных было недостаточным для значимых выводов. С учетом низкой частоты побочных эффектов по сравнению с сульфасалазином и системными стероидами месалазин может быть рекомендован в качестве начального пробного лечения при легком течении БК, но частота положительных результатов недостаточно высока [4,11]. Общая эффективность препаратов 5–АСК не превышает 30%. Не доказана целесообразность их использования в качестве противорецидивной терапии. Системные глюкокортикостероиды Глюкокортикостероиды используются в терапии воспалительных заболеваний кишечника уже в течение 50 лет и традиционно являются препаратами первой линии при тяжелой БК [1,2,4]. Однако в контексте вышесказанного стероиды следует рекомендовать при среднетяжелом тяжелом течении заболевания и в случае неэффективности 5–АСК при легком течении [4,11]. Эффективность кортикостероидов и выраженность побочных эффектов зависят от скорости их метаболизма в печени, биодоступности, аффинности к рецепторам и от других параметров. Препаратом выбора считается преднизолон и его метилированные аналоги (метилпреднизолон). Средняя доза преднизолона внутрь в период атаки БК может составлять 40–60 мг, однако более эффективной следует считать дозу из расчета 1 мг/кг массы тела в сутки, а в очень тяжелых случаях доза может быть увеличена до 1,5–2 мг/кг в сутки. Применение высоких доз стероидов внутрь при тяжелой атаке БК конкурирует по эффективности с внутривенной высокодозной гормональной терапией (250–500 мг метилпреднизолона или гидрокортизона в сутки в течение 7 дней). Применение преднизолона в минимальной и средней дозе 0,25–0,75 мг кг/сут. приводило к улучшению у 60% больных, по сравнению с 30% в группе плацебо [7]. Более убедительные результаты были получены в отношении 6–метилпреднизолона в дозе 48 мг [8]. Другие исследования подтвердили, что системные стероиды при БК проявляют более высокую активность, чем плацебо, сульфасалазин, антибиотики и азатиоприн, однако их применение сопряжено с высокой частотой побочных явлений [13,15,17,18–23]. Переносимость кортикостероидов в значительной степени зависит от пути введения, дозы, продолжительности терапии, половой и индивидуальной чувствительности к препаратам. Распространенные побочные эффекты включают лунообразное лицо, стероидный диабет, остеопороз, изменения настроения, бессонницу, отеки, прибавку в весе, стрии. Таким образом, при доказанной высокой эффективности системных стероидов в индукции ремиссии при БК их длительное применение ограничено частыми и разнообразными побочными эффектами. По той же причине невозможно применять стероиды для поддержания ремиссии. Топические стероиды Необходимость использовать в лечении БК преимущественно стероидные гормоны и ограничения, обусловленные их побочными эффектами, привели к созданию безопасной альтернативы системным стероидам, не уступающим им по эффективности. Новая группа препаратов получила название «топических» стероидов. Это гормоны местного действия, создающие высокую концентрацию препарата в очаге поражения (в кишке) и практически не имеющие побочных эффектов [11,24–26]. В России в 2004 году зарегистрирован один из самых эффективных топических стероидов для лечения БК – будесонид. Будесонид продемонстрировал аналогичную активность с системными кортикостероидами, отличаясь при этом лучшей переносимостью и меньшим влиянием на гипоталамо–гипофизарно–адреналовую систему. Преимущества будесонида перед системными стероидами заключаются в особенностях его фармакодинамики. Прежде всего будесонид обладает высоким сродством к глюкокортикоидным рецепторам в тканях–мишенях (в данном случае к рецепторам слизистой оболочки кишки), во много раз превышающим аффинность традиционных средств: преднизолона и гидрокортизона. Так, афинность будесонида к стероидным рецепторам в 100 раз выше, чем у гидрокортизона, в 50 раз выше, чем у преднизолона и примерно в 18 раз выше, чем у метилпреднизолона. Кроме того, у будесонида минимальная способность всасываться из желудочно–кишечного тракта, низкая системная биодоступность (не более 10%) по сравнению с преднизолоном и гидрокортизоном и высокий пресистемный метаболизм. Последнее качество обеспечивает отсутствие в крови токсичных метаболитов после первого прохождения препарата через печень. Указанные свойства будесонида позволяют в определенной мере повысить эффективность лечения больных, нуждающихся в гормональной терапии. Активность препарата повышается благодаря высокому сродству к стероидным рецепторам, микрогранулированной галенической форме с высвобождением высоких концентраций в терминальном отделе подвздошной и в толстой кишке. Отсутствие побочных эффектов, свойственных стероидам системного действия, обусловлено низкой всасываемостью из просвета кишки в сочетании с высоким пресистемным метаболизмом и низкой системной биодоступностью. Привлекательные особенности будесонида делают возможным длительный прием препарата для купирования атаки БК без опасности развития побочных эффектов. Дискутируется вопрос о применении будесонида для противорецидивной терапии этого заболевания [27,28]. Рандомизированные кинические исследования продемонстрировали сходную эффективность системных стероидов и будесонида при значительно меньшем числе побочных эффектов последнего [20,23,29,30]. Оптимальная доза будесонида составила 9 мг в сутки, длительность лечения 12–16 недель с последующей постепенной отменой. Будесонид оказался эффективен преимущественно при среднетяжелом течении БК в форме терминального илеита и илеоколита и в этих случаях должен быть препаратом первой линии [4,11,26]. С нашей точки зрения, его следует применять и при легком течении БК той же локализации. Не показан будесонид при БК с системными аутоиммунными проявлениями. При тяжелом течении БК эффективность препарата в указанной дозе недостаточна. Иммуносупрессоры При отсутствии ответа на лечение гормонами, в случаях стероидорезистентности и стероидозависимости назначают препараты резерва – иммуносупрессоры [32–35]. Применяют азатиоприн и 6–меркаптопурин, метотрексат и циклоспорин А. Данные об эффективности иммуносупрессоров при БК весьма противоречивы. Частота достижения клинического эффекта и выхода в ремиссию как для азатиоприна, так и для метотрексата не превышает 70% [32]. Циклоспорин при БК менее эффективен, его действие проявляется больше у больных язвенным колитом. Применение иммуносупрессоров в определенной мере ограничено широким спектром побочных эффектов. Для азатиоприна это тошнота, рвота, диарея, гриппоподобный синдром с повышением температуры и миалгией, угнетение костного мозга с лейкопенией, нейтропенией (реже с агранулоцитозом), тромбоцитопенией. Прием азатиоприна может также сопровождаться гепатотоксическими реакциями в виде цитолиза и холестаза, панкреатитом, развитием полиневритов. Считается, что препарат повышает риск малигнизации, хотя многие оспаривают это положение [36]. Побочные эффекты развиваются с частотой 6–20%. Метотрексат является средством выбора у больных БК, не ответивших на лечение стероидами и азатиоприном [34,37]. Частота побочных эффектов при приеме метотрексата составляет 10–20% (среди них – тошнота, рвота, диарея, язвенный стоматит, лейкопения, тромбоцитопения, анемия, гепатотоксическое действие, легочный фиброз, алопеция). При длительном применении возможен некроз гепатоцитов и фиброз печени. Действие азатиоприна и метотрексата развивается медленно, улучшение может быть заметно не ранее, чем через 3–4 недели, для получения максимального эффекта необходим срок 4–6 мес., из–за чего иммуносупрессоры не могут применяться в острых ситуациях, они пригодны только для лечения хронических вялотекущих активных форм БК. Азатиоприн используется также для поддержания ремиссии, но способность метотрексата поддерживать длительную ремиссию считается сомнительной. Ремиссия, индуцированная метотрексатом сохраняется в течение одного года лишь у 40% больных [38]. Таким образом, применение иммуносупрессоров лимитировано, с одной стороны, побочными эффектами и медленно развивающимся действием, с другой стороны, они часто не дают желаемого результата. Практически, альтернативным методом лечения пациентов с резистентным течением БК является оперативное лечение. Инфликсимаб Новое направление в лечении больных БК, не ответивших на лечение стероидами (как системными, так и топическими), предусматривает избирательное подавление синтеза и активности фактора некроза опухоли (ФНО). С этой целью широко используется инфликсимаб, представляющий собой химерные моноклональные антитела к ФНО–a и состоящий на 25% из мышиного белка и на 75% из человеческого иммуноглобулина. Инфликсимаб используется за рубежом уже 8 лет, а в России прежде всего был зарегистрирован для лечения двух заболеваний, сходных по механизмам развития воспаления: БК и ревматоидного артрита (в настоящее время зарегистрирован также для лечения язвенного колита). Инфликсимаб рекомендуется при не осложненной стероидорезистентной форме БК и при свищевой форме, причем он активен как при среднетяжелом, так и при тяжелом течении заболевания [33,39,40]. В случае не осложненного течения для индукции ремиссии достаточно одной внутривенной инфузии из расчета 5 мг/кг/сут. При свищевой форме используют 3–кратное введение препарата с интервалом в 2 недели [41,42]. Ифликсимаб обладает пролонгированным действием. Успешные результаты получены у больных БК с развитием воспаления в области илеоанального резервуара и при перианальной локализации БК [43]. В контролируемых мультицентровых испытаниях частота ответа на инфликсимаб при стероидорезистентных формах БК колеблется в интервале 50–82%, частота достижения клинической ремиссии составляет 25–48% через 4 недели [44–46]. Длительное лечение инфликсимабом в течение 44 недель оказалось эффективным, хорошо переносимым методом купирования симптомов БК и достижения ремиссии у пациентов, не ответивших на традиционное лечение, а при поддерживающей терапии ремиссия сохранялась в течение 54 недель у 39% больных [47]. Примечательно, что у больных, получавших инфликсимаб для поддержания ремиссии, удалось полностью отказаться от применения кортикостероидов [47]. Инфликсимаб также оказался единственным на настоящий момент препаратом, позволившим достичь не только клинической, но и эндоскопической ремиссии при БК [47]. Действие инфликсимаба развивается быстро, уже через 2 недели можно наблюдать начало клинического эффекта. Продолжительность его действия – до 30 недель после однократной инфузии, однако через 8–12 недель концентрация антител в сыворотке снижается, поэтому у больных с наиболее упорной формой заболевания рекомендуются повторные инфузии каждые 8 недель для поддержания клинического ответа [45]. На экспертном совете по разработке новых стандартов применения инфликсимаба в странах ЕС и США в октябре 2005 г. (UC and CD: Treating to New Standards Expert Round Table. 19.10.2005) было предложено включить в показания к лечению не только стероидорефрактерные формы БК и язвенного колита (ЯК), но рекомендовать инфликсимаб как препарат первой линии при тяжелых формах этих заболеваний. В настоящее время в России инфликсимаб включен в список жизненноважных препаратов для лечения БК, включен с стандарты лечения БК (МЗ РФ) и зарегистрирован для лечения ЯК. Противорецидивная терапия Вопрос о поддерживающей терапии БК после достижения ремиссии остается не до конца решенным. Сульфасалазин, пероральный месалазин и преднизолон в низких дозах неэффективны для поддержания ремиссии. Будесонид в дозе 6 мг приводит к удлинению времени до наступления рецидива, однако не позволяет поддерживать ремиссию на протяжении года и не предотвращает рецидивы БК после операций [31]. Антибиотики не изучены в клинических исследованиях по этому показанию. В качестве средств поддерживающей терапии также эффективны азатиоприн, 6–меркаптопурин, но их применение лимитировано большим числом побочных эффектов. Таким образом, имеющиеся на настоящий момент данные не позволяют рекомендовать для поддерживающей терапии ни один препарат, как имеющий благоприятное соотношение эффективность/безопасность. В этой связи некоторые авторы рекомендуют больным с легкой и среднетяжелой БК только терапию, направленную на достижение ремиссии с последующим возобновлением ее при возникновении рецидива [11]. Заключение Настоящая работа преследовала две цели: во–первых, продемонстрировать недостаточную обоснованность традиционных подходов к лечению БК, прежде всего ее легких и среднетяжелых форм. Во–вторых, показать возможности новых лекарственных препаратов и их конкретную нишу в терапии БК. Исходя из вышесказанного выбор тактики лечения при разных формах БК с учетом тяжести, локализации и характера осложнений можно представить, как показано в таблице 1.
Литература 1. Адлер Г. Болезнь Крона и язвенный колит.– Гоэтар–Мед.– 2001.–500 с. 2. Белоусова Е.А. Язвенный колит и болезнь Крона.– Триада.–2002.– 128 с. 3. Морозова Н.А., Белоусова Е.А. Системные атоиммунные проявления воспалительных заболеваний кишечника (устное сообщение) 4. Белоусова Фармакотерапия и алгоритм лечения болезни Крона легкой и средней степени тяжести с позиций медицины, основанной на доказательствах.–Фарматека.– 2004.–№ 13.– с.8–18. 5. Anthonisen P, Barany F, Folkenborg O, et al. The clinical effect of salazosulphapyridine (Salazopyrin R) in Crohn’s disease. Scand J Gastroenterol 1974; 9: 549–54. 6. Van Hees PA, Van Lier HJ, Van Elteren PH, et al. Effect of sulphasalazine in patients with active Crohn’s disease: a controlled double–blind study. Gut 1981; 22: 404–9. 7. Summers RW, Switz DM, Sessions JT, et al. National Cooperative Crohn’s Disease Study: results of drug treatment. Gastroenterology 1979; 77: 847–69. 8. Malchow H, et al. European Cooperative Crohn’s Disease Study (ECCDS): results of drug treatment. Gastroenterology 1984; 86: 249–66. 9. Das KM, Eastwood MA, McManus JP, et al. The relationship between metabolites and the response to treatment in inpatients. Gut 1973; 14: 631–41. 10. Taffet SL, Das KM. Sulfasalazine. Adverse effects and desensitization. Dig Dis Sci 1983; 28: 833–42. 11. Sandborn W. J., Feagan B. G. Mild to Moderate Crohn’s Disease – Defining the Basis for a New Treatment Algorithm.Aliment Pharmacol Ther 2003;18:263–77. 12. Tremaine WJ, Schroeder KW, Harrison JM, et al. A randomized, double–blind, placebo–controlled trial of the oral mesalamine (5–ASA) preparation, Asacol, in the treatment of symptomatic Crohn’s colitis and ileocolitis. J Clin Gastroenterol 1994; 19: 278–82. 13. Gross V, Andus T, Fischbach W, et al. Comparison between high dose 5–aminosalicylic acid and 6–methylprednisolone in active Crohn’s ileocolitis. A multicenter randomized double–blind study. German 5–ASA Study Group. Z Gastroenterol 1995; 33: 581–4. 14. Scholmerich J, Jenss H, Hartmann F, the German 5–ASA Study Group. Oral 5–aminosalicylic acid versus 6–methylprednisolone in active Crohn’s disease. Can J Gastroenterol 1990;4:446–51. 15. Prantera C, Cottone M, Pallone F, et al. Mesalamine in the treatment of mild to moderate active Crohn’s ileitis: results of a randomized, multicenter trial. Gastroenterology 1999; 116: 521–6. 16. Thomsen OO, Cortot A, Jewell D, et al. A comparison of budesonide and mesalamine for active Crohn’s disease. International Budesonide–Mesalamine Study Group. N Engl J Med 1998; 339: 370–4. 17. Rijk MC, van Hogezand RA, van Lier HJ, et al. Sulphasalazine and prednisone compared with sulphasalazine for treating active Crohn disease. A double–blind, randomized, multicenter trial. Ann Intern Med 1991; 114: 445–50. 18. Martin F, Sutherland L, Beck IT, et al. Oral 5–ASA versus prednisone in short term treatment of Crohn’s disease: a multicentre controlled trial. Can J Gastroenterol 1990; 4: 452–7. 19. Yang YX, Lichtenstein GR. Corticosteroids in Crohn’s disease. Am J Gastroenterol 2002; 97: 803–23. 20. Gross V, Andus T, Caesar I, et al. Oral pH–modified release budesonide versus 6–methylprednisolone in active Crohn’s disease. German/Austrian Budesonide Study Group. Eur J Gastroenterol Hepatol 1996; 8: 905–9. 21. Rutgeerts P, Lofberg R, Malchow H, et al. A comparison of budesonide with prednisolone for active Crohn’s disease. N Engl J Med 1994; 331: 842–5. 22. Prantera C, Zannoni F, Scribano ML, et al. An antibiotic regimen for the treatment of active Crohn’s disease: a randomized, controlled clinical trial of metronidazole plus ciprofloxacin. Am J Gastroenterol 1996; 91: 328–32. 23. Bar–Meir, S, Chower, Y, Lavy, A, et al. Budesonide versus prednisone in the treatment of active Crohn’s disease. Gastroenterology 1998; 115:835. 24. Yang YX, Lichtenstein GR. Corticosteroids in Crohn’s disease. Am J Gastroenterol 2002; 97: 803–23. 25. Lyckegaard E, Hakansson K, Bengtsson B. Compassionate use of budesonide capsules (ENTOCORT EC) in patients with Crohn’s disease. Gastroenterology 2002; 122: T1665. 26. Lofberg, R, Rutgeerts, P, Malchow, H, et al. Budesonide prolongs time to relapse in ileal and ileocecal Crohn’s disease: A placebo controlled one year study. Gut 1996; 39:82. 27. Hellers, G, Cortot, A, Jewell, D, et al. Oral budesonide for prevention of postsurgical recurrence in Crohn’s disease. Gastroenterology 1999; 116:294. 28. Greenberg GR, Feagan BG, Martin F, et al. Oral budesonide for active Crohn’s disease. Canadian Inflammatory Bowel Disease Study Group. N Engl J Med 1994; 331: 836–41. 29. Rutgeerts P, Lofberg R, Malchow H, et al. A comparison of budesonide with prednisolone for active Crohn’s disease. N Engl J Med 1994; 331: 842–5. 30. Kane SV, Schoenfeld P, Sandborn WJ, et al. Systematic review: The effectiveness of budesonide therapy for Crohn’s disease. Aliment Pharmacol Ther 2002; 16: 1509–17. 31. Greenberg GR, Feagan BG, Martin F, et al. Oral budesonide for active Crohn’s disease. Canadian Inflammatory Bowel Disease Study Group. N Engl J Med 1994; 331: 836–41. 32. Elson C.O. The effects of immunosuppressive agents on cytokines. //Aliment. Pharmacol. Ther.– 1996.– v.10.–suppl.2.–p.100–105. 33. Sanborn W.J. Steroid–dependent Crohn’s disease. // Scand. J. Gastroenterol..– 2000.– v. 14.– (Suppl. C).– 17C. 34. Sands B.E Medical therapy of steroid–resistant Crohn’s disease. // Scand. J. Gastroenterol.– 2000.– v. 14.– (Suppl. C).– 33C. 35. Steinhart H. Steroid resistant and steroid dependent Crohn’s disease. // IBD, salicylates and other relevant therapies–Proceeding of the International IBD Symposium.– London.– 1999.– p.83–90 36. Lewis J.D., Sanford–Schwartz J., Lichtenstein G.R. Azatioprine for maintenance of remission in in Crohn’s disease: benefits outweigh the risk of lymphoma // Gastroenterology. –2000.– v. 118.– p.1018–1024 37. Lemann M., Zenjari T., Cosnes J., Mesnard B. Methotrexate in Crohn’s disease: long–term efficacy and toxity.– Am. J. Gastroenterol. 2000.– v. 95.– p.1730–1734 38. Feagan B.G., Fedorak R.N., Irvine E.J., Wild G. et all. A comparison of methotrexate with placebo for the maintenance of remission in Crohn’s disease // N. Engl. J. Med.– 2000.– v.342.– p. 1627–1632 39. Белоусова Е.А., Морозова Н.А., Никитина Н.В. Инфликсимаб (ремикейд) в лечении рефрактерных форм болезни Крона.–РМЖ.–2005.–т.7.–№1.–с.28–32 40. Sands B., Anderson F., Bernstein C. Infliximab Maintenance Therary for Fistulizung Crohn’s Disease.– N.Eng.J.Med. 2004.–v.350.– p.876–885. 41. Lichtensteyn G., Yan S., Bala M. et all. Infliximab Maintenance Treatment Reduces Hospitalizations, Surgeries, and Procedures in Fistulizing Crohn’s Disease. – Gastroenterology 2005.–v.128.–p.863–869 42. Present D.H., Rutgeerts P., Targan S., Hanauer S.B. et all. Infliximab for the treatment of fistulas in patiens with Crohn’s disease.– N. Engl. J. Med.– 1999.– v. 340.– 1398–1405 43. Ricart E., Panaccione R., Loftus E., Tremain W. Successful management of Crohn’s disease of the ileoanal pouch with infliximab // Gastroenterology.– 1999.– v. 117.– p. 429–432 44. Hanauer S., Feagan B., Lichtenstein G. et all. Maintenanse Infliximab for Crohn’s Disease: the ACCENT I Randomised Trial.– Lancet 2002.–v.359.–p.1541–1549. 45. Rutgeerts P. A Critical Assessment of new Therapies in Inflammatory Bovel Diseases. // J.Gastroenterol. Hepatol. 2002.–V.17.–Suppl..–S177 QR. 46. Targan S.R., Van Deventer S.J.H., et all. A short–term study of chimeric monoclonal antibody cA2 to tumor necrosis factor ? for Crohn’s disease.// N.Engl.J.Med. –1997.–v.337.–p.1029–1035 47. Rutgeerts P., D’Haens G., Targan S. et al. Efficacy and Safety of Retreatment with Anti–Tumor necrosis factor antibody (Infliximab) to maintain remission in Crohn’s disease // Gastroenterology, 1999.– V.117.–P.761–769.
Лечение
Базисные средства лечения ЯК включают 4 группы медикаментов: препараты 5-аминосалициловой кислоты (5-АСК), глюкокортикостероиды (ГКС), иммуносупрессоры и ингибиторы фактора некроза опухоли α. Первые две группы считаются препаратами первой линии [1–3]. В настоящей статье рассматриваются только вопросы, связанные с лечением ЯК аминосалицилатами.
Препараты 5-АСК (сульфасалазин и месалазин) используются в лечении легких и среднетяжелых форм ЯК для индукции ремиссии и как поддерживающая противорецидивная терапия в стадии ремиссии [1–3]. Основной механизм действия 5-АСК состоит в ингибировании циклооксигеназного и липооксигеназного путей метаболизма арахидоновой кислоты, подавлении синтеза активных медиаторов воспаления, главным образом лейкотриенов, и особенно лейкотриена В4 [7]. Кроме того, 5-АСК подавляет синтез провоспалительных цитокинов: интерлейкина-1, -2 и фактора некроза опухоли α, продукцию антител В-лимфоцитами и нейтрализует свободные кислородные радикалы [8]. Показано также, что 5-АСК способна подавлять транскрипционный ядерный фактор NF-κB и активность стимулирующих его субстанций [9].
Первым препаратом группы аминосалицилатов был сульфасалазин, синтезированный в 1946 г. Он представляет собой 5-АСК, соединенную азотистой связью с сульфаниламидом (сульфапиридином). Последний является инертной частью молекулы, препятствует всасыванию препарата в тощей кишке и фактически служит переносчиком 5-АСК в толстую кишку. Связь между 5-АСК и сульфапиридином расщепляется в подвздошной и толстой кишке под влиянием бактериальных ферментов (азоредуктаз), и освободившаяся 5-АСК оказывает свое противовоспалительное действие, блокируя синтез медиаторов в слизистой оболочке толстой кишки. Лишь 20–30 %-ная свободная 5-АСК всасывается из толстой кишки, поэтому ее системное действие весьма незначительно. Основная часть препарата остается в просвете кишки и кишечном эпителии в частично ацетилированной форме. Таким образом, высвободившаяся из сульфасалазина 5-АСК оказывает главным образом местное действие.
Сульфасалазин токсичен и вызывает широкий спектр побочных явлений, включая лейкопению с агранулоцитозом, токсико-аллергические кожные поражения, нарушение функции почек, панкреатит, бесплодие у мужчин и др. Эти реакции встречаются среди 15–20 % больных. Развитие побочных эффектов связано с сульфаниламидной частью препарата, поскольку сульфапиридин почти полностью всасывается из толстой кишки и метаболизируется в печени. Проблема токсичности, как известно, была решена созданием препаратов 5-АСК без сульфапиридина в молекуле (месалазин, олсалазин, балсалазид), не уступающих сульфасалазину по эффективности, но лишенных его побочных эффектов.
До сих пор наибольшее распространение как за рубежом, так и в России имели таблетированные препараты месалазина (Салофальк, Пентаса, Азакол, Мезакол), сходные по механизму действия и эффективности, но различающиеся характером энтеросолюбильного покрытия (L- или S-эудрагитное, акриловое или этилцеллюлозное), соответственно, местом и скоростью высвобождения 5-АСК в кишечнике [1, 10]. Существует четкая корреляция между внутрипросветной концентрацией 5-АСК и клинической эффективностью препарата, поэтому локализация поражения обязательно должна учитываться при назначении аминосалицилата. Растворение L-эудрагитного энтеросолюбильного (Салофальк) и S-эудрагитного покрытия (Азакол) зависит от рН в просвете кишки, и оно разрушается при его определенных значениях в терминальном отделе подвздошной кишки и проксимальных отделах толстой кишки, где и достигается максимальная лечебная концентрация 5-АСК. От этих форм месалазина отличается Пентаса, имеющая микрогранулированную структуру и этилцеллюлозное покрытие. Растворение этилцеллюлозной оболочки не зависит от уровня рН в кишечнике и начинается с двенадцатиперстной кишки, обеспечивая медленное, постепенное и равномерное освобождение 5-АСК на всем протяжении тонкой кишки и в проксимальных отделах толстой кишки. Все указанные препараты с успехом используются для лечения распространенного легкого и среднетяжелого ЯК, создавая в просвете кишки эффективную концентрацию 5-АСК. Однако таблетированные препараты, к сожалению, малоэффективны при лечении левостороннего, тем более дистального, ЯК (проктита), поскольку концентрация активного вещества в толстой кишке снижается в каудальном направлении, в результате чего в нисходящую и сигмовидную кишку попадает минимальная часть 5-АСК, а в прямой кишке ее практически нет. Для лечения ЯК с поражением прямой кишки и левостороннего колита существуют лекарственные формы месалазина в виде клизм, пен и свечей. Часто для повышения эффективности терапии используют комбинацию перорального приема месалазина и его ректального введения. Такое лечение достаточно дорого и технически неудобно для пациентов, что снижает приверженность лечению и терапевтический эффект, повышая риск рецидива.
Ниже приведены традиционные схемы лечения дистального и распространенного ЯК легкого и среднетяжелого течений. Эти схемы разработаны Российской группой по изучению ВЗК на основе Европейского консенсуса [11].
Лечение проктита легкого и среднетяжелого течения
1-я линия терапии:
• суппозитории с месалазином 1–2 г/сут. Начало терапевтического ответа в течение 2 недель. Длительность индукционного курса – 6–8 недель.
В отсутствие эффекта: 2-я линия терапии:
• комбинация месалазина в суппозиториях 1 г и месалазина в таблетках 2–3 г или
• комбинация месалазина в суппозиториях 1 г и ректальных форм ГКС (суппозитории с преднизолоном 5–10 мг 1–2 раза в сутки).
При достижении клинико-эндоскопической ремиссии поддерживающая терапия:
• месалазин местно (суппозитории) 1–2 г 3 раза в неделю в виде монотерапии или в комбинации с таблетками месалазина 1,5–2,0 г – не менее 2 лет.
Лечение левостороннего и тотального ЯК легкого течения
• 1-я атака или рецидив: месалазин в таблетках внутрь 3 г/сут (или сульфасалазин 4 г/сут) в комбинации с месалазином в клизмах 2–4 г/сут (в зависимости от эндоскопической активности). Начало терапевтического ответа – до 2 недель. Длительность индукционного курса – 6–8 недель.
В отсутствие эффекта добавить ректальные формы ГКС (микроклизмы с суспензией гидрокортизона 125–250 мг/сут).
При достижении клинико-эндоскопической ремиссии поддерживающая терапия:
• месалазин в таблетках 1,5 г/сут внутрь + месалазин в клизмах 2 г 2 раза в неделю;
• допустимо назначение сульфасалазина 3 г вместо месалазина.
Лечение левостороннего и тотального ЯК средней тяжести
Первая атака или рецидив: месалазин в таблетках 4–5 г/сут в комбинации с месалазином в клизмах 2–4 г/сут (в зависимости от эндоскопической активности).
При достижении ремиссии поддерживающая терапия:
• месалазин в таблетках 1,5 г/сут внутрь + месалазин в клизмах 2 г 2 раза в неделю;
• допустимо назначение сульфасалазина 3 г/сут вместо месалазина.
Лечение язвенного колита легкой и средней степени тяжести
Выступление профессора Шифрина О.С. в рамках II Международного Интернет Конгресса специалистов по внутренним болезням.
Профессор Шифрин О.С.: – Добрый день, дорогие коллеги. Я сделаю сегодня доклад на тему воспалительных заболеваний кишечника.
(00:13) Заставка: Препараты 5-аминосалициловой кислоты в лечении неспецифического язвенного колита.
Профессор Шифрин О.С.: – И посвящен он будет лечению язвенного колита: как оптимально использовать препараты 5-аминосалициловой кислоты в лечении этого тяжелого, непростого в диагностическом и в лечебном плане заболевания. Какие же цели преследует клиницист, берясь за сложное дело курации пациента с язвенным колитом? Прежде всего он должен достичь клинической ремиссии, но этого мало. Он должен стараться достичь клинической ремиссии без использования стероидных препаратов. Поддержание клинической ремиссии должно быть длительным. Очень важным залогом успеха длительного поддержания клинической ремиссии является достижение эндоскопической ремиссии, а в перспективе мы будем стремиться к достижению и гистологической ремиссии. Как известно, в лечении воспалительных заболеваний кишечника используется относительно небольшое количество препаратов. Есть тенденция, что ряд препаратов, которые ранее использовались в лечении только болезни Крона, сейчас с успехом применяется и при язвенном колите. Это относится и к азатиоприну, и к антицитокиновым препаратам, и к некоторым антибиотикам, которые также используются при токсических формах язвенного колита.
К лечению пациентов с язвенным колитом и болезнью Крона существует два подхода: или мы назначаем последовательно препараты от наименее сильного эффекта и, соответственно, от наиболее слабых побочных эффектов, к более сильным препаратам, которые дают большее количество побочных эффектов. Такой подход представляется наиболее закономерным. Другой подход – когда уже на ранних этапах, и это особенно касается болезни Крона, назначаются антицитокиновые препараты. Это препараты, которые не меняют естественное течение заболевания, но в то же время грозят возникновением многих тяжелых побочных эффектов. Следует вспомнить, что препараты 5-аминосалициловой кислоты первой линии лечения язвенного колита обладают наибольшей степенью доказательности эффективности своего действия. Уже к 2000 году на основании большого количества контролированных рандомизированных исследований было показано, что эти препараты в эффективности своего действия подкреплены высшим уровнем доказательности – 1А.
Первым препаратом 5-аминосалициловой кислоты, который стал использоваться при язвенном колите, являлся «Сульфасалазин», состоящий из двух частей: из 5-аминосалициловой кислоты соединенной с сульфапиридином, который используется в качестве носителя 5-аминосалициловой кислоты под действием азоредуктаз, вырабатываемых бактериями толстой кишки, молекулы препарата распадаются на свои исходные части и проявляют фармакологическое действие. Я остановлюсь несколько позже на многочисленных побочных эффектах данного препарата. И к назначению «Сульфасалазина» сейчас в XXI веке следует относиться с большой осторожностью.
Итак, вспомним рекомендации Европейского общества по изучению колитов и болезни Крона в аспекте использования препаратов 5-аминосалициловой кислоты при язвенном колите. При распространенной форме колита, при тотальном колите, но с умеренной активностью, показано назначение в качестве базисной терапии обострений не менее 2 грамм месалазина в день. Это подкрепляется высоким уровнем доказательности 1А. И что очень важно, при тотальном колите также следует использовать местные топические препараты месалазина – это резко повышает эффективность лечения.
При левостороннем колите с умеренной активностью также показана комбинация перорального месалазина и препаратов местного действия. При этом достоверно повышается эффективность лечения с уровнем доказательности 1В. При проктите со слабой умеренной активностью возможно инициальное назначение суппозиториев с месалазином с высоким уровнем доказательности. Но при отсутствии эффекта данная местная терапия должна подкрепляться назначением и пероральных форм препарата. Поддерживающая терапия препаратами 5-аминосалициловой кислоты рекомендована всем пациентам, у которых нам удалось добиться клинической и эндоскопической ремиссии после применения в качестве терапии обострения препаратов 5-аминосалициловой кислоты.
Пероральная терапия составляет первую линию поддерживающей терапии и должна использоваться при тотальном колите обязательно с применением пероральных форм. При проктите или левостороннем колите возможно применение для поддержания ремиссии (не для индукции ремиссии) использование только местных форм месалазина. Если не удается достичь успешного поддержания ремиссии только местными формами, последние следует комбинировать с таблетками. И не нужно забывать минимальные дозы, которые необходимы для эффективного поддержания ремиссии. Они должны быть не менее 1 грамма. В то же время топические препараты месалазина, в частности суппозитории, должны назначаться не реже трех раз в неделю при дистальном колите. Безусловно, рекомендации – это рекомендации. И врач-клиницист, имеющий опыт лечения подобных больных, безусловно, может самостоятельно решать многие вопросы о назначении препарата. Гайдлайны ЕССО вовсе не требуют скрупулезного их соблюдения. Прежде всего, решает реальная клиническая картина.
Так, согласно опыту нашей клиники, очень важно рассматривать клинические особенности дебюта заболевания. Они тоже в какой-то мере предрасполагают к поддержанию ремиссии в дальнейшем тем или иным препаратом. Так при чисто диарейном варианте дебюта (не диарейно-гематохезийном) язвенного колита препараты 5-аминосалициловой кислоты также оказались наиболее показаны. Препараты 5-аминосалициловой кислоты важны еще в отношении профилактики развития колоректального рака, к сожалению, нередкого осложнения язвенного колита – это решающая линия профилактики колоректального рака. Скрининг, генетические исследования пока еще окончательно не разработаны. Поэтому придается особое значение длительному назначению препаратов 5-аминосалициловой кислоты, для того чтобы предупредить развитие колоректального рака у наших пациентов.
Первым препаратом 5-аминосалициловой кислоты был «Сульфасалазин». Он показал эффект, но он показал и высокую частоту различных побочных эффектов при его применении. Согласно нашим данным у 40% больных язвенным колитом, которые принимали «Сульфасалазин», возникали те или иные побочные эффекты. После «Сульфасалазина» были разработаны так называемые диазосоединения 5-аминосалициловой кислоты: «Олсалазин», в котором две молекулы 5-аминосалициловой кислоты соединены диазосвязью и «Балсалазид», в котором 5-аминосалициловой кислота соединена с остатком 4-амино-бензоил-аланина. Но, к сожалению, данные препараты показали примерно такую же частоту побочных эффектов, как и «Сульфасалазин».
Позже появились высвобождающие системы, в начале – преимущественно рН-зависимые. То есть высвобождение месалазина, заключенного в таблетке, зависело, прежде всего, от рН кишечного содержимого. Недостатком данной группы препаратов является то, что, поскольку вследствие воспаления стенки кишки меняется нормальные показатели кишечного рН, нередко данные препараты не работают. Положение изменилось после разработки препаратов месалазина, а именно микрогранул месалазина, покрытых этилцеллюлозной оболочкой, высвобождение которых зависит от времени нахождения субстанции в кишечнике.
Высвобождение препарата «Пентаса», который представляет данную форму, начинается уже в двенадцатиперстной кишке. То есть этот препарат хорош для лечения не только язвенного колита, но очень подходит для лечения болезни Крона. Препарат равномерно распределяется в тонкой и толстой кишке. Что очень важно – он не задерживается в желудке, что позволяет избежать резкого повышения концентрации в крови. Благодаря постепенному высвобождению, препарат достигает и дистальных отделов кишечника. И скорость высвобождения препарата остается постоянной в широких пределах рН внутрикишечного содержимого. То есть в этом плане препарат очень выигрышный. Распределение препарата многократно изучалось различными методами, в частности методом сцинтиграфии. И здесь показано, что месалазин высвобождается как в тонкой, так и в толстой кишке. И зона применения данного препарата – и болезнь Крона, и язвенный колит. Причем при этих заболеваниях применяются различные формы. При изучении распределения препарата мы отметили, что распределение «Пентаса» было очень равномерным и относилось как к начальным отделам тонкой кишки, начиная с двенадцатиперстной, так и к дистальным отделам толстой кишки.
Позвольте рассказать о случае из нашей клинической практики. В нашу клинику обратилась пациентка 35 лет с жалобами: жидкий стул с примесью слизи, иногда – крови, до 5-7 раз в день, метеоризм, слабость, похудание за год почти на 7 кг. Больна в течение двух лет. Молодой женщине довольно быстро был поставлен диагноз язвенного колита, к сожалению, это не всегда так. Как и при болезни Крона, мы имеем большие проблемы в стране с ранней постановкой данных заболеваний. Недавно в нашу клинику поступил пациент с болезнью Крона, которому диагноз не был поставлен в течение 24 лет его наблюдения при типичной клинической картине. То есть безусловно, мы должны глубже изучать клинику этих заболеваний.
Итак, у пациентки появилась гематохезия, диарея, и она стала худеть. Поставлен правильный диагноз – язвенный колит. Врачи пошли механически по пути увеличения дозы «Сульфасалазина». Вначале она принимала 2 грамма, потом стала принимать 3 грамма и, наконец, 4 – эффекта не было. У этой пациентки дело обошлось без побочных эффектов, к счастью. Но клинический эффект назначением «Сульфасалазина» достигнут не был. В нашей клинике поставили диагноз «неспецифический язвенный колит, тотальная форма, активность по Truelove I», и он был подтвержден. Мы широко применяем лучевые методы исследования для подтверждения диагноза, в частности, компьютерную томографию. Метод компьютерной колонографии позволяет уточнить поражение, на каком этапе поражена кишка, выраженность поражения, толщину кишечной стенки, оценить клетчатку, примыкающую к кишечнику, наличие лимфоузлов и так далее.
Мы назначили пациентке «Пентасу» – 3 г/сут. Как известно, данный препарат можно применять один раз в день – это повышает комплаенс пациента. Естественно, принимать лекарства человеку легче однократно, чем три раза в день. И, соответственно, пациенты с большей охотой будут выполнять рекомендации врача. Согласно совершенным рекомендациям ECCO, терапию пероральным препаратом – таблетками «Пентасы», необходимо было дополнить новой формой «Пентасы», которая предложена сейчас, и которая уже есть в нашем распоряжении – суппозиториями, свечами «Пентасы», которые содержат 1 грамм месалазина. Свечи «Пентасы» могут использоваться однократно, а не два раза в день, как ранее предлагалось их использовать. И с применением местной и пероральной терапии нам довольно быстро удалось достичь улучшения клинической картины.
Но я уже говорил, что нашей целью является достижение не только клинической ремиссии, а достижение и эндоскопической ремиссии. Для оценки динамики состояния в этом плане мы используем клинико-эндоскопический индекс Мейо, который объединяет как клинические показатели, так и эндоскопические показатели. После лечения таблетками и суппозиториями «Пентасы» у пациентки нормализовалась частота стула, исчезли ректальные кровотечения, гематохезия и полностью нормализовалась эндоскопическая картина.
Что мы имеем в итоге: активность заболевания 0 баллов, мы достигли клинико-эндоскопической ремиссии. Нам следует прекратить терапию? Нет. И согласно нашему опыту и рекомендациям ЕССО, рекомендациям Американской гастроэнтерологической ассоциации поддерживающую терапию следует продолжать, но дозу препарата можно уменьшить. Таблетки «Пентасы» мы постепенно уменьшили с 3 грамм приема препарата в сутки до 1 грамма. Суппозитории «Пентасы» мы предложили пациентке использовать с кратностью три раза в неделю. Какой можно сделать вывод? Препараты 5-аминосалициловой кислоты остаются первой линией лечения неспецифического язвенного колита. К счастью, в распоряжении врачей появляются новые все более эффективные препараты, содержащие месалазин.
(17:25) Заставка.
Профессор Шифрин О.С.: – Поступило несколько вопросов: «Какой грозный побочный эффект от применения месалазина?»
Надо сказать, что это довольно безопасный препарат. Если сравнивать его с препаратами иных групп – это, пожалуй, самый безопасный препарат. Он может давать цефалгию, может давать абдоминалгию, может давать расстройство стула. Иногда он вызывает такие панкреотоксические реакции, но это бывает нечасто. И я повторяю, этот препарат наиболее безопасен среди всех иных препаратах, применяемых при лечении воспалительных заболеваний кишечника.
Вопрос: «Нужно ли принимать пробиотики при терапии язвенного колита?»
Это спорный вопрос, который обсуждается. Считается, что штамм Escherichia coli 1917 обладает определенным эффектом, и он даже включен в рекомендации. Но тем не менее обсуждается вопрос об использовании других штаммов микроорганизмов. В частности, при болезни Крона – Saccharomyces boulardii и так далее. Этот вопрос требует дальнейшей разработки, но сам по себе очень интересный.