ГАСТРЭКТОМИЯ
(греч. gaster желудок + греч. ektome иссечение, удаление; син.
экстирпация желудка
) — операция полного удаления желудка. Один из методов хирургического лечения злокачественных опухолей желудка, значительно реже применяется при некоторых других заболеваниях (полипоз, высоко расположенная язва, синдром Золлингера — Эллисона).
Первую успешную Г. произвел в 1897 г. швейц. хирург Шлаттер (С. Schlatter). Операция была закончена наложением пищеводно-тонкокишечного анастомоза. В 1898 г. Бригхем и Мак-Донелд (С. В. Brigham, R. М. McDonald) сообщили об успешной Г. с пищеводно-дуоденальным анастомозом. В России первую экстирпацию желудка при раке с благоприятным исходом произвел
В. М. Зыков в 1911 г. Техническая сложность операции была причиной очень медленного ее внедрения в хирургическую практику. Так, Н. П. Тринклер (1911) приводит сводную статистику 25 случаев Г., из которых только 13 были успешными. К 1933 г. в мировой литературе были опубликованы сведения о 165 операциях, выполненных 55 хирургами (летальность 63%). В 40-х и 50-х годах 20 в. была детально разработана техника операции, предложены многочисленные варианты. Г. получила широкое распространение и стала в крупных хирургических учреждениях обычным оперативным вмешательством.
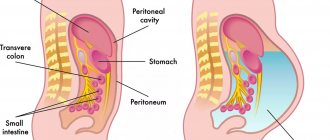
Рис 1. Схема восстановления непрерывности пищеварительного тракта после гастрэктомии: а — эзофагоеюноанастомоз; б — эзофагодуоденостомия; 1 — пищевод; 2 — диафрагма; 3 — тощая кишка; 4 — двенадцатиперстная кишка.
Наиболее распространенным способом реконструкции при Г. является простейший — эзофагоеюноанастомоз с брауновским соустьем (рис. 1,а). Другие модификации Г. используются реже, по определенным показаниям.
Предложен ряд приемов, обеспечивающих создание искусственного резервуара на месте удаленного желудка с помощью боковых анастомозов. С целью предупреждения рефлюкса кишечного содержимого по приводящей петле применяли анастомозы по Ру. Большое внимание было уделено разработке модификаций оперативного вмешательства, позволяющих после Г. сохранять пассаж пищи через двенадцатиперстную кишку (эзофагодуоденостомия — рис. 1,6). Однако из-за анатомических особенностей пищевода и двенадцатиперстной кишки эта операция может быть применена лишь в ограниченном числе случаев.
После разработки методов кишечной пластики при операциях на желудке стали применять замещение удаленного Желудка участком тонкой кишки, причем восстановление пассажа через двенадцатиперстную кишку часто сочетали с одновременным созданием объемистых резервуаров. Ряд технических предложений [операции А. Е. Захарова, А. М. Бетанели, Пота (E. J. Poth)] был вызван стремлением замедлить пассаж через трансплантируемый на место желудка тонкокишечный сегмент; для этого же Ниссен, Шперлинг (R. Nissen, E. Sperling) и др. предложили оставлять неудаленным привратник. Восстановление пассажа через двенадцатиперстную кишку в некоторых модификациях Г. достигается трансплантацией сегментов толстой кишки. Многие из перечисленных оперативных вмешательств отличаются большой технической сложностью и травматичность»), что удерживает хирургов от широкого их применения онкологическим больным.
Показания
Г. производят при раке тела желудка или верхней его трети, а также при опухолях, распространяющихся на большую часть органа. При ограниченных опухолях кардиального отдела желудка в ряде случаев обоснованной является резекция проксимального отдела — операция, имеющая функциональные преимущества перед Г. Подавляющее большинство современных хирургов отрицательно относится к идее производить Г. по принципиальным показаниям, т. е. при любой локализации рака желудка, как это в свое время предлагали К. П. Сапожков (1946), Скотт и Лонгмайер (H. Scott, W, Longmire, 1949), Лахей (F. Lahey, 1950) и ДР.
Окончательное решение о возможности радикального удаления опухоли желудка и об объеме операции хирург принимает лишь в процессе самого вмешательства, когда уточняются пределы распространения и характер опухолевого роста (экзофитный, эндофитный), наличие метастазов в лимф, узлах. Каждый хирург, оперирующий на желудке по поводу злокачественных опухолей, всегда должен быть готов к Г.
Большое практическое значение Имеет вопрос о показаниях к так наз. комбинированной Г., когда вместе с желудком удаляется частично или полностью орган, на который переходит опухоль (поперечная ободочная кишка, селезенка, поджелудочная железа, печень). Решение этого вопроса зависит от данных Клинико-рентгенологического исследования, а также и от операционных находок. Опыт показывает, что комбинированные операции обоснованы только в тех случаях, когда прорастание опухоли желудка в смежные органы носит ограниченный характер или имеет место ограниченное увеличение лимф, узлов, напр, в воротах селезенки. Подобные операции становятся бесперспективными при множественных метастазах.
Противопоказания
складываются из противопоказаний онкологического характера (распространение опухоли на близлежащие органы, метастазирование за пределы регионарных лимф, бассейнов, отдаленные метастазы) и противопоказаний общего плана (высокая степень операционного риска у пожилых больных с сопутствующими заболеваниями) .
Предоперационная подготовка
должна проводиться с учетом конкретных особенностей, выявленных в результате клинического исследования, и ограничиваться, по возможности, короткими сроками (7—10 дней). Вопрос о рациональной предоперационной подготовке должен решаться хирургом совместно с анестезиологом, терапевтом и другими специалистами. Основные элементы предоперационной подготовки направлены на восстановление нарушенного биол, равновесия и коррекцию гомеостаза: полноценное питание, обеспечивающее энергетический, азотный и витаминный баланс; возмещение дефицита воды и электролитов внутривенными инфузиями жидкостей; коррекция нарушения объема циркулирующей крови переливанием крови, эритроцитарной массы, белковых кровезаменителей; лечение нарушений сердечно-сосудистой системы; нормализация нарушений функции внешнего дыхания (дыхательная гимнастика, санация дыхательных путей). Антибиотики в предоперационном периоде назначаются по специальным показаниям (прорастание опухоли в поперечную ободочную кишку, сопутствующие воспалительные заболевания легких).
Обезболивание
при Г. общее. Многокомпонентный эндотрахеальный наркоз с применением мышечных релаксантов и управляемого дыхания позволяет спокойно провести операцию и создает оптимальные условия для эффективных мероприятий, предупреждающих нарушения гемодинамики и газообмена.
Возможные осложнения после удаления желудка
Гастрэктомия относится к очень большим операциям, в связи с чем существует определенное количество рисков и осложнений:
- травма соседних с желудком органов, например, печени, поджелудочной железы и тонкого кишечника;
- кровотечения, вызванные повреждением кровеносных сосудов;
- повреждение нервов, в результате чего может нарушиться функции кишечника;
- инфекции и абсцессы;
- недостаточная герметичность швов в области кишечника;
- чрезмерное рубцевание области операции с риском развития непроходимости кишечника;
- воспаление поджелудочной железы и желчных протоков;
- воспаление пищевода (изжога), вызванное попаданием желчи в пищевод;
- нарушение заживления ран;
- грыжи рубца на коже живота;
- стеноз анастомоза (сужение соединительного шва);
- пептическая язва анастомоза;
- пневмония и тромбоэмболия;
- железодефицитная анемия.
Учитывая все возможные последствия удаления желудка при раке, следует позаботиться о соответствующем лечении после гастрэктомии. Все вышеуказанные осложнения могут быть причиной необходимости проведения дальнейших операций. На ранних стадиях у многих пациентов развивается ранний или поздний демпинг-синдром. В связи с тем, что еда непривычно быстро проходит через пищеварительный тракт, после приема пищи у пациента могут возникнуть через полчаса (ранний демпинг-синдром) или через 2-3 часа (поздний демпинг-синдром) тошнота, головокружение и слабость, и вплоть до коллапса системы кровообращения. Все эти факторы в обязательном порядке учитываются в схеме лечения, и, после удаления желудка, для каждого пациента клиники Nordwest составляется своя программа реабилитации и восстановления.
Техника операции
Гастрэктомией в строгом смысле этого слова считают такую операцию, когда в удаленном препарате, помимо желудка, обнаруживают элементы пищеводного и кишечного эпителия. Операция по поводу рака включает В себя, кроме удаления желудка, удаление всего его связочного аппарата и регионарных лимф, узлов.
Правильный выбор операционного доступа при Г. играет существенную роль, в значительной мере определяя радикальность операции, и обеспечивает условия для надежного наложения анастомозов. В каждом конкретном случае доступ избирают с учетом локализации и характера роста опухоли, а также возраста и общего состояния больного.
Чрезбрюшинная Г.
— наиболее частая операция при распространенном раке желудка. Этот доступ менее травматичен, чем трансплевральный или комбинированный, и, следовательно, более показан пожилым и ослабленным больным. Наилучший доступ к верхним отделам желудка обеспечивает срединная лапаротомия (см.), к-рая при необходимости может быть дополнена резекцией мечевидного отростка грудины и частичной стернотомией. При субкардиальной локализации рака с ограниченным распространением на абдоминальный отдел пищевода чрезбрюшинную Г. производят, прибегая к диафрагмокруротомии по А. Г. Савиных.
Рис. 2. Схематическое изображение границ гастрэктомии (черная линия; пунктиром обозначена граница пересечения большого сальника). Рис. 3. Схема мобилизации желудка по большой кривизне и подготовки к пересечению желудочно-селезеночной связки: 1 — диафрагма; 2 — пищевод; 3 — желудочноселезеночная связка (пережата); 4 — поджелудочная железа; 5 — большой сальник; 6 — желудок. Рис. 4. Схема наложения пищеводно-кишечного анастомоза двухрядным швом: 1 — наложение первого ряда швов; 2 — наложение второго ряда швов.
Основные этапы чрезбрюшинной Г. с наложением эзофагоеюноанастомоза следующие. После ревизии брюшной полости, к-рая включает осмотр задней стенки желудка, желудочно-поджелудочной связки, ворот селезенки, при возможности выполнения радикальной операции приступают к мобилизации желудка (границы представлены на рисунке 2). Большой сальник отделяют от поперечной ободочной кишки, освобождают желудок по большой кривизне по ходу желудочно-селезеночной связки и в области дна (рис. 3). Дистальную часть желудка мобилизуют перевязкой правых желудочных сосудов, после чего перевязывают и пересекают левую желудочную артерию в ее начальном отделе. Желудок отсекают от двенадцатиперстной кишки, культю последней ушивают. Далее, обеспечив хорошую экспозицию поддиафрагмального пространства, пересекают оба блуждающих нерва, абдоминальный отдел пищевода, удаляют желудок и приступают к наложению пищеводно-кишечного анастомоза (рис. 4).
Рис. 5. Схема наложения эзофагоеюноанастомоза аппаратом ПКС-25: а и б — этапы операции; в — операция завершена; 1 — пищевод; 2 — сшивающий аппарат ПКС-25; 3 — тощая кишка; 4 — селезенка; 5 — поперечная ободочная кишка; 6 — поджелудочная железа.
Существует большое число различных модификаций наложения анастомоза тощей кишки с пищеводом — наиболее ответственного этапа операции. Преимущество остается на стороне технически наиболее простых и надежных методов, к к-рым следует отнести так наз. горизонтальные пищеводно-кишечные анастомозы, формируемые двухрядными швами. Широкое распространение получил метод наложения пищеводно-кишечного анастомоза с помощью сшивающего аппарата ПКС-25 (рис. 5).
Чресплевральная Г.
показана при раке верхнего отдела желудка, переходящем на пищевод, или если имеются признаки прорастания опухоли в диафрагму. Разрез производят по VII или VIII межреберья) в положении больного на правом боку (см. Торакотомия). Целесообразно продолжить разрез на переднюю брюшную стенку по направлению к пупку с пересечением реберной дуги. После ревизии плевральной полости производят диафрагмотомию и операцию продолжают в брюшной полости. Чресплевральный доступ обеспечивает большие возможности для тщательной ревизии органов верхнего этажа брюшной и грудной полостей и позволяет более надежно наложить пищеводно-кишечный анастомоз. В нашей стране первая Г, чресплевральным доступом была произведена Б. В. Петровским в 1946 г.
Г. абдомино-торакальным доступом
показана при раке верхнего отдела желудка, когда имеются сомнения в операбельности. Положение больного — на правом боку с наклоном тела на 45° к операционному столу. Через абдоминальную часть разреза осуществляют ревизию брюшной полости, после чего в случае неоперабельности брюшную стенку ушивают, и операция на этом заканчивается. Если радикальная операция оказывается выполнимой, разрез продолжают по VIII межреберью и вскрывают плевральную полость. Комбинированный двухмоментный доступ (срединная лапаротомия и последующая торакотомия), требующий проведения операции в два этапа и изменения положения больного на операционном столе, не имеет каких-либо преимуществ.
При Г., выполняемой чресплевральным или абдомино-торакальным доступом, мобилизацию желудка осуществляют в направлении сверху вниз, т. е. начинают с мобилизации пищевода и проксимального отдела желудка. Основные детали техники операции остаются теми же.
Послеоперационный период
Лечение после операции должно строиться с соблюдением принципов индивидуализации. Основные мероприятия: 1) адекватное послеоперационное обезболивание, обеспечивающее профилактику болевого шока, достаточную легочную вентиляцию и восстановление нормальных функций организма (обезболивающие средства, длительная перидуральная анестезия, леч. наркоз); 2) лечение дыхательной недостаточности и профилактика легочных осложнений (оксигенотерапия, дыхательная гимнастика, средства, улучшающие дренирование бронхиального дерева, антибиотики и сульфаниламиды); 3) профилактика и лечение сердечно-сосудистых нарушений (сердечные гликозиды, эуфиллин, по показаниям — глюкокортикоиды); 4) профилактика тромбоэмболических осложнений (ранняя двигательная активность больного, леч. физкультура и массаж, назначение антикоагулянтов под контролем коагулограммы); 5) коррекция водно-электролитных нарушений и полноценное парентеральное питание (внутривенное вливание физиол, раствора, полиионных растворов, содержащих калий, концентрированных растворов глюкозы, переливание препаратов, содержащих белки, аминокислоты, эмульгированные жиры, переливание крови, витаминотерапия).
Питание больных через рот обычно начинают с 5-го дня после Г., причем в первый день разрешают воду или чай, в последующие дни жидкую пищу (кисель, соки, сырые яйца, сливочное масло, бульон, жидкая каша и др.); питание дробное, небольшими порциями до 6 раз в сутки, К 14—15-му дню больных переводят на стол № 1 (см. Лечебное питание).
Послеоперационные осложнения
: недостаточность швов пищеводно-кишечного со устья (наиболее частое осложнение), пневмония, тромбоэмболия легочной артерии.
Питание после удаления желудка
Многих пациентов и их родственников волнует вопрос, что можно есть после удаления желудка, нужно ли соблюдать диету. Конечно, гастрэктомия накладывает свои ограничения относительно питания, ведь полноценный процесс переваривания пищи теперь становится невозможным. Несмотря на это, с течением времени пациент имеет возможность употреблять все категории продуктов, соблюдать полноценность рациона с точки зрения употребления белков, жиров, необходимых витаминов. Принципиальное изменение в этом вопросе касается способа приготовления пищи и количества употребляемых продуктов за одну трапезу. Преимущество следует отдавать приготовлению на пару, тушению и варке. Одна порция должна быть небольшой, питание в течение дня — дробное. Диета после гастрэктомии предполагает отказ от очень жирных, жареных продуктов, сладкого.
Переедание может вызвать неприятные ощущения и боль, поэтому за размером порций важно следить также внимательно, как за тем, что подается во время еды. Первое время после того, как была проведена гастрэктомия пациенты питаются посредством капельниц: питательные вещества подаются через кровь.
Результаты операции
Полное удаление желудка часто приводит к значительным нарушениям в организме оперированных. Пациенты, практически излеченные от рака, в отдаленном послеоперационном периоде предъявляют ряд жалоб, свидетельствующих о том, что организм не всегда обеспечивает необходимый уровень компенсации утраченных функций. Многие нарушения имеют выраженную клиническую картину (расстройства питания, агастральная анемия, рефлюкс-эзофагит, демпинг-синдром и др.) и могут быть объединены понятием «синдром после гастрэктомии» (см. Постгастрорезекционный синдром). Больные, перенесшие Г., нуждаются в постоянном врачебном наблюдении и лечении.
Летальность после гастрэктомии составляет в среднем ок. 7% с колебаниями (от 3,3 до 26,1%, по данным разных авторов). Отдаленные результаты операции различны в зависимости от стадии, характера опухоли (гистол, строение, тип роста) и ее локализации в желудке (по данным многих авторов, 5-летняя переживаемость составляет ок. 30%).
Библиография:
Бабичев С. И. Тотальная гастрэктомия, М., 1963; Березов Ю. Е., Рак кардиального отдела желудка, М., 1960; Квашнин Ю. К. и Панцырев Ю. М. Последствия гастрэктомии, М., 1967; Маят В. С. и др. Резекция желудка и гастрэктомия, М., 1975; Пете р с о н Б, Е. Рак проксимального отдела желудка, М., 1972; Петровский Б. В. Хирургическое лечение рака пищевода и кардии, М., 1950; Ц а ц а н и-ди К. Н. и Богдан о в А. В. Пищеводногкишечные и пищеводно-желудочные анастомозы, М., 1969; Юдин С. С. Этюды желудочной хирургии, М., 1955; McNeer G. a. Pack G. Т. Neoplasms of the stomach, Philadelphia, 1967; Schlatter C. t)ber Ernahrung und Verdauung nach vollstandiger Entfernung des Magen-Osophagoenterostomie bein Menschen, Bruns’ Beitr. klin. Chir., Bd 19, S. 757, 1897
Ю. М. Панцырев.
Ход оерации
При операции LCRYGB размер желудка уменьшается с помощью хирургического скобочного шва. Эта бариатрическая процедура разрезает желудок таким образом, что остается резервуар размером с грецкий орех. Затем измеряется так называемая «билиопанкреатическое ответвление» (50 см). Дистальные кишечные петли соединены с резервуаром (гастроэнтероанастомоз ГЭА). Это приводит к транспортировке пищи из желудка непосредственно в тонкую кишку. Соединение тонкой кишки (еюно-еюнальноый анастомоз ЕЕА) образуется на расстоянии 120-150 см от ГЭА.