Питание всухомятку, перекусы на бегу – это стало уже привычным в современном мире. К сожалению, с каждым годом неуклонно увеличивается и число больных гастритами, а также язвой желудка и 12-перстной кишки. Сегодня существует множество лекарственных средств для терапии этих заболеваний. Один из препаратов – Де-Нол – эффективное и безопасное, которое поможет справиться с гастритом и язвой.
Фармакологическое действие
Препарат оказывает вяжущее действие, благодаря чему на поверхности слизистой желудка и 12-перстной кишки в месте поражения образуется пленка. Таким образом, пострадавшие области оказываются защищенными от агрессивного действия желудочного сока, а значит, прогрессирование процесса приостанавливается. Наличие защитной пленки способствует рубцеванию язвенных поражений.
Де-Нол губителен для Helicobacter pylori, которая является основной виновницей образования язв на слизистой желудочно-кишечного тракта. Ни один штамм этой болезнетворной бактерии не имеет резистентности к данному лекарственному средству.
Кроме того, прием препарата благотворно сказывается на процессе пищеварения в желудке за счет того, что улучшает микроциркуляцию в слизистой оболочке его антрального отдела.
Показания и противопоказания
Де-Нол защищает слизистую оболочку от воздействия соляной кислоты, активных ферментов и других агрессивных факторов, способствую тем самым заживлению эрозивных и язвенных повреждений. Все это определяет показания к назначению препарата:
- Гастриты, гастродуодениты, дуоденит и другие воспалительные заболевания желудочно-кишечного тракта.
- Язвенная болезнь желудка и двенадцатиперстной кишки. В данной ситуации лекарственное средство применяют не только для лечения обострений, но и для снижения риска их возникновения.
- Синдром раздраженного кишечника, который сопровождается расстройством стула, диспепсическим синдромом и болями в животе.
- Гастропатии, обусловленные приемом медикаментозных препаратов или алкоголя.
- Необходимость эрадикации хеликобактерной инфекции. Де-Нол проникает в глубокие слои слизистой оболочки желудка и блокирует метаболизм бактерии.
- Возможно использование при хроническом холецистите или панкреатите, если при них нарушается транспортная функция ЖКТ.
Противопоказания к применению препарата:
- Возраст младше 4 лет.
- Беременность (действующее вещество вызывает мутации у плода, приводит к возникновению врожденных заболеваний нервной системы).
- Период лактации.
- Хроническая почечная недостаточность.
- Индивидуальная непереносимость висмута трикалия дицитрата или вспомогательных компонентов препаратов.
От чего помогают таблетки Де-Нол
Прием этого лекарственного средства показан при:
- Острых и хронических гастритах и гастродуоденитах;
- Обострениях язвы желудка и 12-песрстной кишки;
- Гастропатии, развившейся в результате приема НПВС или алкоголя;
- Функциональных диспепсиях.
Кроме того, врач-гастроэнтеролог может назначить прием Де-Нола при панкреатите. В данном случае препарат помогает устранить дискинезию кишечника, которая нередко сопровождает хронический воспалительный процесс в поджелудочной железе.
Цена в странах СНГ
Стоимость лекарственного средства меняется в зависимости от территориального расположения аптечной сети. Цена 1 упаковки «Де нола»:
- Украина – от 338 до 408 гривен за 112 таблеток с 0,12 г действующего вещества
- Российская федерация – от 890 до 926 рублей за 112 таблеток
- Республика Беларусь – от 34 до 49 белорусских рубля за то же количество
Производитель выпускает еще 1 лекарственную форму – 1 упаковка в 56 таблеток.
Как надо пить Де-Нол
Взрослые и дети старше 12 лет могут принимать по 4 таблетки в сутки. Их можно разделить на 4 или 2 приема.
Таблетки рекомендовано принимать за полчаса до еды, запив водой.
Препарат также применяется при заболеваниях желудка и 12-перстной кишки, которые ассоциированы с бактерией Helicobacter pylori. Де-Нол включается в схемы уничтожения этого микроба наряду с антибактериальными препаратами.
По мнению специалистов, благодаря этому препарату повышается эффективность схемы эрадикации (уничтожения) Helicobacter pylori. Кроме того, прием Де-Нола не сопровождается риском развития лишних побочных реакций, что также немаловажно при использовании такой серьезной схемы лечения.
Некоторые выводы
Хеликобактер можно лечить при помощи препарата Де-Нол.
Изучив инструкцию на это препарат можно сделать определенные выводы:
- Де нол оказывает бактерицидное действие на Хеликобактер, не являясь антибиотиком
- Антибиотики – это продукты, выделенные из определенного вида органических субъктов – грибов, дрожжей. Основной компонент «Де нола» — неорганическое соединение.
- Де нол – дорогостоящий препарат, но существуют и бюджетные аналоги известного противоязвенного средства.
- Лечение язвы комплексное и «Де нол» не может препаратом монотерапии.
Относится ли Де-Нол к антибиотикам
Несмотря на то, что препарат способен уничтожать Helicobacter pylori, он не относится к группе антибактериальных средств. Следовательно, его прием не связан с появлением таких неприятных побочных симптомов, как диарея и кандидоз слизистых.
Бактерии не могут выработать устойчивость к Де-Нолу по причине особенностей его фармакологического действия. Именно поэтому включение этого препарата для уничтожения патогенной бактерии способствует полному избавлению от инфекции.
Как работают ингибиторы протонной помпы
Есть более 500 препаратов для лечения язвы
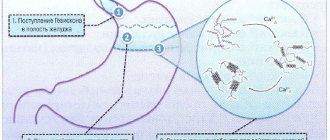
Такое замысловатое название на самом деле обозначает группу препаратов, блокирующих синтез соляной кислоты. Это происходит за счет выведения из строя фермента, транспортирующего в полость желудка такую составную часть формулы кислоты, как ионы водорода. Эта блокада продолжается до тех пор, пока не синтезируются новые ферментные молекулы.
К таким лекарствам относятся Париет, Омез, Нексиум, Омепрозол, Пантопрозол, Лансопрозол, Рабепрозол. Все они обладают очень высокой эффективностью, сохраняя благоприятную среду для того, чтобы заживали дефекты слизистой оболочки, исчезли симптомы диспепсии. Этому способствует сохранение лечебного эффекта в течение 7-12 часов после приема. Заживление язвы двенадцатиперстной кишки происходит за срок 2-4 недели.
Побочные действия препарата Де-Нол
Прием препарата может сопровождаться следующими побочными эффектами:
- Тошнотой и рвотой, учащенным стулом или запором.
- Со стороны ЦНС – развитием энцефалопатии. Данное явление наблюдается только при длительном приеме препарата в высоких дозах.
- Кожным зудом и высыпаниями в случае гиперчувствительности к компонентам лекарственного средства.
Развитие побочных симптомов при приеме Де-Нола наблюдается редко. Обычно при соблюдении всех правил приема этого лекарственного средства пациенты не сталкиваются с подобными проблемами.
Особые указания к применению
Хотя препарат отпускается без рецепта, не стоит забывать о мерах безопасности и соблюдать определенные правила применения лекарственного средства:
- длительность курса лечения не должна быть больше двух месяцев
- суточные дозы должны строго соблюдаться
- употребление лекарственных средств содержащих висмут противопоказано
Симптомы передозировки
Передозировка Де-Нола сопровождается нарушенной функциональной активностью почек. Эти изменения являются обратимыми: после отмены препарата работа почек полностью нормализуется.
В случае передозировки применяются солевые слабительными и энтеросорбенты. Также рекомендуется промывание желудка.
В редких случаях при многократном превышении дозы возможно развитие почечной недостаточности. При этом нарушения работы почек можно компенсировать только гемодиализом.
Препараты висмута в практике врача
Висмут — химический элемент 15-й группы шестого периода периодической системы химических элементов Д. И. Менделеева; имеет атомный номер 83, представляет собой при нормальных условиях блестящий серебристый с розоватым оттенком металл. Собственно, как «висмут» элемент введен в химическую номенклатуру в 1819 г. шведским химиком Й. Берцелиусом. Не обладая ковкостью и тягучестью, висмут легко измельчается в порошок. Висмут был известен с давних времен (первые упоминания о нем в химической литературе относятся к XV веку), но долгое время его считали разновидностью олова, свинца или сурьмы. Представление о висмуте как о самостоятельном химическом элементе сложилось лишь в XVIII веке, после того как в 1739 г. немецким химиком И. Поттом была установлена его химическая индивидуальность [1, 2].
Биологическая роль висмута изучена слабо, ученые предполагают, что этот элемент индуцирует синтез низкомолекулярных белков, принимает участие в процессах оссификации, образует внутриклеточные включения в эпителии почечных канальцев. Современный уровень знаний не позволяет определенно говорить о какой-либо физиологической роли висмута в организме человека. Его поступление в организм с водой или пищей незначительно, т. к. всасывание висмута, поступившего в желудочно-кишечный тракт, крайне мало и составляет около 5%. Суточное поступление висмута в организм с продуктами питания составляет 0,02 мг, а с воздухом — 0,00001 мг.
Гораздо более вероятным представляется поступление висмута в организм с лекарственными препаратами при приеме их внутрь или через кожу (при наружном применении). Суммарно в организм человека с пищей, а также с воздухом и водой поступает висмута в количестве 5–20 мкг/сутки. После всасывания висмут обнаруживается в крови в виде соединений с белками, а также проникает в эритроциты. Между органами и тканями висмут распределяется относительно равномерно. Некоторое накопление висмута может наблюдаться в печени, почках (до 1 мкг/г), селезенке и костях. Обнаруживается висмут и в головном мозге. Висмут относится к категории тяжелых металлов, он является умеренно токсичным элементом. Ряд источников даже называет висмут «самым безобидным» из всех тяжелых металлов. Будучи очень близок по своим свойствам к свинцу, висмут значительно менее ядовит. В связи с этим экологи ратуют за постепенную замену свинца в промышленных и производственных процессах на висмут. Профессиональные отравления или кожные заболевания при работе с висмутом почти не отмечаются, канцерогенность этого металла также не установлена. Обычно даже громадные дозы висмута, принятые перорально, не вызывают отравления, что объясняется трудностью всасывания соединений висмута [2].
За транспортировку висмута к различным органам в организме ответственны лейкоциты. Захваченный лейкоцитами и разнесенный током крови и лимфы по всему организму висмут накапливается в селезенке, центральной нервной системе и органах выделения, к которым относятся почки, печень, кишечник, слюнные железы. Его биодоступность очень низка — 0,16–1,5% от принятой дозы. Средняя концентрация висмута в крови после курсового лечения не превышает 3–58 мкг/л. Следы этого элемента были обнаружены в поте, слезах и грудном молоке. Резорбированный висмут выделяется с мочой. Длительный прием препаратов висмута в больших дозах может вызвать симптомы «висмутовой» энцефалопатии (особенно у больных с нарушением функции почек). На основании анализа 945 клинических случаев было доказано, что побочные эффекты возникают лишь при применении очень высоких доз препаратов (до 20 г/сут) на протяжении длительного (2–20 лет и более) времени [3].
Висмут упоминается в трудах многих авторов книг XV–XVII веков, в частности, у Валентина и Парацельса. 150 лет назад некоторые соединения висмута применялись как обеззараживающее, подсушивающее, вяжущее и антисептическое средство. Висмут является элементом, который, подобно серебру, обладает антимикробными свойствами. Самостоятельное применение висмута для терапевтических целей по причине ряда нежелательных эффектов затруднительно, поэтому оптимизация применения висмута как антибактериального агента связана с разработкой соответствующих форм и комплексов (солей), позволяющих эффективно осуществлять транспорт данного иона к непосредственному месту действия. Терапевтическая активность соединений висмута известна достаточно давно и описана для различных солей висмута, а его пероральное и парентеральное введение предназначалось для лечения ряда заболеваний, таких как сифилис, стенокардия Винсента и амебиазная дизентерия [4]. Когда соли висмута стали широко востребованными, было налажено мелкосерийное производство их препаратов в виде микстур. Широкую известность в Великобритании первой половины XX века получил висмута аммония цитрат (ВАЦ), иногда висмута тартрат, известный как «висмут цитрат аммония с пепсином». Препараты висмута описаны в различных статьях британской фармакопеи (British Pharmaceutical Codex) начиная с издания 1929 г.
Примерно в это же время в Германии были разработаны препараты висмута, в качестве комплексообразователя в которых применялись белковые или пептидные гидролизаты и их фракции (German Pat. № 117 269, German Pat. № 101 683, German Pat. № 202 955). Но они обладали явными недостатками — это ненормируемое высвобождение ионов висмута, (обусловленное значениями рН желудка), адсорбировались в верхних отделах ЖКТ, образуя соединения, обусловливающие проникновение ионов висмута во внутренние среды организма. Эти недостатки способствовали поиску новых эффективных и безопасных производных висмута.
Соединения висмута обладают противоспирохетозным действием, и механизм их действия сводится к тому, что ионы висмута, проникая в спирохеты, связывают сульфгидрильные группы (SН) их ферментов, приводя к нарушению жизнедеятельности и гибели возбудителей сифилиса. Подобные препараты вводятся внутримышечно, так как при приеме внутрь висмутсодержащие соединения практически не всасываются из пищеварительного тракта. Однако при парентеральном поступлении висмута в организм существует опасность поражения тех органов, в которых накапливаются ионы висмута. Токсическая и летальная дозы восемьдесят третьего элемента для человека не определены. Опасным считается хроническое поступление висмута в количествах 1–1,5 грамма в день. Значение солей висмута в медицине с течением времени возрастает. На основе галлата, тартрата, карбоната, трибромфенолята, субцитрата и субсалицилата висмута разработано множество лекарств. В лечебной практике применяются такие препараты, как Викалин, Викаир, Викрам, Нео-Анузол, Висмутовая мазь, Дерматол, Ксероформ, Пентабисмол, Бисмутогви, Де-Нол, Новобисмол и другие.
Предыдущие исследования определили, что сочетание висмута с тиоловыми (-SH, сульфгидрильными) соединениями, такие как, например, этандитиол висмута, улучшают антимикробную активность висмута, по сравнению с другими его солями. Поиск новых оптимизированных трансмиттеров висмута продолжается, о чем свидетельствует недавний патент на изобретение [5], описывающий получение и применение висмут-тиоловой композиции в качестве эффективного антибактериального агента.
Сегодня в России гастроэнтерологи наиболее широко применяют коллоидный субцитрат висмута, или, как его еще называют, висмута трикалия дицитрат (ВТД). Открытие Helicobacter pylori (H. pylori) в 1983 г. австралийцами J. Warren и B. Marshall совершило революцию в лечении язвенной болезни [6], оно возобновило интерес к соединениям висмута, так как было установлено, что соли висмута эффективно подавляют рост H. pylori в сочетании с антибиотиками или в комбинации с антибиотиками и кислотосупрессивными препаратами [7, 8]. Первое рандомизированное контролируемое исследование (РКИ) с применением висмута в антихеликобактерной терапии выявило, что висмут был эффективнее монотерапии эритромицином [9]. Другое РКИ в течение 6 недель сравнивало эффективность коллоидного субцитрата висмута против циметидина при H. pylori-положительной язвенной болезни двенадцатиперстной кишки, в результате висмут успешно эрадицировал H. pylori у 50% больных [10]. Следующее РКИ оценивало совместное применение коллоидного субцитрата висмута и циметидина, отдельно или в сочетании с тинидазолом, в результате было выявлено, что коллоидный субцитрат висмута и тинидазол достигли эрадикации H. pylori почти у 75% пациентов [11]. С добавлением второго антибиотика тетрациклина или амоксициллина частота эрадикации в более поздних РКИ превысила уже 80% [12–14]. Тем не менее, были выявлены некоторые проблемы, связанные с тройной терапией на основе висмута, — это большое количество таблеток, которые пациенты были обязаны принять, продолжительность терапии и побочные эффекты, например, изменение вкуса, тошнота и диарея. Систематический обзор и метаанализ A. Ford и соавт. убедительно свидетельствуют о том, что соединения висмута, используемые либо отдельно, либо в сочетании с антибиотиками и ингибиторами протонной помпы (ИПП) для эрадикации H. pylori, являются безопасными и хорошо переносятся [15].
ВТД замедляет процессы всасывания некоторых антибиотиков (тетрациклин, амоксициллин), способствуя тем самым повышению их концентрации в желудочном содержимом — месте приложения при лечении хеликобактериоза. В исследованиях in vitro и in vivo было показано, что ВТД обладает синергизмом с другими антибиотиками в отношении H. pylori. Благодаря этому свойству он стал непременным компонентом антихеликобактерной терапии, а его сочетание с двумя антибиотиками и поныне называют «классической тройной терапией». Кроме того, одним из способов преодоления резистентности H. pylori является применение в качестве базисного препарата коллоидного трикалия дицитрата висмута. Это положение подтверждается изучением антибактериальной активности in vitro комбинаций различных препаратов с кларитромицином и амоксициллином в отношении штаммов H. pylori, чувствительных или резистентных к макролидам. Было показано, что свойства ВТД играли решающую роль в преодолении резистентности штаммов и получении стойкого бактерицидного эффекта указанных комбинаций препаратов [16].
Многочисленные научные исследования, проведенные на фоне применения висмута трикалия дицитрата при эрозивно-язвенных поражениях различной этиологии, показали, что препарат обладает широким спектром механизмов цитопротекции. ВТД снижает активность пепсина (на 20–30%); селективно связывается с белками дна язвы и создает защитный слой — барьер для диффузии H+, который препятствует повреждению области слизистой оболочки (СО) желудка, лишенной защитного эпителиального покрова; стимулирует локальный синтез простагландинов (в среднем на 50%); увеличивает секрецию слизи и гидрокарбонатов; усиливает местный кровоток; подавляет продукцию цитокинов клетками воспалительного инфильтрата; обеспечивает реконструкцию экстрацеллюлярного матрикса и полноценный ангиогенез; усиливает репаративный эффект, опосредованный эпидермальным фактором роста. Морфологически слизистая оболочка гастродуоденальной зоны после заживления язвы ближе к нормальной микроструктуре, чем при лечении другими средствами. Применение высоких доз ВТД стимулирует выработку простагландина Е2 в желудочной слизи, которая рассматривается как часть механизма, ускоряющего заживление язвенных поражений. Терапевтические дозы ВДТ вызывают устойчивую стимуляцию продукции простагландинов [17].
Механизм антибактериального действия висмута трикалия дицитрата связан не только с нарушением адгезии микроорганизмов к эпителию слизистой оболочки, но и с нарушением синтеза АТФ в бактериальной клетке. Так, в исследовании in vitro инкубация H. pylori с висмута трикалия дицитратом приводила к выраженному угнетению роста микроорганизма и его последующей гибели [18]. Благодаря антихеликобактерной активности препараты коллоидного висмута позволяют повысить или сохранить эффективность эрадикационной терапии, особенно в условиях растущей антибиотикорезистентности H. pylori. Антихеликобактерный моноэффект ВТД составляет в среднем 14–40%. Преимущество препарата состоит в том, что не существует естественной или приобретенной резистентности H. pylori к ионам висмута. Сочетание с антибиотиками увеличивает степень эрадикации до 50%, а сочетание двух базисных препаратов — ингибитора протонной помпы и висмута трикалия дицитрата — с двумя антибиотиками позволяет преодолеть резистентность штаммов H. pylori к производным нитримидазолов либо кларитромицину.
Интересные результаты представили C. Srinarong и соавт. — 7-дневная стандартная тройная терапия плюс ВТД и пробиотик обеспечили отличную эрадикацию H. pylori (100%) в районах с низкой его резистентностью к кларитромицину, таких как Таиланд, независимо от CYP2C19 генотипа возбудителя [19].
В последние годы показано значение окислительного стресса, потенцируемого бактериями H. pylori (особенно имеющими генотип CagA+/vacAs1), в развитии хронического гастрита [20]. Препараты висмута оказались способными улавливать свободные кислородные радикалы, образующиеся при окислительном стрессе и повреждающие СО желудка, что служит одной из составляющих их цитопротективного действия [21].
BTД хорошо зарекомендовал себя и как препарат, который с успехом может назначаться при лечении эрозивно-язвенных поражений желудка и двенадцатиперстной кишки, вызванных приемом нестероидных противовоспалительных препаратов (НПВП-ассоциированной гастропатии). Так, при сравнительном изучении эффективности применения ВТД и ранитидина заживление язв и множественных эрозий желудка и двенадцатиперстной кишки через 4 нед лечения было достигнуто у 84,6% больных, получавших ВТД, и лишь у 50% пациентов, получавших ранитидин [22]. В сравнительном исследовании по эффективности применения ВТД (в дозе 240 мг 2 раза в сутки) в комбинации со стандартной дозой омепразола (20 мг в сутки) и монотерапии омепразолом у больных с НПВП-ассоциированной гастропатией заживление эрозивно-язвенных поражений желудка и двенадцатиперстной кишки через 2 нед лечения было достигнуто соответственно у 56,7% и 30,3% больных, а через 4 нед — у 100% и 93,9% пациентов. Повышение уровня простагландинов в СО желудка, отмечавшееся на фоне приема ВТД, свидетельствовало о цитопротективном действии препарата [23, 24].
Благодаря известным антидиарейным свойствам, соединения висмута широко используются для лечения эпизодических поносов у детей и взрослых на протяжении целого столетия [25–28]. Ряд исследований подтвердили эффективность висмута субсалицилата в профилактике и лечении диареи (E. coli энтеротоксигенной) путешественника. Энтеротоксигенная E. coli обнаруживалась реже у тех путешественников, которые получали висмута субсалицилат, чем у тех, кто получали плацебо, доказывая, что висмута субсалицилат предотвращает диарею, уменьшая количество и подавляя размножение энтеротоксигенной E. coli [29].
Два исследования сообщили об эффективности лечения висмутом в клизмах при язвенном колите с поражением дистальных отделов. Клинико-лабораторное улучшение наблюдалось у 60% пациентов, резистентных к обычной терапии, а у 40% пациентов была достигнута полная ремиссия после 8 недель терапии [30]. Многоцентровое, двойное слепое, рандомизированное, сравнительное исследование показало, что при сравнении эффективности лечения висмутом в клизмах с клизмами 5-аминосалициловой кислоты был установлен эквивалентный терапевтический эффект при лечении левостороннего язвенного колита [31]. Пероральный висмут также эффективен при микроскопическом колите [32] и в качестве колостомического дезодоранта [33].
В дополнение к своим антибактериальным свойствам [34, 25], висмут также обладает противовоспалительными эффектами [36] при прохождении по кишечнику. Существуют экспериментальные данные, подтверждающие роль висмута в ингибировании активности индуцируемой синтазы оксида азота в эпителиальных клетках кишечника, а также в индукции гемоксигеназы-1, тем самым обуславливая терапевтический эффект при воспалительных и окислительных реакциях, связанных с воспалительными заболеваниями кишечника [37]. Еще одно экспериментальное исследование показало способность висмута поглощать кислород свободных радикалов в контексте химических повреждений слизистой желудка [38]. Учитывая эти антибактериальные и противовоспалительные механизмы, можно теоретически предположить, что висмут должен играть определенную роль в патогенетическом лечении острой и хронической диареи, как антибактериальный и антитоксический агент [39].
Сероводород, другие зловонные и токсичные соединения продуцируются бактериями толстой кишки при гниении белка. При умеренно тяжелой форме язвенного колита [40] сероводород участвует в ингибировании окисления бутирата слизистой толстой кишки, что делает слизистую оболочку более уязвимой к воспалительным агентам [41, 42]. Висмут, соединяясь с сероводородом, образует нерастворимый безвредный сульфид висмута и окрашивает кал в черный цвет [43].
Целью нашего оригинального исследования стала оценка сравнительных характеристик инфракрасных спектров (ИК-спектров) двух готовых лекарственных форм висмута. В исследовании проанализированы спектральные характеристики наиболее востребованных висмут-содержащих препаратов, а именно препаратов Де-Нол® (Нидерланды) и Новобисмол® (Россия). Активным действующим веществом этих препаратов является висмута трикалия дицитрат.
Спектральные характеристики получены с помощью инфракрасного фурье-спектрометра ФСМ-1202 (Россия). Фармакологически активная часть таблетированной формы смешивалась с бромидом калия (Fluka, Германия) в соотношении 1:100, и с помощью гидравлического пресса формировался диск. Измерение проводили в диапазоне 4000–400 см-1, с разрешением 4 см-1 и числом сканов 25. Управление прибором и обработка данных осуществлялась с применением программы Fspec 4,0. Исследованные нами образцы имели идентичные инфракрасные спектры (рис.).
Спектральная характеристика образцов висмута трикалия дицитрата интересна с точки зрения спектральных характеристик комплексного соединения. Так, на спектре образцов можно отметить две характеристические широкие полосы поглощения 1579 и 1393 см-1, обусловленные валентными симметричными и асимметричными колебаниями в СОО-фрагменте. Такой тип связей возникает в хелатном соединении между карбоксильными группами цитратных фрагментов и комплексообразователем висмутом. Именно данная хелатная форма обуславливает сдвиг полос поглощения соответствующий RСОO- и в обычных условиях прослеживаются около 1560 и 1410 см-1. Необходимо отметить, что подобные смещения в ИК-области полос поглощения для комплексных соединений другого типа ранее описывались в литературе [44]. Полоса поглощения 1290 см-1, обнаруженная у комплекса, по нашему мнению, обусловлена колебаниям С-О и О-Ме (где Ме — ионы калия или висмута). Именно ионы металлов обуславливают смещение деформационных (внеплоскостных) колебаний ОН (950–900 см-1) до значения 845 см-1, что соответствует рассматриваемому висмутовому комплексу. Колебаниям С-С-связей соответствует полоса поглощения 910 см-1. Соответственно полосы 1142, 1076, 1020 см-1 обусловлены валентными колебаниям С-О и фрагментам СН-О– [45].
Таким образом, данное исследование указывает на практически полную фармацевтическую эквивалентность исследованных нами препаратов Де-Нол® и Новобисмол®.
Литература
- Глинка Н. Л. Общая химия. Л.: Химия, 2004. 702 с.
- https://ru.wikipedia.org/w/index.php?title=Висмут.
- Висмутсодержащие препараты в гастроэнтерологии. Обзор // Здоровье Украины. 2009. № 13–14. С. 64–65.
- Kuever R. A., Wheeler L. M. Bismuth compounds / United States Patent US2414650. Publication Date: January 21, 1947. Application Number: US48796443A.
- Bismuth-thiols as antiseptics for epithelial tissues, acute and chronic wounds, bacterial biofilms and other indications / United States Patent US8389021. Publication Date: 03.05.2013.
- Warren J. R., Marshall B. J. Unidentified curved bacilli on gastric epithelium in active chronic gastritis // Lancet. 1983. № 321. Р. 1273–1275.
- Wolle K., Malfertheiner P. Treatment of Helicobacter pylori // Best Pract Res Clin Gastroenterol. 2007. № 21. Р. 315–324.
- Marshall B. J., Warren J. R. Unidentified curved bacilli in the stomach of patients with gastritis and peptic ulceration // Lancet. 1984. № 1. Р. 1311–1315.
- McNulty C. A., Gearty J. C., Crump B., Davis M., Donovan I. A., Melikian V., Lister D. M., Wise R. Campylobacter pyloridis and associated gastritis: investigator blind, placebo controlled trial of bismuth salicylate and erythromycin ethylsuccinate // Br Med J (Clin Res Ed). 1986. № 293. Р. 645–649.
- Coghlan J. G., Gilligan D., Humphries H., McKenna D., Dooley C., Sweeney E., Keane C., O’Morain C. Campylobacter pylori and recurrence of duodenal ulcers — a 12-month follow-up study // Lancet. 1987. № 2. Р. 1109–1111.
- Marshall B. J., Goodwin C. S., Warren J. R., Murray R., Blincow E. D., Blackbourn S. J., Phillips M., Waters T. E., Sanderson C. R. Prospective double-blind trial of duodenal ulcer relapse after eradication of Campylobacter pylori // Lancet. 1988. № 2. Р. 1437–1442.
- Graham D. Y., Lew G. M., Evans D. G., Evans D. J., Klein P. D. Effect of triple therapy (antibiotics plus bismuth) on duodenal ulcer healing. A randomized controlled trial // Ann Intern Med. 1991. № 115. Р. 266–269.
- Graham D. Y., Lew G. M., Klein P. D., Evans D. G., Evans D. J. Jr., Saeed Z. A, Malaty H. M. Effect of treatment of Helicobacter pylori infection on the long-term recurrence of gastric or duodenal ulcer. A randomized, controlled study // Ann Intern Med. 1992. № 116. Р. 705–708.
- Rauws E. A., Tytgat G. N. Cure of duodenal ulcer associated with eradication of Helicobacter pylori // Lancet. 1990. № 335. Р. 1233–1235.
- Ford A. C., Malfertheiner P., Giguère M. et al. Adverse events with bismuth salts for Helicobacter pylori eradication: Systematic review and meta-analysis // World J Gastroenterol. 2008. № 14 (48). Р. 7361–7370.
- Щербаков П. Л., Вартапетова Е. Е., Нижевич А. А. и др. Эффективность и безопасность применения висмута трикалия дицитрата (де-нол) у детей // Клин. фармакол. тер. 2005. № 1. С. 41–44.
- Оковитый С. В., Ивкин Д. Ю. Препараты висмута — фармакологические основы клинического эффекта // Лечащий Врач. 2015. № 10. С. 1–7.
- Stratton C. W., Warner R. R., Coudron P. E., Lilly N. A. Bismuth-mediated disruption of the glycocalyx-cell wall of Helicobacter pylori: ultrastructural evidence for a mechanism of action for bismuth salts // J Antimicrob Chemother. 1999, May. № 43 (5). Р. 659–666.
- Srinarong C., Siramolpiwat S., Wongcha-Um A., Mahachai V., Vilaichone R. K. Improved Eradication Rate of Standard Triple Therapy by Adding Bismuth and Probiotic Supplement for Helicobacter pylori Treatment in Thailand // Asian Pac J Cancer Prev. 2014. № 15 (22). Р. 9909–9913.
- Augusto A. C., Miguel F., Mendonca S. et al. Oxidativestress expression status associated to Helicobacter pylori virulence in gastric disease // Clin. Biochem. 2007. Vol. 40. P. 615–622.
- Bagchi D., McGinn Th., Ye X. et al. Mechanism of gastroprotection by bismuth subsalicylate against chemically induced oxidative stress in cultured human gastric mucosal cells // Dig. Dis. Sci. 1999. Vol. 44. P. 2419–2428.
- Каратеев А. Е., Насонов Е. Л., Раденска-Лоповок С. Г. Эффективность висмута трикалия дицитрата (Де-Нола) при гастропатиях, индуцированных нестероидными противовоспалительными препаратами: открытое контролируемое 4-недельное исследование // Тер. арх. 2005. № 2. С. 45–49.
- Маев И. В., Вьючнова Е. С., Стасева И. В. Сравнительная оценка различных схем терапии гастропатий, вызванных нестероидными противовоспалительными препаратами // Тер. арх. 2004. № 2. С. 27–30.
- Шептулин А. А., Визе-Хрипунова М. А. Современные возможности применения препаратов висмута в гастроэнтерологии // Российский журнал гастроэнтерологии, гепатологии, колопроктологии. 2010. № 3. С. 63–67.
- DuPont H. L., Sullivan P., Pickering L. K., Haynes G., Ackerman P. B. Symptomatic treatment of diarrhea with bismuth subsalicylate among students attending a Mexican university // Gastroenterology. 1977. № 73. Р. 715–718.
- Bierer D. W. Bismuth subsalicylate: history, chemistry, and safety // Rev Infect Dis. 1990. № 12. Р. S3–S8.
- Gryboski J. D., Kocoshis S. Effect of bismuth subsalicylate on chronic diarrhea in childhood: a preliminary report // Rev Infect Dis. 1990. № 12. Р. S36–S40.
- Figueroa-Quintanilla D., Salazar-Lindo E., Sack R. B. et al. A controlled trial of bismuth subsalicylate in infants with acute watery diarrheal disease // N Engl J Med. 1993. № 328. Р. 1653–1658.
- De la Cabada B. J., Dupont H. L. New Developments in Traveler’s Diarrhea // Gastroenterol Hepatol. 2011, Feb. № 7 (2). Р. 88–95.
- Ryder S. D., Walker R. J., Jones H., Rhodes J. M. Rectal bismuth subsalicylate as therapy for ulcerative colitis // Aliment Pharmacol Ther. 1990. № 4. Р. 333–338.
- Pullan R. D., Ganesh S., Mani V. et al. Comparison of bismuth citrate and 5-aminosalicylic acid enemas in distal ulcerative colitis: a controlled trial // Gut. 1993. № 34. Р. 676–679..
- Fine K. D., Lee E. L. Efficacy of open-label bismuth subsalicylate for the treatment of microscopic colitis // Gastroenterology. 1998. № 114. Р. 29–36.
- Degos R. Bismuth in the treatment of syphilis // Int J Dermatol. 1977. № 16. Р. 391–392.
- Sun H., Zhang L., Szeto K. Y. Bismuth in medicine // Met Ions Biol Syst. 2004. № 41. Р. 333–378.
- Degos R. Bismuth in the treatment of syphilis // Int J Dermatol. 1977. № 16. Р. 391–392.
- Ericsson C. D., Tannenbaum C., Charles T. T. Antisecretory and antiinflammatory properties of bismuth subsalicylate // Rev Infect Dis. 1990. № 12. Р. S16–S20.
- Cavicchi M., Gibbs L., Whittle B. J. Inhibition of inducible nitric oxide synthase in the human intestinal epithelial cell line, DLD-1, by the inducers of heme oxygenase 1, bismuth salts, heme, and nitric oxide donors // Gut. 2000. № 47. Р. 771–778.
- Bagchi D., McGinn T. R., Ye X. et al. Mechanism of gastroprotection by bismuth subsalicylate against chemically-induced oxidative injury in human gastric mucosal cells // Gastroenterology. 1998. № 114. Р. A62.
- Thazhath S., Haque M., Florin T. Oral bismuth for chronic intractable diarrheal conditions? // Clin Exp Gastroenterol. 2013. № 6. Р. 19–25.
- Florin T. H. J., Gibson G. R., Neale G., Cummings J. H. A role for sulfate reducing bacteria in ulcerative colitis? // Gastroenterology. 1990. № 98. Р. A170.
- Roediger W. E. The colonic epithelium in ulcerative colitis: an energy-deficiency disease? // Lancet. 1980. № 2. Р. 712–715.
- Chapman M. A., Grahn M. F., Boyle M. A., Hutton M., Rogers J., Williams N. S. Butyrate oxidation is impaired in the colonic mucosa of sufferers of quiescent ulcerative colitis // Gut. 1994. № 35. Р. 73–76.
- Suarez F. L., Furne J. K., Springfield J., Levitt M. D. Bismuth subsalicylate markedly decreases hydrogen sulfide release in the human colon // Gastroenterology. 1998. № 114. Р. 923–929.
- McQuillin F. J., Parker D. G., Stephenson G. R. Transition metal organometallics for organic synthesis // Cambridge university press, Cembridge. 1991. P. 19–20.
- Преч Э., Бюльманн Ф., Аффольтер К. М. Определение строения органических соединений / Мир; БИНОМ. 2006. 438 с.
Е. Ю. Плотникова1, доктор медицинских наук, профессор А. С. Сухих, кандидат медицинских наук
ГБОУ ВПО КемГМА МЗ РФ, Кемерово
1 Контактная информация
* Препарат в РФ не зарегистрирован.
Как правильно диагностировать атрофию слизистой желудка?
Для диагностики атрофического гастрита используется ФГДС (гастроскопия) с забором не менее 5 биоптатов (небольших фрагментов слизистой) из разных отделов желудка. Количество биоптатов определено строением желудка, так как атрофия в разных отделах развивается разными темпами, и поэтому необходимо произвести забор из всех пяти отделов.
Диагноз устанавливается врачом-морфологом после проведения гистологического исследования. На основании данного исследования подбирается лечение и определяется периодичность обследований для своевременного выявления онкологического процесса.
Также для оценки выраженности атрофии используется определение активности секреторной функции желудка по лабораторному анализу крови – Гастропанель (ссылка).
Диагностику хеликобактерной инфекции проводят с помощью исследования биоптатов и 13С-уреазного дыхательного теста.
При аутоиммунном гастрите проводятся лабораторная диагностика анализа крови на определение антител к клеткам желудка и к внутреннему фактору Кастла.