Соляная кислота Раствор хлорводорода в воде, который является бесцветной прозрачной жидкостью.
Из-за присутствия единственного элемента (односоставной примеси) в воде считается едкой в силу своих химических свойств. При соприкосновении с воздухом исходит «дымок».
Формула HCl
Техническая кислота (Cl – H) имеет такую же формулу, но отличается по цвету – из-за примесей железа и хлора отдает желтоватым оттенком. Концентрация раствора зависит от температурного режима хранения, и при 20 градусах она составляет 38% с плотностью 1,18 г/см3. Соль раствора называется хлоридом.
Альтернативные названия
Хлористоводородная кислота или хлористый водород.
Получение соляной кислоты
Соляную кислоту получают путём растворения газообразного хлороводорода в воде. Его сжигают в хлоре, в результате чего на выходе имеется синтетическая кислота. Также получение возможно из побочных газов при хлорировании углеводорода. В первом случае она будет иметь меньше примесей, а второй необходим в промышленности, когда спрос на абгазную кислоту увеличивается.
В лабораторных условиях используют серную кислоту и поваренную соль:
- При температуре в 550 градусов и выше поваренная соль дает избыток.
- При проведении гидролиза магния и алюминия хлоридов (нагревание гидратированной соли).
- При получении оксихлоридов, когда происходит неполное растворение солей (реакция не завершается).
Чем выше температура окружающей среды, тем ниже способность к растворению. Поэтому на практике используют 36%-ую кислоту, хотя при 0-1 градусе кислород поглотит больше половины примесей, что равно 45%-ой кислоте.
Физические свойства
Хлороводородная кислота — это прозрачная жидкость без цвета с характерным едким запахом. Образуется при пропускании хлороводорода через воду. В реакциях также участвует в жидком состоянии. Хорошо растворяется в воде, т. е. смешивается с ней. Соляная кислота, полученная промышленным путем, имеет слегка желтую окраску из-за примесей элементов. Концентрированная кислота, как и хлороводород, “дымит” во влажном воздухе.
Молекулярная кристаллическая решетка, в узлах которой находятся молекулы HCl, в молекуле — ковалентная полярная связь.
Свойства соляной кислоты
Физические свойства
Физические свойства кислоты зависят от степени концентрации растворенного хлороводорода. При повышении наблюдается: • Увеличение плотности раствора; • Увеличение молярности; • Снижение водородного показателя (pH); • Увеличение вязкости вещества; • Снижение удельной теплоёмкости; • Увеличение давления пара; • Снижение температуры кипения; • Вариации температуры плавления.
Последние меняются так: при минимальной и максимальной концентрации плавление достигает максимальных показателей. Средняя концентрация поддаётся плавлению в минимальных температурах. Затвердевшее вещество даёт кристаллогидраты – HCl·H2O, HCl·6H2O, HCl·3H2O, HCl·2H2O.
Химические свойства
- Взаимодействует с металлами (Ме) электрохимических потенциалов:
Mg+2HCl = MgCl2+H2.
Образуется соль с выделением водорода.
- Взаимодействует с оксидами Ме:
Na2O+2HCl = 2NaCl+H2O
с образованием соли и воды.
- Реакция нейтрализации с гидроксидами Ме:
NaOH+HCl = NaCl+H2O
с образованием растворимой соли и воды.
Также вступает в реакцию с солями Ме, окислителями с выделением хлорного газа и аммиаком с выделением густого белого дыма из кристаллов аммония хлорида.
Получение
Алхимики называли С. к. муриевой (от лат. muria – рассол, рапа) и получали её прокаливанием поваренной соли с купоросом. В сер. 17 в. И. Глаубер предложил способ получения концентрир. С. к. нагреванием поваренной соли с серной кислотой. Широко доступной С. к. стала в 19 в. в связи с разработкой Н. Лебланом способа получения соды, в котором хлороводород был побочным продуктом. Совр. произ-во С. к. (синтетич., абгазной, реактивной) заключается в абсорбции HCl водой. В зависимости от способа отвода теплоты абсорбции процессы подразделяются на изотермические, адиабатические и комбинированные.
При изотермич. абсорбции процесс осуществляется с отводом теплоты, и темп-ра кислоты поддерживается постоянной за счёт непосредственного охлаждения абсорбера либо благодаря охлаждению циркулирующей кислоты в выносном холодильнике. При этом теоретически можно получить С. к. любой концентрации, т. к. с понижением темп-ры уменьшается и парциальное давление HCl над С. к. Изотермич. абсорбцию следует применять для получения концентрир. С. к. (35–38%) и для переработки хлороводорода низкой концентрации. В последнем случае при содержании в реакционных газах св. 40% примесей (азота, водорода, метана и др.) проведение абсорбции в изотермич. условиях нецелесообразно ввиду ухудшения теплоотдачи и уменьшения полноты абсорбции. Изотермич. абсорбцию можно проводить в поверхностных абсорберах – газ проходит над поверхностью неподвижной или медленно текущей жидкости. Такие абсорберы применяют лишь при сравнительно небольших масштабах произ-ва. Обычно устанавливают каскад абсорберов.
При адиабатич. абсорбции процесс осуществляется без отвода теплоты. С. к. нагревается до кипения за счёт теплоты растворения хлороводорода. При этом увеличивается давление паров С. к. и начинается интенсивное испарение воды. Последнее вызывает снижение темп-ры кипящей кислоты и возрастание концентрации С. к. Темп-ра абсорбции определяется точкой кипения С. к. соответствующей концентрации. Исходный газ, содержащий НСl, вводят снизу в колонну; противотоком ему поступает абсорбент (обычно вода). Вместо воды или вместе с водой для орошения колонны может применяться разбавленная С. к. Если абсорбентом является кислота, эффективность абсорбции НСl снижается и составляет 95–99% в зависимости от концентрации кислоты и давления паров НСl. Если абсорбентом является вода, НСl может быть полностью поглощён. Концентрация НСl в жидкости возрастает в направлении от верха колонны к низу.
Комбинир. схема абсорбции состоит из адиабатич. и изотермич. ступеней, варьирующихся в зависимости от мощности, состава реакционного газа и др. условий.
Синтетич. С. к. производят из HCl, полученного при взаимодействии H2 и Cl2. Для получения реактивной С. к. (марки «ч», «чда», «хч» концентрацией 35–38%) используют HCl, полученный из испарённого хлора и электролитич. водорода в графитовых печах с последующей изотермич. абсорбцией дистиллированной водой в графитовых абсорберах. Бóльшую часть С. к. производят из HCl, содержащегося в отходящих газах («абгазах») процессов хлорирования, дегидрохлорирования, пиролиза хлорсодержащих соединений, получения хлоридов металлов и др. Абгазная С. к., как правило, содержит примеси: хлор, хлорорганич. соединения, кислоты, спирты, альдегиды и др. Для очистки абгазной С. к. используют: отдувку инертным газом (HCl, воздух, азот, метан и др.); отпарку, при которой концентрация кислоты снижается на 1–2%; предварительную промывку абгазной С. к., при которой растворяются водорастворимые примеси; сорбционные методы и др. Мировое произ-во С. к. ок. 20 млн. т/год.
Применение соляной кислоты
Применение широко распространено в сферах гидрометаллургии и гальванопластике. Проводится очистка поверхностей металлов при помощи кислот; для получения цинковых хлоридов. Иногда техническая соляная кислота необходима для чистки керамики и металлических изделий. Для этого берётся ингибированная кислота, предназначенная специально для дезинфекций.
В пищевой промышленности она необходима для урегулирования кислотности продуктов. Зарегистрировано вещество под кодом пищевой добавки Е507. Чаще всего используется при изготовлении зельтерской воды (содовая).
В фармацевтической промышленности соляная кислота нужна для изготовления лекарственных препаратов, предназначенных для смеси с ферментами пепсинов. При недостатке естественной кислоты в желудочном соке в концентрации 0,5% назначается приемом внутрь.
Где встречается
Встретить ее в натуральном виде можно в составе кисломолочных продуктов. Образуется она призамешивании и выстаивании дрожжевого теста. Для получения применяют сбраживание раствора сахара и молочных отходов при помощи молочнокислых бактерий.
Продукт Е270, активно используемый в пищевой и перерабатывающей промышленности, является представителем группы карбоновых кислот, выглядит он как прозрачная, не имеющая осадка жидкость, имеет специфичный запах и характерный кислый вкус. Наличие его в составе консервов предупреждает возникновение процессов брожения и развития болезнетворных микробов.
В живых организмах молочная кислота вырабатывается в результате расщепления глюкозы, представляющей собой источник энергии для работы мышц и мозга.
Чем активнее трудится человек, тем большее количество ее вырабатывает его организм. Для взрослого мужчины нормой считается выработка 120-150 г в сутки. Излишки ее выводятся через почки.
Желудок и пищевод / Вечная борьба с кислотой?
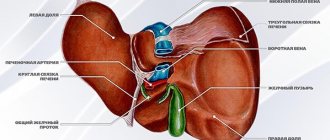
Несмотря на то, что основная функция желудка, это механическая обработка пищи, все же есть и дополнительные. В том числе и выделение соляной кислоты и желудочного сока. Кислота выполняет одну из очень важных функций – обезвреживание поступившей в организм пищи от микробов. Соляная кислота, которую выделяет желудок способна убить 85-95% всех попадающих с пищей бактерий. Именно благодаря ей у нас не возникает ежедневное пищеводе отравление.
Кроме того, кислота подготавливает к перевариванию самые сложные для пищеварения продукты – белки. Они должны расщепляться на мелкие кусочки, аминокислоты, чтобы попасть в организм. Соляная кислота раскручивает сложную структуру молекулы белка, для того, чтобы потом в кишечнике этот белок дорезали ферменты.
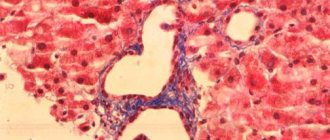
Кислоту выделяют специальные клетки, расположенные в стенке желудка, они называются главные клетки или париетальные клетки. В каждой такой клетке есть специальный кислотный насос. Он качает ионы водорода в желудок, там они соединяются с ионами хлора и получается соляная кислота.
Кислотный насос можно запустить разными «кнопками», все они включаются различными веществами. Например, есть гистаминовая кнопка, соматостатиновая кнопка, ацетилхолиновая кнопка – по названию веществ, запускающих выработку соляной кислоты. На эти кнопки действуют многие лекарственные препараты, блокирующие выделение кислоты в желудке. Но каждый способ имеет свои особенности, например, при разных заболеваниях, или, когда мы принимаем разные таблетки. Кроме того, к выделителям кислоты подключены нервные волокна, которые по сигналу «сверху» тоже могут влиять на выделение кислоты в желудке.
Многим очень интересно, когда же правильно пить воду, и что происходит, когда мы пьем воду во время еды. Некоторые считают, что это приводит к разведению или разбавлению желудочного сока и уменьшению кислотности. Это мнение отчасти правильное, но не полностью.
Дело в том, что желудок выделяет определенное количество соляной кислоты. Количество кислоты зависит от объема пищи. В норме существует прямая регулирующая связь между тем количеством пищи, которое прошло через рот и пищевод в желудок, и точно соответствующим этому количеством кислоты. Чем больше съели, тем больше кислоты выделил желудок, и наоборот, чем меньше съели, тем меньше кислоты выделил желудок.
Если мы добавим в желудок воды или другой жидкости, то количество выделяемой кислоты не изменится. На примере условных цифр, мы съели 500 г еды и на это образовалось 100 г кислоты. Добавили воды, кислоты как было 100 г, так и осталось 100 г. Да, она стала чуть более разведенной, но это никак не влияет на переваривание. Во-первых, потому что в желудке ничего не переваривается, это происходит чуть дальше. Во-вторых, в большем объеме кислота быстрее обрабатывает содержимое. В-третьих, более жидкое содержимое быстрее покинет желудок и быстрее начнет перевариваться.
Многие люди при возникновении неприятных ощущений в желудке или при появлении изжоги самостоятельно начинают принимать какие-то лекарства или народные средства. На самом деле нет ничего плохого в том, что они делают это самостоятельно, главное, чтобы это было не бездумно! Нужно хотя бы немного понимать, что происходит в желудке.
Некоторые народные средства представляют собой просто щелочь, она нейтрализует часть кислоты в желудке. На первый взгляд становится легче, но если при воспалении убрать не всю кислоту, то вылечиться невозможно. А если убрать всю кислоту с запасом, то можно то же самое воспаление еще и усилить щелочью или, например, содой. Будьте аккуратнее.
Многие лекарства нужно, на самом деле, просто правильно начинать принимать и правильно заканчивать принимать. Некоторые до сих пор используют старые препараты, на которых развивается так называемое «ускользание» эффекта, то есть сначала лекарство помогает. А потом перестает помогать. Другие встречаются с синдромом «рикошета», когда сразу после завершения приема таблеток симптомы начинаются снова. Все эти трудности на пути к полному излечению легко преодолеваются, если о них знать и знать, что с этим делать. К сожалению, знают не все, поэтому мучаются с болячками долго, если не сказать пожизненно.
Если желудок выделяет мало кислоты, скорее всего вы не будете об этом знать и думать. Потому, что уменьшение количества кислоты не беспокоит никакими симптомами, происходит постепенно и незаметно. Проблема только в том, что с течение времени слизистая оболочка в желудке становится слабой, тонкой, в ней развивается атрофия, метаплазия и дисплазия, и в конце это приводит к раку желудка.
Важно знать, что количество кислоты становится не настолько меньше и это не настолько важно, по сравнению с количеством самих клеток, которые ее выделяют. Когда проводят диагностику, нужно посмотреть в результатах обследований, какая степень выраженности этой самой атрофии, и есть ли она вообще. Если есть, то методы лечения абсолютно иные и в корне отличаются от обычного гастрита, тогда лечение не помогает.
Нужно постараться не допустить последней стадии и постепенно восстановить состояние желудка. К сожалению, так получается, что нам всем ставят гастрит, и не указывают какой, есть ли атрофия или ее нет. В результате мы получаем не самое эффективное лечение, назначенное вслепую, или постоянное возобновление симптомов, которые нужно был взять и вылечить.
Нельзя терпеть симптомы со стороны желудка, если они стали регулярными илипоявляются чаще одного раза в неделю. Вопреки мнению о том, что гастрит есть у всех,спешу сообщить, что это не так. Гастрит – это воспаление желудка, которое нужнопросто взять и вылечить. Но до конца! Так, чтобы оно не возвращалось снова. Поскольку внашей стране есть определенные проблемы с организацией здравоохранения, в надеждеисправить ситуацию мы создали этот проект.
Больше статей
Следующая статья
Кислотность желудочного сока
Такой важный аспект, как рН желудка напрямую зависит от соляной кислоты. И если наблюдается отклонение от нормы, возникает гастрит, диспепсические расстройства и другие неприятные состояния. Кислотность в желудке может быть пониженной, нормальной и повышенной.
Несмотря на «популярность» повышенной pH, зачастую у людей наблюдается пониженная или же нормальная кислотность. Последняя составляет от 0,8 до 1,5.
Пониженная кислотность желудка
Пониженная кислотность возникает при постоянных стрессах и воспалительных заболеваниях. Происходит это за счет возбуждения симпатической нервной системы, которая напрямую влияет на продукцию желудочного сока. Понижение кислотности влечет за собой ухудшение переваривания пищи и спазм желудка. Еда остается в полости, начинает гнить, усиливая размножение патогенных бактерий. Человек мучится от метеоризма и тошноты. Последняя является ответом на спазм желудка. Более того, активно нарушается процесс всасывания всех питательных элементов, содержащихся в нашей пище, что ведет к нарушению работы всего организма. Кстати, именно на почве естественного снижения pH после 40 лет человек начинает стремительно стареть. То есть соляная кислота в желудке фактически влияет на здоровье всего организма.
Желудок, удивленный чрезмерным размножением бактерий, начинает включать защитную функцию, в результате чего появляется воспаление. Его лечат препаратами, которые еще больше угнетают выработку соляной кислоты – и круг замыкается. Человек вынужден постоянно посещать врача.
Даже изжога, которую мы привыкли считать следствием повышения количества желудочного сока, считается лишь продуктом уксуснокислого брожения.
В больном желудке начинает активно образовываться молочная кислота. Из-за невозможности желудка вырабатывать достаточное количество слизи, она повреждает стенки органа. В таких случаях ставят диагноз – гастродуоденит.
Белки и кислотность желудочного сока
Роль соляной кислоты в переваривании белков пока до сих пор невыяснена. Однако установлено, что при воспалительных заболеваниях желудка нарушается ее секреция и, как следствие, переваривание белков.
Значение белков в нашем организме трудно переоценить. Эта группа делится на множество подгрупп, каждая из которых занимается своим делом. Так, белки-гормоны управляют жизненными процессами (рост и размножение), белки-ферменты обеспечивают химические процессы (дыхание, пищеварение, метаболизм), гемоглобин насыщает клетки кислородом.
Денатурация белков (это облегчает процесс их последующего расщепления) дает возможность организму использовать по максимуму их свойства. Каждый белок состоит из аминокислот. Большинство из них синтезируется нашим организмом, но есть группа так называемых незаменимых аминокислот, которые поступают в организм только извне.
Применение
С. к. используют для получения хлоридов металлов, травления металлич. поверхностей, очистки поверхностей сосудов, нефтяных и газовых скважин от карбонатов, обработки руд, при произ-ве органич. продуктов и др. В мед. практике разбавленную С. к. применяют при заболеваниях, связанных с недостаточной кислотностью желудочного сока.
Концентрир. С. к. вызывает сильные ожоги слизистых оболочек, разрушает зубы.
Первая помощь и неотложная терапия
При ингаляционных отравлениях С. к. пострадавшего необходимо немедленно вынести на свежий воздух, дать ингаляцию кислорода. Горло следует прополоскать 2% р-ром гидрокарбоната натрия, этим же р-ром промыть глаза и нос. При затруднении дыхания закапывают по 4—5 капель 2—3% р-ра эфедрина в нос 3—4 раза в день, подкожно вводят 1 мл 0,1% р-ра атропина. В тяжелых случаях при отравлениях аэрозолем С. к. для профилактики и лечения пневмонии применяют ингаляции аэрозолей антибиотиков, назначают курс лечения антибиотиками и сульфаниламидами.
При попадании С. к. высокой концентрации на кожу необходимо немедленно обмыть кожу водой в течение 5—10 мин. (лучше 2—4% р-ром гидрокарбоната натрия); дальнейшее лечение — симптоматическое (см. Ожоги).
При поражении глаз после промывания р-ром гидрокарбоната натрия в глаза закапывают по 1 капле 2% р-ра новокаина или 0,5% р-ра дикаина с адреналином (1:1 000), затем в конъюнктивальный мешок закладывают стерильное вазелиновое или персиковое масло. В последующем лечение состоит в закапывании в глаза 30% р-ра альбуцида, применении гидрокортизоновой глазной мази.
При пероральных отравлениях необходимо срочно промыть желудок через зонд водой и затем провести симптоматическое лечение (см. Отравления).