Тогда что вы советуете? Сразу идти к врачу?
Да, он должен оценить все риски. Те же противодиарейные препараты по-хорошему надо принимать только после рекомендации врача. Плохими признаками указывающими на серьезные поражения кишечника являются такие симптомы, сопровождающие диарею: повышение температуры тела, кровь в стуле, ложные позывы на дефекацию, отеки ног, увеличение размеров живота. Если же у вас диарея развивается на фоне любого стресса – то есть у вас установлен диагноз синдром раздражённого кишечника – то вам тоже нужно обратиться к врачу, пусть в плановом режиме: ковид – это тоже очень большой стресс для организма.
Причины и последствия диареи
Понос у детей и взрослых могут вызвать множество причин. Вот общие факторы риска, которые провоцируют приступы диареи:
- нарушения кишечной перистальтики,
- скопление токсинов в кишечнике при инфекционных заболеваниях органов ЖКТ,
- дисбактериоз на фоне приема антибиотиков,
- ферментопатия или ферментная недостаточность,
- аутоиммунные патологии,
- индивидуальная непереносимость пищевых продуктов,
- непривычная еда и акклиматизация,
- отравления,
- переедание.
При поносе каловые массы становятся жидкими или приобретают кашицеобразную консистенцию, зловонный запах, частота стула увеличивается. Это может привести к серьезным последствиям:
- нарушению микрофлоры,
- обезвоживанию,
- снижению артериального давления,
- головокружению,
- сильной слабости.
Особенно опасна диарея для детей, поскольку у них обезвоживание наступает быстрее, чем у взрослых. Устранить проблему частого стула и восстановить организм после диареи поможет правильное лечение, поэтому нельзя пренебрегать обращением к специалисту.
Какой должна быть диета после коронавируса?
Если вы легко перенесли инфекцию и никаких осложнений со стороны ЖКТ у вас нет, то вам можно посоветовать «средиземноморскую диету». Она, кстати, подходит для всех, поскольку наиболее полноценна и согласно исследованиям продлевает жизнь. Она не требует особых ограничений и досаточно проста: половина тарелки – овощи и фрукты в любом виде, четверть – злаки (макароны, крупы и хлеб), четверть – белки (курица, рыба, яйца, кролик). Сладости и красное мясо – не чаще 2-х раз в неделю. Сосиски, колбаса и паштеты – чем реже, тем лучше.
Если осложнения со стороны ЖКТ после коронавируса всё-таки есть, то вам показано щадящее питание на время диареи: есть меньше свежих овощей и фруктов, исключить молочные продукты, а также жареную, копчёную и солёную пищу. Очень важно отметить что щадящее питание всегда временное, в современной гастроэнтерологии пожизненные диеты крайне редки, исключением пожалуй является целиакия.
Кишечное расстройство: как подобрать лекарство
Лучшее лечение — это профилактика острых кишечных инфекций. Однако несмотря на все предупреждения, с расстройством кишечника сталкивался практически каждый человек, а средства на этот случай есть в каждой домашней аптечке. Так давайте разберемся, как действуют привычные для нас таблетки, чтобы в час «икс» принять правильное лекарство.
Справка: во время болезни угнетаются основные функции кишечника: нарушается переваривание пищи и перистальтика, выработка секрета пищеварительных желез и кишечного сока. Наиболее частым проявлением кишечного расстройства является нарушение водно-электролитного баланса в кишечнике – диарея.
А теперь представьте, что ваш кишечник – это труба, которая ведет к крану на вашей кухне, с которой начались проблемы. Нормальные медленные и волнообразные движения кишечника ускоряются, вода не успевает всасываться стенками, появляется жидкий стул. Такое состояние сравнимо с протеканием крана. Нужно срочно устранить проблему, пока квартира не оказалась затопленной.
Оказываем первую помощь: активированный уголь и другие энтеросорбенты
При расстройстве кишечника первым делом применяют энтеросорбенты – активированный уголь, который имеется практически в каждой аптечке, и более современные препараты. Лекарства поглощают и связывают токсичные вещества, попавшие в желудочно-кишечный тракт и вызвавшие проблему.
Что происходит с иммунитетом при диарее?
Кишечник является важным органом иммунной системы. В нём есть лимфоидная ткань, которая воспроизводит иммунокомпетентные клетки. Эти клетки способны вырабатывать иммуноглобулины в ответ на попавшие в кишечник чужеродные антигены. Иммуноглобулины — защитные белковые молекулы, которые связывают патогены и не дают им вредить нашему организму. Эффективность действия выделяемых иммуноглобулинов зависит от времени их нахождения в кишечнике: чем дольше, тем эффективнее. Вместе с жидким стулом потеря иммуноглобулинов увеличивается, их количество для подавления инфекции может стать недостаточным.
Наверх к содержанию
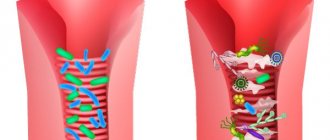
Диарея и патогены
Собственная микрофлора защищает кишечник человека от колонизации патогенными микроорганизмами1. Представители лакто- и бифидофлоры препятствуют подселению патогенов и конкурируют с ними за питательные вещества и «жилую площадь». Помимо этого, нормальная микрофлора вырабатывает активные субстанции, замедляющие рост вредных микробов2. Во время диареи скорость прохождения пищи по кишечнику увеличивается, вместе с кишечным содержимым теряются и полезные бактерии3. Патогенная флора начинает расти, поддерживать инфекционный процесс и усиливать воспаление в кишечнике.
Наверх к содержанию
Нарушения микробиоценоза кишечника у детей и его коррекция
Важнейшую роль в жизнедеятельности организма человека играет микробиоценоз кишечника — микроэкологическая система организма, которая сложилась в процессе филогенетического развития в пищеварительном канале человека. На значение микробной флоры для здорового человека впервые обратил внимание в 1907 году И. И. Мечников. Процесс взаимодействия микроорганизмов, обитающих в кишечнике, и собственно слизистой оболочки достаточно сложен и его изучению посвящено немало монографий и научных работ.
Всю микрофлору кишечника можно разделить на три группы: основная флора, среди которой наибольший интерес представляют бифидобактерии (Bifidobacterium bifidum, Bifidobacterium brevis, Bifidobacterium longum, Bifidobacterium adolescentis и др.) и лактобациллы (Lactobacillus acidophilus, Lactobacillus fermentum, Lactobacillus brevis, Lactobacillus lactis и др.), сопутствующая флора, представленная в основном кишечными палочками с типичными биологическими свойствами и энтерококками (Enterococcus fecalis, Enterococcus faecium), и остаточная флора, которая представлена условно-патогенными бактериями семейства энтеробактерий: клебсиеллами, цитробактерами, протеями и др., стафилококками (Staphylococcus epidermidis, Staphylococcus saprophyticus) и дрожжеподобными грибами.
Одна из основных функций нормальной микрофлоры — защитная, так как бактерии-симбионты человека обладают выраженной антагонистической активностью по отношению к патогенным и условно-патогенным микроорганизмам. Так, например, бифидобактерии образуют в процессе своей жизнедеятельности молочную, уксусную, муравьиную и янтарную кислоты, что снижает рН среды кишечника и препятствует колонизации его посторонними микроорганизмами, попавшими сюда извне. Лактобациллы в процессе брожения молочной кислоты образуют антибиотические вещества — лактолин, лактоцидин, ацидофилин. Полноценная кишечная палочка способна к синтезу колицинов и микроцинов — специфических белков, обладающих антибактериальной активностью. Таким образом, представители основной и сопутствующей микрофлоры кишечника тормозят рост и размножение гнилостных и патогенных микроорганизмов — кишечных палочек с атипичными биологическими свойствами, клебсиелл, протеев, некоторых видов сальмонелл и шигелл, золотистого стафилококка.
Присутствие микробных ассоциаций в кишечнике определяет состояние синтетической функции печеночных клеток путем участия в печеночно-кишечной циркуляции важнейших компонентов желчи — солей желчных кислот, холестерина и желчных пигментов.
Участие нормальной микрофлоры кишечника в обменных процессах организма человека определяется, с одной стороны, утилизацией кишечными микроорганизмами непереваренных пищевых соединений и инактивацией биологически активных веществ, выделяющихся с пищеварительными соками, а с другой стороны, синтезом представителями нормофлоры кишечника витаминов группы В, витамина К, никотиновой и фолиевой кислот, различных биологически активных соединений: экстрогенов, промазина, морфина, колхицина, диэстилбестрена, дигоксина и др.
Еще одной из важнейших функций микрофлоры организма человека является участие в формировании иммунобиологической реактивности макроорганизма. Показано, что в результате антигенной стимуляции аутофлорой иммунной системы в организме человека создается и поддерживается общий пул иммуноглобулинов.
Известно, что энтероциты кишечника, основная функция которых всасывать питательные вещества из просвета кишки, не всегда получают полноценное питание от самого организма, через базальную мембрану, к которой они фиксированы. Это объясняется тем, что процессы инфузии в клетках эпителия кишечника протекают как бы только в одну сторону — от верхушки энтероцитов к базальной мембране, а не наоборот. Вот и приходится энтероцитам «добывать пропитание» для себя также из просвета кишки. Эта питательная субстанция для клеток эпителия, называемая бутиратом, состоит из различных продуктов жизнедеятельности симбионтной флоры, обитающей в просвете кишки, которая представляет собой смесь короткоцепочечных жирных и летучих кислот, моносахаров и липидов.
При подавлении симбионтной флоры условно-патогенными и патогенными бактериями, выработка бутирата снижается или прекращается вовсе, энтероциты в состоянии дефицита питания атрофируются и процессы пищеварения нарушаются. Известны работы, описывающие механическое повреждение условно-патогенной кишечной палочкой в таких условиях кишечных ворсинок. Эшерихии буквально «обгрызают» энтероциты, ослабленные из-за дефицита питания.
Таким образом, нормальная микрофлора с ее специфическими функциями — защитной, обменной и иммуноиндуцирующей, питательной — определяет микробную экологию пищеварительного тракта и участвует в поддержании гомеостаза макроорганизма. Нарушение любой из функций приводит к нарушению различных видов метаболизма, возникновению дефицита микронутриентов: витаминов, микроэлементов, минеральных веществ в организме человека, снижению его иммунного статуса.
Нарушения состава и количественного соотношения в микробиоценозе кишечника возникают от разнообразных причин: характера питания, возраста, проведения антибактериальной, гормональной или лучевой терапии, наличия хронических заболеваний желудочно-кишечного тракта, измененной иммунобиологической реактивности организма и состояния окружающей среды и наступают задолго до клинических проявлений — они служат предвестником отклонений в клинико-физиологическом статусе организма. Эти изменения нормальной микрофлоры получили название дисбактериоза или дисбиоза, который со временем проявляет себя клиническими местными симптомами, а затем и общими нарушениями, которые отягощают течение различных заболеваний человека и затрудняют его лечение. Преобладание роста каких-либо представителей микробной флоры кишечника, происходящее в силу перечисленных выше обстоятельств, получило название синдрома избыточного бактериального роста (СИБР) и является одним из вариантов проявления дисбактериоза. Следовательно, вместе с лечением человека от той или иной болезни надо оздоровить и его кишечник.
Для характеристики дисбактериоза кишечника в разные годы были предложены различные классификации, учитывающие вид микробной флоры, тип нарушений, тяжесть течения и клинические формы и т. д., но ни одна из известных на сегодня классификаций не может полностью удовлетворить врача при решении практических задач нормализации и коррекции микробиоценоза кишечника и рационально построить лечение и профилактику дисбактериоза у пациентов. Мы использовали классификацию, С. Д. Митрохина (1998), которая позволяет охарактеризовать степени тяжести дисбактериоза толстой кишки с позиций оптимизации современных подходов к лечению и профилактике дисбактериозов.
Микроэкологическая классификация степеней тяжести дисбиоза кишечника (С. Д. Митрохин, 1998)
I степень тяжести — увеличено или уменьшено общее количество кишечных палочек. Кишечные палочки с атипичными биологическими свойствами отсутствуют. Количество бифидобактерий и лактобацилл не изменено. Изменения в общих показателях микробного метаболитного паспорта фекалий характерны лишь в отношении пула летучих жирных кислот, содержания фенилпропионовой кислоты, скатола и метиламина. Общее содержание летучих жирных кислот у больных с I степенью тяжести дисбактериоза может быть меньшим или большим аналогичного у здоровых лиц. Будет снижено содержание скатола. Напротив, содержание фенилуксусной кислоты и метиламина будет повышено. Будут отмечатся изменения удельного веса щавелевоуксусной кислоты в профиле других карбоновых кислот (ДКК). Дисбактериоз латентный, компенсированный, кишечные дисфункции не регистрируются.
II степень тяжести — незначительно снижено количество бифидобактерий и лактобацилл. Наблюдаются количественные и качественные (появление форм с атипичными биологическими свойствами) изменения кишечных палочек. Высеваются в умеренном количестве условно-патогеннные кишечные микроорганизмы. Отмечаются изменения как в общих, так и в специфических показателях микробного метаболитного паспорта фекалий. Что выражается в снижении величины экскреции с фекалиями фенольных соединений: п-крезола и индола. В десятки раз уменьшается количество скатола в испражнениях. Обратная картина наблюдается в отношении фенилпропионовой кислоты, количество которой на порядок превышает таковое у здоровых лиц. Профиль фенольных соединений (ФС) также меняется: удельный вес индола возрастает более чем в 2 раза, несколько снижался удельный вес п-крезола и более чем в десять раз снижен удельный вес скатола. В целом экскреция с фекалиями карбоновых и ароматических аминокислот, фенольных и индольных соединений (за исключением фенилаланина) при II степени тяжести дисбиоза снижена. Снижается экскреция с фекалиями гистамина и серотонина. Изменен аминный профиль: удельный вес гистамина и серотонина ниже, удельный вес представителя простых аминов — метиламина выше. Дисбактериоз локальный (местный), субкомпенсированный, кишечные дисфункции, как правило, не наблюдаются.
III степень тяжести — существенное снижение количества бифидобактерий (105–106) в сочетании со снижением количества лактобацилл и резким изменением типичных свойств кишечных палочек (значительное преобладание гемолитических, лактозонегативных форм). Значительное увеличение количества условно-патогенных бактерий с патогенными свойствами (гемолитических форм) и патогенных дрожжеподобных грибов (родов Candida, Geotrichum и др.). Характерны еще более выраженные изменения как в общих, так и в специфических показателях микробного метаболитного паспорта фекалий. Снижена величина экскреции с фекалиями фенольных соединений: п-крезола и индола. В фекалиях практически отсутствует скатол. Напротив, содержание фенилпропионовой кислоты в каловых массах резко увеличивается. Профиль ФС меняется таким образом, что существенно увеличивается удельный вес индола и значительно снижается удельный вес п-крезола. Существенно изменяется величина экскреции аминов: содержание в фекалиях гистамина и серотонина может быть выше или ниже по сравнению с нормой (зависит от нозологической формы основного заболевания). Содержание карбоновых кислот в фекалиях больных с III степенью дисбиоза меняется следующим образом: резко уменьшается пул летучих жирных кислот, практически не обнаруживается щавелевоуксусная кислота и значительно возрастает экскреция с каловыми массами альфа-кетоглутаровой кислоты. Изменен профиль летучих жирных кислот. При нарушениях стула по типу диареи удельный вес уксусной кислоты ниже, удельный вес пропионовой и масляной кислот, наоборот, повышен, при констипации наблюдается противоположная картина. Отмечается снижение или увеличение удельного веса молочной и аналогичные изменения удельного веса альфа-кетоглутаровой кислот в профиле ДКК. Дисбактериоз локальный (местный), декомпенсированный, кишечные дисфункции, как правило, наблюдаются.
IV степень тяжести — резкое снижение или отсутствие бифидобактерий, значительное уменьшение количества лактобацилл, резкое уменьшение количества или отсутствие кишечных палочек с типичными свойствами, значительное возрастание количества как облигатных, так и факультативных видов (в норме не встречающихся) кишечных бактерий и дрожжеподобных грибов с патогенными свойствами. Выявляются патогенные кишечные бактерии (сальмонеллы, шигеллы, йерсинии). Качественные изменения в микробном метаболитном паспорте остаются такими же, как и при третьей степени, но их количественные характеристики еще более изменены, характерна глубокая разбалансировка биохимических регуляторных механизмов микробной экосистемы, сочетающаяся с аналогичной разбалансировкой микробной инфраструктуры кишечника. Дисбактериоз распространенный (с бактериемией), декомпенсированный (с угрозой генерализации инфекции, сепсиса или септикопиемии), наблюдаются выраженные кишечные дисфункции.
Лечением дисбиоза врачи всех уголков мира занимаются давно. В результате многолетнего кропотливого поиска наиболее действенных мер и способов к настоящему времени образовалось большое количество лекарственных препаратов и биологических активных добавок, которые в той или иной степени влияют на состояние микрофлоры и используются для восстановления нарушенного равновесия кишечной экоструктуры.
Большое разнообразие на российском рынке лекарственных средств, необходимость рационального выбора лечебных воздействий и их сочетаний убедительно свидетельствуют о необходимости некоторой систематизации и схематизации лечения дисбактериоза кишечника, не исключая при этом опыта и творческого характера в работе лечащего врача и индивидуального подхода к коррекции и профилактике дисбактериоза кишечника.
В настоящее время разработаны следующие основные принципы комбинированной коррекции микроэкологического дисбаланса кишечника:
- коррекция моторно-секреторной функции желудочно-кишечного тракта, включающая ферментотерапию, поливитаминотерапию, назначение спазмолитиков, антидиарейных, желчегонных и стимулирующих регенеративные процессы препаратов;
- энтеросорбция и энтеропротекция, заключающаяся в назначении энтеросорбентов, выводящих из организма как патогенные микроорганизмы, так и продукты их жизнедеятельности;
- селективная деконтаминация патогенной и условно-патогенной микрофлоры кишечника, проводимая на основе назначения бактериофагов, кишечных антисептиков, фитонцидов и антибактериальных препаратов;
- коррекция нормальной микрофлоры кишечника с помощью различных пробиотиков;
- функциональное питание, заключающееся в употреблении кисломолочных и других вариантов продуктов с включением в них в качестве активного действующего начала бифидобактерий (фруктовые и овощные соки, жевательные резинки, мороженое, кондитерские изделия, салаты, сыры, сметана, кефир, масло, крем, творог, десерты и др.). В настоящее время бифидобактерии включены в состав более 70 различных продуктов питания.
Чрезвычайно важными элементами лечения и профилактики дисбактериоза кишечника также являются следующие моменты:
- санитарно-просветительная работа с пациентами и их родственниками о роли микрофлоры и необходимости ее коррекции;
- длительное сотрудничество врача и пациента;
- соблюдение диетического режима и функционального питания;
- применение медикаментозных и немедикаментозных методов лечения и профилактики дисбактериоза кишечника.
При построении тактики рационального, индивидуального лечения и профилактики дисбактериоза кишечника, особенно у детей различного возраста, у которых процессы формирования собственной экосистемы продолжаются до 10–12 летнего возраста, врачу необходимо решить следующие задачи:
- нормализация работы кишечника (первый принцип комбинированной терапии);
- создание условий, способствующих более благоприятному развитию собственной флоры (аутофлоры) организма (второй принцип комбинированной терапии);
- санация кишечника от патогенной и условно-патогенной флоры (третий принцип комбинированной терапии);
- длительное интермиттирующее лечение (пульс-терапия) при III–IV степени тяжести дисбактериоза не менее 6 месяцев (четвертый принцип комбинированной терапии);
- сохранение и поддержание микробной экологии кишечника (пятый принцип комбинированной терапии).
Для нормализации работы кишечника используются и индивидуально подбираются средства с учетом нарушений функций толстой кишки и особенностей действия препаратов с наиболее вероятным воздействием на причину имеющегося нарушения работы кишечника (констипация, диарея) и адсорбирующих свойств, а также ферментативной недостаточности. В последнее время уделяется много внимания проблемам дисбиоза, избыточному бактериальному росту, обусловленному самыми разными факторами, — нарушение макро- и микроэкологии кишечника на фоне антибиотикотерапии, химиотерапии, пищевых отравлений и пр. В этих работах довольно подробно останавливаются и на этиопатогенетических механизмах развития дисбиоза и его последствий и на методах лечения с использованием кишечных антисептиков, антибиотиков и различных моно- или мультиштаммовых пробиотиков. К пробиотикам относятся биологические активные средства, содержащие колонии живых или лиофилизированных микроорганизмов, основная функция которых заместительная, то есть при их приеме необходимо заместить патогенную и условно-патогенную флору штаммами специально выведенных культур бифидо-, лакто- и других бактерий, сходных по своим свойствам со штаммами, обитающими в кишечнике человека. Особенно актуально звучит тема заместительной терапии именно для детей различного возраста. Как уже было сказано, кишечная микрофлора начинает формироваться с первого дня жизни ребенка и заканчивается, по данным разных авторов, к 10–12 годам. Сформированные к этому возрасту соотношения различных групп бактерий индивидуальны для каждого человека и сохраняются в его кишечнике на протяжении практически всей жизни с небольшими колебаниями, зависящими от внешних и внутренних (возрастных) факторов. И если у взрослого человека происходит, по каким-либо причинам, нарушение экосистемы, то в этом случае можно с меньшей оглядкой назначать больным людям антибиотики широкого спектра действия, с последующим курсом пробиотиков. Смысл такого лечения заключается в уничтожении с поверхности кишечника болезнетворных микроорганизмов. Конечно же, в этот период значительно страдает и симбионтная микрофлора. Однако под прикрытием пробиотиков, которые, как правило, назначаются после окончания антибиотикотерапии (а современные виды пробиотиков, имеющих устойчивые к некоторым антибиотикам штаммы, — и во время проведения антибиотикотерапии) в кишке раньше или позже, в зависимости от индивидуальных особенностей организма, поверхность слизистой оболочки кишки вновь заселят те первые «родные» штаммы симбионтов, которые заселились в организме человека при формировании биоценоза в первое десятилетие жизни макроорганизма. Отдельные их представители в любом случае выживут, даже под воздействием антибиотикотерапии, и дадут впоследствии рост новым колониям, которые под «прикрытием» пробиотических штаммов разовьются, и колонизируют всю поверхность слизистой оболочки. А штаммы пробиотиков, являющиеся проходной флорой, покинут организм. Транзиторность нахождения пробиотических микроорганизмов в кишечнике подтверждена исследованиями, которые оценивали длительность их выявления в стуле. По результатам этих работ, уже через 1–4 недели после окончания приема пробиотического средства данные штаммы не определялись в стуле (Ciorba, 2010). Другое дело обстоит с детьми, у которых собственная экосистема кишечника еще не сформировалась окончательно, хотя, конечно, основное соотношение микрофлоры уже определяется к концу первого года жизни. Назначение детям антибиотиков для санации кишечника может пагубно сказаться на дальнейшем формировании нормальной микрофлоры, и в этом случае пробиотики, пусть даже и содержащие нормальные бифидо- и лактобактерии и симбионтные энтерококки, могут создать конкуренцию «родным» штаммам кишечника. Назначение антибактериальной терапии чревато, особенно у детей, возможным быстрым развитием псевдомембранозного колита с преобладанием развития Clostridium difficile. В таком случае, по возможности, детям лучше назначать не антибиотики, а кишечные антисептики, например, нитрофуранового ряда, которые «мягче» действуют на микрофлору, подавляя рост преимущественно аэробных условно-патогенных и патогенных штаммов микроорганизмов. Но для скорейшего восстановления микроэкосферы не всегда бывает достаточно этих антисептиков, пусть даже и неагрессивных и мягко действующих. В настоящее время для детского возраста разработаны специальные наборы штаммов, вошедшие в прописи различных препаратов, которые направлены на скорейшее восстановление естественной микрофлоры ребенка. Однако и они не являются идеальным средством для стимуляции роста собственных, еще не окрепших колоний симбионтных микроорганизмов. В этом случае как раз для стимуляции роста симбионтной флоры бифидо- и лактобактерий и энтерококков и в первую очередь для стимуляции роста первичных, «естественно» заселенных штаммов рекомендуется использовать средства, являющиеся экстрактом жизнедеятельности симбионтной флоры. Т. е. по сути дела прообразом того бутирата, который является питательной средой для энтероцитов. К таким препаратам относится Хилак форте, являющийся метаболическим пробиотиком. Препарат представляет собой прозрачную светло-желтую или желто-коричневую жидкость с характерным кисловатым запахом. В состав препарата входят беззародышевые водные субстраты биосинтетических продуктов бактериального метаболизма четырех видов микроорганизмов, присутствующих в нормальной микрофлоре кишечника: Escherichia coli, Enterococcus faecalis, Lactobacillus acidophilus и Lactobacillus helveticus. Благодаря наличию в препарате естественных продуктов жизнедеятельности бактерий, аналогичных тем, которые имеются в просвете кишки при нормальной микрофлоре, он способствует поддержанию физиологических функций слизистой оболочки кишечника и его микробной экологии. Создает благоприятные условия, обеспечивающие питание ослабленных или поврежденных энтероцитов, восстанавливая тем самым цитомукопротективную способность слизистой оболочки. Ускоряет развитие нормальной кишечной микрофлоры, создавая оптимальную экологическую среду с определенным соотношением кислот. Препарат назначается детям в виде приема 20–40 капель 3 раза в день до или во время еды. Для младенцев дозировка составляет 15–30 капель 3 раза в день. Рекомендуется интермиттирующий ритм по 10–15 дней с перерывами 1–2 месяца.
Возможно, что при приеме препарата не только и не столько восстанавливается кислотность среды в тонкой кишке (так как доза приема препарата очень небольшая), но запускаются некоторые триггерные механизмы, регулирующие процесс цитомукопротекции и влияющие на микроэкологическую систему в кишечнике. Это одно из предположений, научные исследования над которым продолжаются до последнего времени. Однако налицо клиническая эффективность при приеме Хилака форте в случае развития дисбиоза у взрослых и детей различного возраста. На фоне приема этого препарата происходит скорейшее восстановление микроэкологического баланса в кишечнике и исчезают клинические проявления, сопровождающие дисбактериоз, — боли в животе, метеоризм и констипация, о чем свидетельствуют проведенные клинические исследования в разных странах.
Известно, что важную роль в положительном действии пробиотических микроорганизмов выполняют не сами бактериальные клетки, а их метаболиты (Н. И. Урсова, 2013). В этом отношении Хилак форте может быть более предпочтителен, чем лиофилизированные формы различных пробиотических препаратов, которым требуется 8–10 часов для активации и начала выработки продуктов метаболизма (С. К. Аджигайтканова, 2007). Этот вопрос приобретает особенную важность в случае диареи, которая часто сопровождает нарушения микрофлоры. Дело в том, что время нормального транзита содержимого по кишечнику как у взрослых, так и у детей позволяет лиофилизированным пробиотикам пройти активацию. Однако общекишечный транзит при диарее может быть значительно ускорен. Так, по результатам исследования у детей 3–18 месяцев с диареей время общекишечного транзита (Total gut transit time) составляло всего лишь 5 часов (Roy, 1991).
Важным вопросом является коррекция нарушений микрофлоры при приеме антибактериальной терапии. Препараты на основе метаболитов полезных бактерий, таких как Хилак форте, не содержат живых микроорганизмов. Поэтому их применение совместно с антибиотиками может быть более предпочтительным, т. к. последние никоим образом напрямую не уменьшают их эффективность.
В любом случае, для того чтобы не нарушить хрупкую микроэкологическую структуру кишечника или восстанавливать ее после каких-либо агрессивных воздействий, необходимо использовать весь арсенал средств, доступных в настоящее время в медицине в целом и в детской гастроэнтерологии в частности, сочетающий использование наряду с пробиотиками средств, способствующих скорейшей адаптации колоний симбионтных бактерий на слизистой оболочке кишечника, — продуктов естественного метаболизма микроорганизмов, к которым относится и Хилак форте.
В таблице приводятся биохимические критерии состояния микробной экологии кишечника, полученные при обследовании практически здоровых людей — доноров крови [37].
Литература
- Куваева И. Б., Ладодо К. С. Микроэкологические и иммунные нарушения у детей: диетическая коррекция. М., 1991.
- Запруднов А. М., Мазанкова Л. Н. Микробная флора кишечника и пробиотики. М., 1999.
- Коршунов В. М., Володин Н. Н., Ефимов Б. А. и др. Микроэкология желудочно-кишечного тракта. Коррекция микрофлоры при дисбактериозах кишечника. М., 1999.
- Аджигайтканова С. К. Подходы к медикаментозному лечению дисбактериоза кишечника // Болезни органов пищеварения. Приложение РМЖ. 2007. № 2. С. 73–76.
- Урсова Н. И., Римарчук Г. В., Щеплягина Л. А., Савицкая К. И. Современные методы коррекции дисбиоза кишечника у детей (учебное пособие). М., 2000.
- Урсова Н. И. Актуальные и нерешенные проблемы пробиотикотерапии // Лечащий Врач 2013. № 8. С. 60–65.
- Петровская В. Г., Марко О. П. Микрофлора человека в норме и патологии. М., 1976.
- Тимофеева Г. А., Цинзерлинг А. В. Острые кишечные инфекции у детей. Л., 1984.
- Покровский В. И., Гордиенко С. П., Литвинов В. И. (ред.) Иммунология инфекционного процесса. М., 1994.
- Шендеров Б. А. Медицинская микробная экология и функциональное питание. М., 1998.
- Шадрин С. А. Дисбактериоз кишечника у детей. Краснодар, 1999.
- Мухина Ю. Г. Особенности микроэкологии пищеварительного тракта у детей. К проблеме дисбактериоза // Детская больница. 2000, № 2.
- Rosebury T. Microorganisms indigenous to man. N.Y., 1962.
- Collins M. D. Probiotics, prebiotics, and synbiotics: approaches for modulating the microbial ecology of the gut // Am. J. Clin. Nutr. 1999; 69 (Suppl.): S1052–1057.
- Vanderhoof J. A., Whitney D. B., Antonson D. L. et al. Lactobacillus GG in prevention of antibiotic-associated diarrhea in children // J. Pediatr. 1999; 135: 564–568.
- Митрохин С. Д., Щербаков П. Л., Бредихина Н. А., Елизаветина Г. А., Иваников И. О., Минушкин О. Н. Лечение и профилактика дисбактериоза (дисбиоза) кишечника на современном этапе. Практические рекомендации. М., 1999, 48 с.
- Урсова Н. И. Дисбактриозы кишечника в детском возрасте: инновации в диагностике, коррекции, профилактике. М., 2013. 328 с.
- Парфенов А. И. Энтерология. М.: МИА, 2009. 880 с.
- Rambaud J.-C. et al. Gut Microflora. Paris: John Libbey eurotext, 2006. P. 247.
- Amandine Everarda, Clara Belzerb, Lucie Geurtsa et. al. Cross-talk between Akkermansia muciniphila and intestinal epithelium controls diet-induced obesity www.pnas.org/cgi/doi/10.1073/pnas.1219451110 PNAS Early Edition.
- Emmanuelle Le Chatelier, Trine Nielsen, Junjie Qin et al. Richness of human gut microbiome correlates with metabolic markers // 038/nature12506.
- Shuiming Xiao, Na Fei, Xiaoyan Pang et al. A gut microbiota-targeted dietary intervention for amelioration of chronic inflammation underlying metabolic syndrome // FEMS Microbiol& Ecol. 2013, 1–11.
- Лечение и профилактика дисбактериоза (дисбиоза) кишечника на современном этапе. Практические рекомендации.
- Prakash S., Tomaro-Duchesneau C., Saha S., Cantor A. The gut microbiota and human health with an emphasis on the use of microencapsulated bacterial cells // J. Biomed. Biotechnol. 2011: 981214. [email protected] Jul 2: 981214.
- Reid G., Gaudier E., Guarner F. et al. Responders and non-responders to probiotic interventions: how can we improve the odds? // Gut Microbes. 2010; 1: 200–204.
- Rosenberg E., Zilber-Rosenberg I. Symbiosis and development: the hologenome Concept // Birth Defects Res.C. Embryo.Today. 2011; 93: 56–66.
- Roy S. K. et al. Persistent diarrhea: total gut transit time and its relationship with nutrient absorption and clinical response // J Pediatr Gastroenterol Nutr. 1991, Nov; 13 (4): 409–414.
- Tlaskalova-Hogenova H., Stepankova R., Kozakova H. et al. The role of gut microbiota (commensal bacteria) and the mucosal barrier in the pathogenesis of inflammatory and autoimmune diseases and cancer: contribution of germ-free and gnotobiotic animal models of human diseases // Cell Mol.Immunol. 2011; 8: 110–120.
- Xue H., Sawyer M. B., Wischmeyer P. E., Baracos V. E. Nutrition modulation of gastrointestinal toxicity related to cancer chemotherapy: from preclinical findings to clinical strategy // JPEN J. Parenter.Enteral Nutr. 2011; 35: 74–90.
- Whelan K., Schneider S. M. Mechanisms, prevention, and management of diarrhea in enteral nutrition // Curr. Opin. Gastroenterol. 2011; 27: 152–159.
- Delzenne N., Cherbut C., Neyrinck A. Prebiotics: actual and potential effects in inflammatory and malignant colonic diseases // Curr. Opin. Clin. Nutr. Metab Care. 2003; 6: 581–586.
- Cabre E., Gassull M. A. Nutritional and metabolic issues in inflammatory bowel disease // Curr. Opin. Clin. Nutr. Metab Care. 2003; 6: 569–576.
- Meier R., Burri E., Steuerwald M. The role of nutrition in diarrhoea syndromes // Curr. Opin. Clin. Nutr. Metab Care. 2003; 6: 563–567.
- Matthew Ciorba. A Gastroenterologist’s Guide to Probiotics // Clin Gastroenterol Hepatol. 2012; 10 (9): 960–968.
- Reid G., Sanders M. E., Gaskins H. R. et al. New scientific paradigms for probiotics and prebiotics // J. Clin. Gastroenterol. 2003; 37: 105–118.
- Holmes S. Are probiotics and other functional foods the medicines of the future? // Prof. Nurse. 2003; 18: 627–630.
- Митрохин С. Д., Ардатская М. Д., Никушкин Е. В. и др. Комплексная диагностика, лечение и профилактика дисбактериоза (дисбиоза) кишечника в клинике внутренних болезней. Методические рекомендации/Под ред. О. Н. Минушкина. М.: Медицинский центр УД Президента РФ, 1997. 45 с.
П. Л. Щербаков, доктор медицинских наук, профессор
ГБУЗ МКНЦ ДЗМ, Москва
Контактная информация
Диета при нарушении микрофлоры
Для лечения легкой формы дисбактериоза бывает достаточно назначение специальной диеты. Рацион питания должен содержать достаточное количество белков, жиров, углеводов. За пол часа рекомендуется пить стакан теплой воды. Важно, чтоб в рацион питания входили следующие вещества:
- Лакто- и бифидобактерии. Они содержатся в кисломолочных продуктах, в сливочном масле;
- Клетчатка содержится в овощах, фруктах;
- Аминокислоты глутамин и аргинин, источником которых являются мясо курицы, говядина, орехи, рыба, кисломолочные продукты, горох.
Необходимо избегать жирных, жареных, копченых, острых блюд.
Диарея
Диарея (понос) — это патологическое состояние, являющееся клиническим симптомом различных заболеваний желудочно-кишечного тракта, эндокринной системы, а также других патологий. Основным признаком диареи является учащенное опорожнение кишечника, чаще трех раз в сутки, с выделением водянистого или кашицеобразного стула. По характеру течения различают острую и хроническую диарею.
Острая диарея длится не больше трех недель и часто имеет инфекционную природу. Хроническая диарея характеризуется длительным течением (больше 3-х недель), чаще имеет неинфекционную природу, ее может вызывать множество причин.
Основные симптомы
При острой диарее
- жидкий, учащенный стул;
- общее недомогание, боли и спазмы в животе;
- лихорадка;
- иногда рвота;
- присутствие слизи и крови в кале;
- частые болезненные позывы к дефекации.
При хронической диарее
- жидкий, учащенный стул;
- метеоризм, урчание, переливание в кишках;
- боли в животе;
- снижение веса;
- нарушение всасывания и обмена веществ;
- витаминно-минеральная недостаточность.
Механизм развития заболевания
Острую диарею могут вызвать попавшие в организм человека бактерии или вирусы, они воздействуют на клетки слизистой оболочки кишечника, вызывая повышенное выделение электролитов и воды, что приводит к частому и водянистому стулу. Кроме того острая диарея может возникать из-за аллергии на определённые продукты питания, при отравлениях и приеме определенных лекарств. Лекарственные поражения кишечника (прием антибиотиков, НПВС, злоупотребление слабительными) могут вызвать острую диарею, которая постепенно прекращается после отмены препаратов.
Для возникновения хронической диареи существуе несколько механизмов. Они могут приводить к образованию в кишечнике излишков воды, кишечных ферментов, осмотически активных веществ, слизи и гноя в случае воспаления и нарушению перистальтики кишечника.
Хроническая диарея может сопровождать следующие заболевания
- синдром раздраженного кишечника;
- хронические заболевания кишечника, среди них, болезнь Крона, язвенный колит и микроскопический колит;
- нарушение всасывания (синдром мальабсорбции) при целиакии, лактазной недостаточности и других заболеваниях;
- эндокринные заболевания;
- онкологические заболевания желудочно-кишечного тракта;
- аутоиммунные заболевания;
- хронический панкреатит и болезни гепатобилиарной системы.
Кроме того хроническую диарею может вызвать длительный бесконтрольный прием слабительных средств.
Когда необходимо обратиться к врачу?
При острой диарее вовремя оказанная помощь врача обеспечит быстрое выздоровление и отсутствие осложнений, срочная медицинская помощь необходима, если у больного наблюдаются
- высокая температура;
- сильная боль в животе, присутствие крови в стуле;
- признаки обезвоживания;
- симптомы не улучшаются в течении суток или становиться хуже;
- диарея появляется после путешествия в другие страны.
Хроническая диарея обязательно требует консультации гастроэнтеролога, потому что может являться симптомом опасных заболеваний желудочно-кишечного тракта и других органов, а также наносит вред организму, вызывая недостаток витаминов, минералов и значительно ухудшает качество жизни.
Осложнения
При острой диарее может развиться интоксикация, дегидратация, метаболический ацидоз и судорожный синдром (при дефиците кальция, магния, калия). Длительная хроническая диарея приводит к гиповитаминозу, анемии, потере веса, нервным расстройствам.
Что же такое диарея?
Диарея — это учащение и разжижение стула, обычно связанное с нарушением пищеварительного процесса. Но как понять, что есть «часто», а что нет? И какая консистенция стула соответствует норме?
Для каждого возраста — свои цифры.
Нормы стула у детей разного возраста1.
- До 5 дня от рождения: меконий и переходный стул (под меконием понимают все содержимое кишечника ребенка до первого прикладывания к груди). Стул в этом возрасте — это густая вязкая масса темно-оливкового цвета.
- С 5 дня до года: обычные испражнения, кал в виде жидкой сметаны золотисто-желтого цвета с кисловатым запахом. Частота 5–7 раз в сутки в первом полугодии и 2–3 раза в сутки во втором полугодии жизни.
- После года (при введении в рацион ребенка всех продуктов прикорма) стул становится оформленным, приобретает коричневую окраску и характерный каловый запах. Частота должна быть не реже 1 раза в сутки.