Причины рака желчных протоков и факторы риска
К сожалению, несмотря на многолетнее изучение, точные причины развития данного типа рака неизвестны. Существует ряд факторов, которые могут спровоцировать развитие заболевания. К ним относят:
- склерозирующий первичный холангит — это хроническое заболевание неясной этиологии;
- болезнь Кароли — врожденная патология, при которой происходит образование большого количества внутрипеченочных кист;
- гепатоз печени;
- аденомы;
- сахарный диабет;
- паразитарные болезни печени;
- работа на вредном производстве;
- ВИЧ-инфекция;
- синдром Линча — это наследственная патология, которая повышает риск развития онкологических заболеваний органов пищеварения;
- гепатит В, С;
- болезнь Крона — тяжелое хроническое заболевание, при котором наблюдается воспаление слизистых оболочек пищеварительного тракта;
- цирроз печени;
- вредные привычки.
Симптомы рака желчных протоков
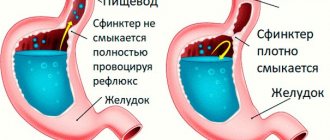
Одним из главных симптомов холангиокарциномы является механическая желтуха, которая сопровождается сильным кожным зудом. Кал у пациента обесцвеченный. Болей перед желтухой обычно нет, приступы колики случаются редко. При быстрой закупорке просвета протока опухолью перед желтухой могут возникать приступы боли.
К симптомам и признакам рака желчных протоков также относят диспепсический синдром, снижение аппетита, потерю веса. Температура тела у части пациентов остается в пределах нормы, у части повышается. В результате застоя желчи нарушается работа печени. Она при пальпации безболезненна, увеличена, имеет гладкий край.
Одним из методов дифференциальной диагностики желтух является пальпация желчного пузыря. При этом опухоль в большинстве случаев не пальпируется, так как расположена в глубине брюшной полости и имеет небольшие размеры. При сдавливании новообразованием воротной вены развивается водянка брюшной полости.
Печеночная желчь
Гепатоциты вырабатывают желчь постоянно, за сутки – 0,5–1 л. На 95–98% печеночная желчь состоит из воды и имеет щелочную реакцию. В ней содержатся соли желчных кислот, билирубин, холестерин, жирные кислоты, лецитин, ионы Na+, K+, Ca2+, Cl-, HCO3- и др. Цвет желчи обусловлен желчными пигментами (билирубин и др.), которые образуются из продуктов распада эритроцитов. Именно желчные пигменты окрашивают содержимое кишечника в коричневый цвет. Роль желчи в пищеварении сводится к эмульгированию и расщеплению жиров, что облегчает их переваривание и всасывание. Желчь усиливает перистальтику кишечника.
Стадии холангиокарциномы
Выделяют четыре стадии заболевания:
Первая стадия. Новообразование находится ниже слияния печеночных протоков, без вовлечения в патологический процесс места их соединения (конфлюенса).
Вторая стадия. Опухоль по-прежнему находится ниже слияния протоков, но распространяется на место их соединения.
Третья стадия. Новообразование продолжает разрастаться и постепенно поражает левый и правый печеночный проток.
Четвертая стадия. Поражаются сегментарные протоки.
Согласно классификации по TNM выделяют следующие типы и степени заболевания:
| T0 | Никаких видимых признаков наличия новообразования нет |
| Tis | Очаг поражения локализован в пределах желчных протоков |
| T1 | Новообразование все еще находится в пределах пораженного органа, начинает прорастать в мышечную и фиброзную ткань |
| T2 | Очаг поражения распространяется за пределы протоков, опухоль начинает прорастать в близлежащие ткани печени |
| T3 | Новообразование распространяется на печеночные артерии |
| T4 | Опухоль прорастает в протоки печени либо в патологический процесс вовлекаются близлежащие сосуды |
Прогноз выживаемости
Средняя пятилетняя выживаемость среди всех пациентов, у которых был диагностирован рак желчных протоков, составляет 8%. Такой низкий показатель связан с тем, что зачастую опухоли диагностируют на поздних стадиях, многие из них имеют «неудобное» расположение, и из-за этого их сложно удалить.
Прогноз пятилетней выживаемости на разных стадиях:
- Если опухоль находится в пределах желчных протоков и не распространяется глубже: 24%.
- Если опухоль проросла в окружающие ткани или распространилась в регионарные лимфатические узлы: 6%.
- Если имеются отдаленные метастазы: 1%.
Прогноз при опухолях желчных протоках не самый благоприятный. С такими типами рака очень сложно бороться. Но это не означает, что нужно опускать руки. В «Евроонко» применяются наиболее современные методы лечения. Мы всегда знаем, чем можно помочь, и для нас нет безнадежных больных.
Диагностика холангиокарциномы
Клинические признаки заболевания не являются специфическими, поэтому поставить диагноз рак желчных путей, основываясь только на данных анамнеза и клинического осмотра, не представляется возможным.
Пациенту дополнительно назначают следующие лабораторные и инструментальные диагностические исследования:
- Анализ крови (биохимический). Дает информацию о наличии в печени патологического процесса, но не позволяет поставить точный диагноз. В крови повышен уровень щелочной фосфатазы, билирубина. Показатели АСТ, АЛТ, а также концентрация альбуминов при данном виде онкологии обычно находятся в пределах нормы.
- Анализ на онкомаркеры холангиокарциномы. Имеет большое диагностическое значение. У пациентов выявляют антиген СА 19-9 (этот антиген также может синтезироваться при холангите и раке поджелудочной железы). Если уровень маркера у больных с хроническим холангитом сильно повышается (до 100 U/ml и больше), то, скорее всего, это говорит о развитии холангиокарциномы.
- УЗИ желчного пузыря и печени. Назначают на начальных этапах диагностики. При помощи данного метода можно обнаружить патологическое расширение протоков в некоторых местах, а также выявить новообразование большого размера.
- Допплерография сосудов печени. Выявляют нарушения кровотока в очаге поражения, но небольшие опухоли при помощи данной методики обнаружить не удается.
- КТ желчевыводящих путей. Более информативный метод диагностики. При помощи КТ можно увидеть опухоли небольшого размера, диагностировать увеличение регионарных лимфоузлов.
- МСКТ. Определяют степень закупорки желчевыводящих путей.
- ПЭТ КТ. Усовершенствованная методика. С ее помощью можно увидеть новообразования узлового типа размером менее одного сантиметра. Но инфильтрационные формы заболевания при помощи данной методики выявить сложно.
- Эндоскопическая ретроградная холецистография. Используется для уточнения диагноза. С ее помощью можно точно определить места закупорки желчных протоков и взять образец тканей для проведения гистологического исследования.
- МРТ. На сегодняшний день является наиболее информативным методом диагностики онкологических патологий желчных протоков и печени. При проведении данного исследования не используются контрастные вещества, метод неинвазивный, поэтому безопасный для здоровья пациента. На МРТ можно увидеть сосуды и желчные протоки в трехмерном изображении, правильно оценить стадию болезни, выявить новообразования небольших размеров, определить тактику дальнейшего лечения и дать прогноз.
Диагностика и лечение функциональных расстройств билиарного тракта
Желчный капилляр – начальная часть желчевыделительной системы – образован внешней поверхностью апикальной части цитоплазматической мембраны смежных гепатоцитов и плотными контактными комплексами, расположенными в местах соприкосновения гепатоцитов. Каждая печеночная клетка участвует в образовании нескольких желчных канальцев. На периферии дольки желчные канальцы сливаются во внутридольковые, которые, выходя в междольковую соединительную ткань, переходят в междольковые канальцы. Далее междольковые канальцы, сливаясь, образуют междольковые протоки 1–го и 2–го порядка, которые выстланы призматическим эпителием, и, наконец, формируются крупные печеночные протоки, выходящие из печени. Прямым продолжением внутрипеченочных протоков являются желчевыводящие пути: правый и левый печеночные протоки, общий печеночный проток. Пузырный проток, отводящий желчь из желчного пузыря, и общий печеночный проток, соединившись, образуют общий желчный проток. Регуляция тока желчи осуществляется несколькими сфинктерами. В общем желчном протоке расположен сфинктер Мирицции. В месте перехода шейки пузыря в пузырный проток мышечные волокна принимают циркулярное направление, формируя сфинктер протока желчного пузыря (Люткенса). Основная роль в регуляции желчевыделения принадлежит сфинктеру Одди, который представлен сфинктерами общего желчного протока, фатерова соска и главного протока поджелудочной железы. Сфинктер общего желчного протока состоит из циркулярных и продольных мышечных волокон. На всем протяжении циркулярный мышечный слой сфинктера Одди независим от мускулатуры стенки двенадцатиперстной кишки. Циркулярные мышечные волокна сфинктера общего желчного протока начинаются в панкреатической его части, а затем окружают интрамуральную часть общего желчного протока и переходят на ампулу. Продольные мышечные волокна сфинктера общего желчного протока располагаются как в восходящем, так и нисходящем направлениях. При этом восходящие волокна окружают наддуоденальную часть и представляют собой продолжение продольного слоя мускулатуры двенадцатиперстной кишки. Нисходящие волокна независимы от мускулатуры двенадцатиперстной кишки. Панкреатический проток у места слияния с общим желчным протоком окружен циркулярными, полуциркулярными и продольными гладкомышечными волокнами. Наружный продольный слой представлен волокнами, берущими начало в мускулатуре двенадцатиперстной кишки. Циркулярные и полуциркулярные волокна располагаются во внутреннем слое и принадлежат самому протоку. При наличии сфинктерных волокон ампулы фатерова соска они располагаются неравномерно: имеется их скопление у основания соска (сфинктер основания соска) и в его устье (сфинктер устья фатерова соска). Таким образом, понятие «сфинктер Одди» включает в себя ряд сфинктеров, расположенных в области холедохо–панкреатодуоденального соустья, а именно сфинктер общего желчного протока, сфинктер фатерова соска (сфинктер устья и основания соска), сфинктер главного панкреатического протока. Наиболее постоянен сфинктер общего желчного протока (100%). Наличие других сфинктеров зависит от варианта впадения общего желчного и панкреатического протоков в просвет двенадцатиперстной кишки [10]. Секреция желчи идет непрерывно, за сутки у человека ее выделяется от 0,5 до 2 л. Направление движения желчи обусловлено градиентом давления между желчным пузырем, желчными протоками и двенадцатиперстной кишкой и координированной деятельностью сфинктеров желчевыделительного аппарата. При закрытом сфинктере Мирицци, открытых сфинктерах Люткенса и Одди сокращение желчного пузыря приводит к выделению желчи в двенадцатиперстную кишку. Из печеночных протоков и общего желчного протока желчь в желчный пузырь поступает в момент закрытия сфинктера Одди (ему и принадлежит решающая роль в создании градиента давления). Сфинктер Одди вне пищеварения закрыт не всегда, и небольшие порции желчи постоянно поступают в двенадцатиперстную кишку. После окончания пищеварительной фазы желчь поступает в желчный пузырь в течение 3 и более часов. Вне пищеварения давление желчи в общем желчном протоке составляет 60–185 мм вод.ст. Во время еды при сокращении желчного пузыря давление поднимается до 150–260 мм вод.ст., что обеспечивает выход желчи в двенадцатиперстную кишку, где давление ниже. При резком повышении давления в билиарной системе (более 300 мм вод.ст.) может прекратиться секреция желчи печенью. При давлении около 280–300 мм вод.ст. обычно появляется боль и в крови повышается уровень щелочной фосфатазы и лейцинаминопептидазы вследствие проникновения желчи в пространство Диссе, а оттуда в синусоиды. Основной объем желчи выделяется после приема пищи. Натощаковое желчевыделение составляет около 20–30% постпрандиального, оно происходит синхронно с фазами сокращения желудка и двенадцатиперстной кишки и предотвращает чрезмерное сгущение желчи. В физиологических условиях желчь в желчном пузыре неоднородна, и разница в разных слоях может достигать 2,5 раза (это создает феномен «слоистой» желчи). Большинство исследователей считают, что внепеченочные желчные пути никогда не находятся в покое и их активная перистальтика рассматривается с точки зрения регуляции тока желчи. Тонус двенадцатиперстной кишки влияет на выход желчи, причем установлено, что поступление кислого химуса в кишку и раздражение большого дуоденального соска могут вызвать его спазм на 4–10 и более минут. Двигательная реакция желчного пузыря и сфинктера Одди существенно зависит от количества и качества пищи, а также от эмоциональных влияний [5,8]. Работа всей билиарной системы строго координирована. Это обеспечивается как нервной, так и гуморальной регуляцией. Двигательная иннервация осуществляется парасимпатической и симпатической нервной системой. Нервные сплетения имеются во всех слоях желчевыводящей системы. Чувствительные волокна желчного пузыря способны воспринимать только растяжение. Показано, что умеренное раздражение блуждающего нерва вызывает координированную активность желчного пузыря и сфинктеров, а сильное раздражение – спастическое сокращение с задержкой эвакуации желчи. Раздражение симпатического нерва способствует расслаблению желчного пузыря. Из гастроинтестинальных гормонов ведущая роль принадлежит холецистокинину – панкреазимину (ХЦК–ПЗ), гастрину секретину, мотилину, глюкагону. Максимальный эффект оказывает ХЦК–ПЗ, который наряду с сокращением желчного пузыря способствует расслаблению сфинктера Одди. Побудительным мотивом к выработке (выбросу ХЦК–ПЗ) является жирная пища, при этом объем желчного пузыря уменьшается на 30–80%. Гормональные влияния сильнее нервных, тем более что ХЦК–ПЗ выступает также и как нейротрансмиттер. До настоящего времени не совсем ясны многие механизмы регуляции: тем более что открываются все новые регулирующие компоненты (в частности эндогенные пептиды группы эндорфинов). Ясно только, что влияние различных гастроинтестинальных гормонов в значительной степени определяется саморегуляцией органов, которая сложна в физиологических условиях и не до конца ясна при различной патологии этой системы [6,9]. Функциональные заболевания желчных путей – комплекс клинических симптомов, развившихся в результате моторно–тонической дисфункции желчного пузыря, желчных протоков и сфинктеров. Согласно последней Международной классификации (Римский консенсус, 2006), дисфункциональные расстройства билиарного тракта принято подразделять на два типа: Е1 – дисфункцию желчного пузыря и Е2 – дисфункцию сфинктера Одди. В последней Международной классификации болезней (МКБ–10) под рубрикой К 82.8 выделены только «дискинезия желчного пузыря и пузырного протока» и под рубрикой К 83.4 «спазм сфинктера Одди». Различают первичные и вторичные дисфункциональные расстройства. Первичные встречаются редко и в среднем составляют 10–15%. При этом снижение сократительной функции желчного пузыря может быть связано как с уменьшением мышечной массы, так и со снижением чувствительности рецепторного аппарата к нейрогуморальной стимуляции. Вторичные дисфункциональные нарушения билиарного тракта могут наблюдаться при гормональных расстройствах: лечении соматостатином, при синдроме предменструального нарушения, беременности, после резекции же¬лудка, наложения анастомозов, ваготомии, системных заболеваниях, целиакии, диабете, гепатите, циррозе печени, еюностомии, а также при наличии воспаления и камней в желчном пузыре; важное значение имеют психоэмоциональные перегрузки, стрессовые ситуации, общие неврозы. Для большинства больных, перенесших холецистэктомию, характерна недостаточность сфинктера Одди с непрерывным истечением желчи, реже отмечается его спазм; после дистальной резекции желудка возникает снижение продукции гормонов с вытекающими моторными расстройствами. Классификация дисфункциональных расстройств представлена в таблице 1. Клинические проявления достаточно хорошо известны: при гиперкинетических расстройствах возникают коликообразные боли различной интенсивности без иррадиации или с иррадиацией вправо, в спину, иногда в левую половину живота (при вовлечении протоковой системы поджелудочной железы). При гипокинезии – тупые боли в правом подреберье, чувство давления, распирания, которые усиливаются при изменении положения тела с увеличением внутрибрюшного давления. Общими для разных форм дисфункции являются горечь во рту, вздутие живота, неустойчивый стул. Центральным симптомом дисфункциональных расстройств является билиарный тип боли. Диагностические критерии дисфункции желчного пузыря 1. Повторяющиеся эпизоды умеренной или тяжелой боли, локализованной в эпигастрии или правом подреберье и продолжающиеся 20 мин. и более по крайней мере в течение 3 мес. (боль определяется как умеренная, когда она нарушает ежедневную деятельность пациента, и как тяжелая, когда требует незамедлительной медицинской консультации или медикаментозного купирования). Кроме того, боль может сочетаться с одним и более из следующих признаков: • тошнота, рвота; • иррадиация боли в спину или правую лопатку; • возникновение боли после приема пищи; • возникновение боли в ночное время. 2. Нарушение функции желчного пузыря. 3. Отсутствие структурных нарушений, объясняющих данные симптомы. Очень важным объективным симптомом нарушенной моторики желчного пузыря является ультразвуковой феномен сладжа, который, по нашим данным, может быть представлен в двух вариантах: а) диффузно; б) пристеночно. Пристеночный вариант в зависимости от клинической ситуации может быть характеризован как «воспалительный» или без воспаления, но тогда элементы осадка, формирующие его, являются достаточно крупными. И все же наличие осадка не объясняет симптом болей. В дополнение к этому анализу должен быть подвергнут весь клинический симптомокомплекс. Диагностические критерии ДСО а) Билиарная ДСО 1–го типа. Приступ болей «билиарного» типа в сочетании с тремя следующими признаками: А. подъем АСТ и (или) ЩФ в два и более раз при 2–кратном исследовании; Б. замедленное выведение контрастного вещества при ЭРПХГ (более 45 мин.); В. расширение общего желчного протока более 12 мм. б) Билиарная ДСО 2–го типа. Приступ болей «билиарного» типа в сочетании с одним или двумя следующими признаками: А. подъем АСТ и (или) ЩФ в 2 и более раз при 2–кратном исследовании; Б. замедленное выведение контрастного вещества при ЭРПХГ (более 45 мин.); В. расширение общего желчного протока более 12 мм. в) Билиарная ДСО 3–го типа Наблюдается только приступ болей «билиарного» типа. г) Панкреатический тип ДСО В его наиболее очевидной форме (подобно билиарному 1–го типа) панкреатический тип ДСО может быть представлен классическим панкреатитом с эпигастральными болями, которые часто иррадиируют в спину и сопровождаются повышением сывороточной амилазы или липазы. Отсутствие традиционных причин панкреатита (злоупотребления алкоголем и камней) часто приводит к диагнозу идиопатического рецидивирующего панкреатита. При менее очевидных формах (подобно 3–му типу билиарной ДСО) боли носят похожий характер, но нет подъема панкреатических ферментов; у многих подобных пациентов симптоматология может быть проявлением синдрома функциональных болей. В тех случаях, когда ЭРПХГ исключает отсутствие стриктуры, показана манометрия билиарного и панкреатического сфинктеров. Дополнительные инструментально–лабораторные диагностические подходы. Как видно из представленных диагностических критериев ІІІ Римского консенсуса, диагноз основывается в основном на клинических проявлениях. Всемирный конгресс гастроэнтерологов (Бангкок, 2002) определил, что медицина, основанная на доказательствах, требует не консенсуса, а доказательств. Там же было констатировано, что ДСО следует отнести не к четко определенным заболеваниям, а к состояниям с вариабельным взаимоотношением «дисфункция – симптом»; неясно, можно ли рассматривать замедленное опорожнение желчного пузыря как определенную клиническую проблему (нозологическую форму). По этой причине ни один из используемых тестов не является стандартом, а диагностическая ценность их остается спорной. Тем не менее наличие указанных жалоб предполагает определенный алгоритм обследования с проведением скрининговых и уточняющих тестов. Функциональные пробы печени – повышение печеночных ферментов и/или билирубина, совпадающее по времени по крайней мере с двумя эпизодами билиарных болей, позволяет заподозрить ДСО. Панкреатические ферменты в крови и моче, значимое повышение амилазы или липазы, совпадающие по времени с панкреатическими болями, предполагает панкреатит, обусловленный ДСО. Болевые провоцирующие тесты – использование морфина (простигмина), провоцирующего ДСО, существенно ограничено его чувствительностью и специфичностью. Ультрасонография (УЗИ) – для оценки функции желчного пузыря проводят ультразвуковое исследование с пробным завтраком. Сократительная способность желчного пузыря считается нормальной, если его объем к 30 мин. уменьшается на 30–70% от исходного. У пациентов с удаленным желчным пузырем ультразвуковое сканирование может быть использовано для определения диаметра общего желчного и/или панкреатического протоков до и после введения провокационных агентов (холецистокинином, морфином, жирной пищей). Расширение общего желчного протока свыше 8 мм может указывать на препятствие оттоку желчи через сфинктер Одди (СО), но эти данные диагностически незначимы, так как подобное явление наблюдается у 34% бессимтомных пациентов после холецистэктомии. Диаметр желчных протоков измеряют с интервалом в 15 мин. в течение 1 ч. В норме диаметр желчных протоков не изменяется. При увеличении диаметра на 2 мм и более по сравнению с исходным можно предположить наличие ДСО. Чувствительность и специфичность провоцирующих тестов (приема жирной пищи, ХЦК–теста, секретинового теста для подтверждения панкретической ДСО) для демаскировки частично суженного холедоха не известны. ЭГДС с осмотром фатерова соска также входит в программу обследования больных для исключения дуоденальной патологии (дивертикул, папиллит). Может быть использовано многофракционное поминутное дуоденальное зондирование, позволяющее определить не только объем различных сегментов желчной системы (желчный пузырь, общий желчный проток), но и функциональное состояние желчного пузыря и отдельных сфинктеров билиарного тракта (методика описана в монографиях В.А. Максимова и соавт., 1998, 2008) [5,6]. Из других инструментально–лабораторных тестов следует упомянуть о динамической холесцинтиграфии, которая основана на избирательном поглощении из крови гепатоцитами и экскреции в составе желчи меченных Тс 99 радиофармпрепаратов. Ценность метода заключается в возможности непрерывного длительного наблюдения за процессами перераспределения РФП в гепатобилиарной системе в физиологических условиях, что позволяет косвенно судить о функциональном состоянии гепатоцитов, количественно оценить эвакуаторную способность желчного пузыря, а также выявить нарушения желчеоттока, связанные как с механическим препятствием в билиарной системе, так и спазмом сфинктера Одди. Показано, что результаты холесцинтиграфии коррелируют с данными манометрии сфинктера Одди [12]. Холедохосцинтиграфия – полезный скрининговый метод отбора больных после холецистэктомии для проведения манометрии сфинктера Одди. Магнитная резонансная холангиопанкреатография (МРХПГ; предпочтительно с введением секретина) – безопасный способ осмотра билиарных и панкреатических протоков, который дает возможность исключить другие заболевания поджелудочной железы и желчных путей, вызывающие сходный болевой синдром (хронический панкреатит, закупорку протока конкрементом, стриктуры протоков, опухоли фатерова соска и т.д.). Использование этой методики целесообразно у больных ДСО 2–го и 3–го типов, при ведении которых рекомендуется избегать по возможности инвазивных обследований (ЭРХПГ и эндоскопическая манометрия СО) [13]. Эндоскопическая ретроградная холангиопанкреатография (ЭРХПГ): данные ЭРХПГ, такие, как диаметр холедоха более 12 мм и замедленное выделение контраста (более 45 мин.), являются диагностическими критериями ДСО. Дополнительными признаками являются расширение панкреатического протока более чем на 5 мм и замедленное выведение контраста из панкреатических протоков (более 10 мин.). Однако премедикация, недостаточная стандартизация метода и риск развития панкреатита существенно ограничивают ценность метода. Трансэндоскопическая манометрия СО – наиболее достоверный метод изучения функции сфинктера Одди. Он включает определение базального давления сфинктера с последующим изучением фазово–волновых изменений давления – амплитуды, частоты и направления распространения фазовых волн. Нормальным показателем давления в общем желчном протоке служит давление, превышающее таковое в двенадцатиперстной кишке на 10 мм рт.ст. Давление в СО, составляющее в обычных условиях 18±4 мм рт.ст., повышается при его спастических сокращениях до 110±25 мм рт.ст. [3,16]. Признаками ДСО при манометрическом исследовании являются; а) повышение базального давления в просвете сфинктеров; б) увеличение амплитуды и частоты фазовых скращений (тахиоддия); в) увеличение частоты ретроградных сокращений; г) парадоксальный ответ на введение аналогов холецистокинина. Манометрия не показана пациентам с ДСО 1–го типа, так как эндоскопическая сфинктеротомия у них оказывается эффективной более чем в 90% случаев (даже при нормальных результатах манометрии). При 3–м типе ДСО патологические изменения функции СО выявляются редко, а риск развития осложнений в результате исследования достаточно высок. У пациентов со 2–м типом ДСО проведение манометрического исследования наиболее обоснованно, так как в 50% случаев у них повышен уровень базального давления сфинктера. У пациентов с панкреатическим типом заболевания велика вероятность развития панкреатита, связанного с проведением исследования [14,15]. Повышенное базальное давление – признак или стеноза, или спазма СО. При спазме давление СО уменьшается после назначения препаратов, расслабляющих гладкую мускулатуру. По этой причине назначение манометрии СО должно основывается на тяжести клинических проявлений и эффективности консервативной терапии. Манометрия позволяет точно установить диагноз до начала применения более радикальных методов лечения. Комплексное психологическое исследование позволяет выявить наличие психоэмоциональных нарушений у пациентов с функциональными заболеваниями желчного пузыря, оценить структуру и степень выраженности этих нарушений. При исследовании психического состояния больных значительное место занимают психометрические методики для лучшего понимания личности пациента и его собственного осмысления и понимания своего заболевания [2,7]. Таким образом, существующий на сегодняшний день комплекс обследования больных с билиарной дисфункцией позволяет отделить группу с органической патологией и предпринять необходимый комплекс лечения (нередко хирургического плана) больных с функциональной патологией, нуждающихся в эффективной фармакотерапии. Основной целью лечения больных с дисфункцией билиарного тракта является восстановление нормального тока желчи и секрета поджелудочной железы по билиарным и панкреатическим протокам. Исходя из основной цели задачами лечения должны являться: а) восстановление, а при невозможности – восполнение продукции желчи (при развитии хронической билиарной недостаточности); б) повышение сократительной функции желчного пузыря (при его несостоятельности); в) снижение сократительной функции желчного пузыря (при его гиперфункции); г) восстановление тоничности сфинктерной системы; д) восстановление давления в двенадцатиперстной кишке (от чего зависит адекватный градиент давления в билиарном тракте) [8,9,11]. До сих пор в системе лечебных мероприятий заметную роль занимает диетотерапия. Адекватный режим питания с частыми приемами небольших количеств пищи (5–6–разовое питание) способствует нормализации давления в двенадцатиперстной кишке и регулирует опорожнение желчного пузыря и протоковой системы. Из рациона исключаются алкогольные напитки, газированная вода, копченые, жирные и жареные блюда и приправы в связи с тем, что они могут вызвать спазм сфинктера Одди. В диетическом рационе учитывают влияние отдельных пищевых веществ на нормализацию моторной функции желчного пузыря и желчевыводящих путей. Так, при гиперкинетическом типе дисфункции должны быть резко ограничены продукты, стимулирующие сокращение желчного пузыря – животные жиры, растительные масла, наваристые мясные, рыбные, грибные бульоны. При гипотонии желчного пузыря больные обычно хорошо переносят некрепкие мясные и рыбные бульоны, сливки, сметану, растительные масла, яйца всмятку. Растительное масло назначают по чайной ложке 2–3 раза/сут. за 30 мин. до еды в течение 2–3 нед. Для предотвращения запоров рекомендуют продукты, способствующие опорожнению кишечника (морковь, тыква, кабачки, зелень, арбузы, дыни, чернослив, курага, апельсины, груши, мед). Это особенно важно потому, что нормально работающий кишечник – это нормальное внутрибрюшное давление и нормальный пассаж желчи в двенадцатиперстную кишку. Использование пищевых отрубей (при достаточном количестве воды) важно не только и не столько для работы кишечника, но и для моторики билиарного тракта, и особенно желчного пузыря, имеющего осадок. Из лекарственных препаратов используют препараты, влияющие на моторную функцию желудочно–кишечного тракта, которая определяется активностью гладкомышечных клеток. При этом нарушение двигательной функции играет значительную роль не только в формировании болевого синдрома, но и большинства диспептических расстройств (чувство переполнения в желудке, отрыжка, изжога, тошнота, рвота, метеоризм, поносы, запоры). Большинство из указанных выше симптомов наблюдаются как при гипотоническом, так и при гиперкинетическом типах дисфункции. Так, при спастической дисфункции любого отдела пищеварительного тракта наблюдается повышение внутрипросветного давления и нарушение продвижения содержимого по полому органу, что создает предпосылки для возникновения болей, интенсивность которых пропорциональна нарастанию давления. ДСО характерна для больных с удаленным желчным пузырем. Это служит косвенным подтверждением того, что желчный пузырь служит резервуаром, «гасящим» чрезмерные всплески давления во всем желчном тракте. После удаления желчного пузыря даже умеренное сокращение сфинктера Одди может привести к существенному повышению давления во всем желчном тракте, и, как следствие, может появиться боль, что подтверждается экспериментами с введением морфина, повышающего давление в желчных путях. При ДСО 1–го типа показано проведение папиллосфинктеротомии, 2–3–го типа – проведение лекарственной терапии. Группа средств, влияющих на тонус гладкой мускулатуры, включает: антихолинэргические вещества, нитраты, блокаторы кальциевых каналов, миотропные спазмолитики, интестинальные гормоны (ХЦК, глюкагон) [4,8]. Антихолинэргические средства. Могут быть использованы как неселективные (препараты красавки, атропин, метацин, платифиллин и др.), так и селективные М1–холиноблокаторы (пирензепин и др.). Побочные эффекты – сухость во рту, затруднение мочеиспускания, нарушение зрения – ограничивают применение препаратов данной группы. Попыткой увеличить безопасность терапии М–холиноблокаторами было создание гиосцина бутилбромида, относящегося к селективным М–холиноблокаторам. Он действует на М2– и М3–подтипы рецепторов [17], локализованных преимущественно в стенках верхних отделов желудочно–кишечного тракта, желчного пузыря и билиарных протоков. В отличие от атропина препарат не проникает через гематоэнцефалический барьер и имеет низкую (8–10%) системную биодоступность. Небольшая часть дозы гиосцина бутилбромида, абсорбированная в кровоток, оказывает также ганглиоблокирующее действие. Гиосцина бутилбромид (Бускопан) накапливается в гладкой мускулатуре желудочно–кишечного тракта, выводится из организма в неизмененном виде почками. Действует преимущественно на желудок, двенадцатиперстную кишку, желчный пузырь. Несмотря на то что гиосцина бутилбромид не проникает в ЦНС, он может вызывать типичные для М–холинолитиков побочные эффекты, которые проходят самостоятельно (в сравнении с плацебо на 4% чаще). Поэтому он противопоказан при глаукоме, доброкачественной гиперплазии простаты, органических стенозах желудочно–кишечного тракта, тахиаритмиях [1]. Блокада мускариновых рецепторов на постсинаптических мембранах органов–мишеней приводит к снижению внутриклеточной концентрации ионов кальция и расслаблению мышц. При этом степень миорелаксации зависит от тонуса парасимпатической нервной системы, что определяет существенные различия индивидуальной эффективности препаратов данной группы. Нами было проведено изучение эффективности и безопасности курсового лечения Бускопаном в дозе 10 мг 3 раза/сут. в течение 14 дней. В исследование было включено 60 больных (10 мужчин, 50 женщин, средний возраст – 47,4±2,7 лет). Из них с дисфункцией желчного пузыря и/или сфинктера Одди было 35 пациентов, с постхолецистэктомическим синдромом – 25 больных. До и после лечения проводилась оценка выраженности симптомов в баллах по шкале Лайкерта, сократительной способности желчного пузыря по результатам ультразвукового исследования и моторики кишки по данным электромиографии. Использовали следующие критерии эффективности: отличная эффективность – нормализация клинических и инструментальных показателей; хорошая – заметное их улучшение; удовлетворительная – незначительное улучшение; плохая – отсутствие или отрицательная динамика клинических и/или инструментальных показателей. Результаты исследования показали, что исходно интенсивность основных симптомов (боль в правом подреберье, тошнота, горечь, чувство тяжести, чувство быстрого насыщения) составляла от 2,5 до 3,7 балла. После лечения отметили достоверное уменьшение интенсивности симптомов от 1,1 до 1,9 балла. Сроки купирования симптомов составляли 3–7 дней. Нормализацию сократительной способности желчного пузыря наблюдали в 80% случаев. По данным электромиографии отметили тенденцию к усилению мощности на частотах двенадцатиперстной кишки при восстановлении коэффициента ритмичности, что свидетельствовало об улучшении пропульсивной способности двенадцатиперстной кишки. Этот эффект Бускопана, видимо, может быть объяснен ганглиоблокирующим действием препарата. Таким образом, отличная и хорошая эффективность Бускопана при лечении больных дисфункцией билиарного тракта составила 91,6% случаев. Переносимость препарата была хорошей в 95% случаев. Высокая эффективность препарата может быть объяснена двойным механизмом действия – расслабляющим на сфинктер Одди и стимулирующим на моторику двенадцатиперстной кишки. Нитраты. Возможно использование нитроглицерина, нитросорбида. Механизм действия нитратов – образование в гладких мыщцах свободных радикалов окиси азота, которые активируют гуанилатциклазу и увеличивают содержание цГМФ, что приводит к их расслаблению. Выраженные кардиоваскулярные эффекты, побочные действия и развитие толерантности делают их непригодными для достаточно продолжительной терапии. Блокаторы кальциевых каналов. Неселективные блокаторы кальциевых каналов (нифедипин, верапамил, дилтиазем и др.) закрывают кальциевые каналы клеточных мембран, препятствуют входу ионов кальция в цитоплазму и вызывают расслабление гладкой мускулатуры. Однако эта группа препаратов действует прежде всего на сердечно–сосудистую систему; для достижения гастроэнтерологических эффектов требуются высокие дозы, что практически исключает их использование. Селективные блокаторы кальциевых каналов (пинавериум хлорид, пинавериум бромид) в основном действуют на уровне толстой кишки. Малое количество препарата (5–10%) действует, по всей вероятности, и на уровне билиарного тракта, но эта сторона их действия и установление места в лечении указанной патологии требуют дальнейших исследований, хотя опосредованные эффекты, связанные с уменьшением внутрипросветного давления, облегчают пассаж желчи. Блокатор натриевых каналов (мебеверин) снижает проницаемость мембраны для внеклеточного натрия, что нарушает поступление натрия в клетку, замедляет процессы деполяризации и блокирует вход кальция в клетку через медленные каналы. В результате прекращается фосфорилирование миозина и отсутствует сокращение мышечного волокна. Кроме того, мебеверин препятствует пополнению внутриклеточных кальциевых депо, что в итоге приводит лишь к кратковременному выходу ионов калия из клетки и ее гипополяризации, которая предупреждает развитие постоянного расслабления мышечной клетки. Таким образом, мебеверин приводит только к снятию спазма без развития гипотонии гладкой мускулатуры [4]. На подавлении активности фосфодиэстеразы (ФДЭ) основан эффект традиционных спазмолитиков, таких как дротаверин. ФДЭ представлена в гладкомышечных клетках кишечника, желче– и мочевыводящих путей, ее блокада дротаверином оказывает спазмолитическое действие, независимо от степени контракции и причины, ее вызвавшей. Дротаверин обладает противоотечным и антивоспалительным эффектами, так как ФДЭ IV типа активно участвует в процессе развития воспаления. В настоящее время среди миотропных спазмолитиков обращает на себя внимание препарат гимекромон, который оказывает избирательное спазмолитическое действие на сфинктер Одди и сфинктер желчного пузыря, а также усиливает образование и отделение желчи [9]. Ботулинический токсин – сильный ингибитор выделения ацетилхолина: при использовании в виде инъекций в СО уменьшает его давление, улучшает ток желчи и приносит симптоматическое облегчение, но ответ на лечение преходящий. Говоря о гипофункции желчного пузыря, основными походами к лечению следует считать: 1. препараты, усиливающие моторику желчного пузыря (холекинетики) – холецистокинин, сульфат магния, оливковое масло и др.; 2. прокинетики (домперидон, метоклопрамид) для нормализации давления в двенадцатиперстной кишке и улучшения градиента давления в билиарном тракте; 3. препараты, уменьшающие висцеральную гиперчувствительность или воспаление (НПВП); 4. холецистэктомию. При сочетании гипомоторной дисфункции желчного пузыря и гипертонуса сфинктера Одди целесообразно использование Бускопана или добавление к холекинетикам гимекромона. Таким образом, имеющиеся диагностические тесты (УЗИ, ЭРПХГ, манометрия сфиктера Одди, МРПХГ) позволяют выделить больных с органической и функциональной патологией билиарной системы и определить соответствующий лечебный подход. Существующий набор препаратов для коррекции нарушений моторики билиарного тракта достаточен для оптимизации его работы у большего количества больных. Бускопан нормализует тонус протоков и сфинктеров и регулирует градиент давления, восстанавливая нормальный пассаж желчи. По нашим данным, Бускопан является препаратом выбора и обеспечивает максимальный положительный эффект.
Литература 1. Сфинктеры пищеварительного тракта / Под ред. проф. В.Ф. Байтингера. Томск, 1994. 207 с. 2. Максимов В.А. и соавт. Функциональные расстройства и острые неинфекционные заболевания органов пищеварения. М., 2009, 383 с. 3. Corazziari E. Shatter E.A., Hogan W.J. et al. Functional Disorders of the Biliary Tract and the Pancreas // Rome II. The Functional Gastrointestinal Disorders. Diqgnosis, Pathophysiology and Treatment, Second Edition, 1999 – P. 433–481. 4. Cohen S, Bacon BR, Berlin JA, et al. National Institutes of Health State–of–Science Conference Statement: ERCP for diagnosis and therapy, January 14–16, 2002. Gastrointest Endosc. 2002;56:803–809. 5. Smith M.T. Нарушение функции сфинктера Одди // Секреты гастроэнтерологии: Пер. с англ. – М.; СПб: БИНОМ, Невский диалект, 1998. – С. 357–372. 6. Лейшнер У. Практическое руководство по заболеваниям желчных путей. – М.: ГЭОТАР Медицина, 2001. – 264 с. 7. Вишневская В.В., Лоранская И.Д., Малахова Е.В. Билиарные дисфункции – принципы диагностики и лечения // РМЖ. 2009. – Т. 17. – № 4. – С. 246–250. 8. Махов В.М., Ромасенко Л.В., Турко Т.В. Коморбидность дисфункциональных расстройств органов пищеварения // РМЖ. – 2007. – Т. 9. – № 2. – С. 37–42. 9. Geenen J.E. The efficacy of endoscopic sphincterotomy after cholecystectomy in patients with sphincter of Oddi dysfunction // New Engl. J. Med. – 1989. – Vol. 320. – P. 82–87. 10. Lehman G.Y., Sherman S. Sphincter of Oddi dysfunction // Int. J. Poncreatol. – 1996. –Vot.20. – P. 11–25. 11. Яковенко Э.П., Григорьев П.Я. Хронические заболевания внепеченочных желчевыводящих путей. Диагностика и лечение. Методическое пособие для врачей. – 2000. – 31 с. 12. Маев И.В., Самсонов А.А., Салова Л.М. и соавт. Диагностика и лечение заболеваний желчевыводящих путей: учебное пособие. – М.: ГОУ ВУНМЦ МЗ РФ, 2003. – 96 с. 13. Курыгин А.А., Багаев В.А., Курыгин Ал.А., Сысоева Л.И. Моторная функция тонкой кишки в норме и при некоторых патологических состояниях. Санкт–Петербург: НАУКА,1994. – 202 с. 14. Белоусов Ю.Б. Спазмолитические средства // Фармацевт. вестн. – 2001. – № 36 – с. 235. 15. Минушкин О.Н., Максимов В.А Билиарно–печеночная дисфункция. Понятие, классификация, диагностика, лечебные подходы и место Одестона в лечении. М., 2008, 26 с. 16. Минушкин О.Н. Дисфункциональные расстройства билиарного тракта. Патофизиология, диагностика и лечебные подходы. М., 2003, 23 с. 17. Tytgat G. Hyoscine butylbromide: a review of its use in the treatment of abdominal cramping and pain. Drugs 2007; 67(9):1343–1357.
Методы лечения холангиокарциномы
Выбор тактики терапии при раке протока желчного пузыря зависит от степени запущенности заболевания, локализации новообразования, возраста пациента, его общего самочувствия, наличия сопутствующих заболеваний.
Хирургические методы
Оперативное вмешательство при холангиокарциноме печени — это единственный вариант добиться полного выздоровления пациента. Но проведение радикальной операции возможно лишь в том случае, когда патология была выявлена на ранней стадии, опухоль имеет небольшие размеры и не вышла за пределы протоков. К сожалению, на этой стадии болезнь диагностируют крайне редко и обычно случайно, при проведении обследования по поводу другой патологии.
Вид оперативного вмешательства зависит от локализации очага поражения. При раке внутрипеченочных желчных протоков проводится частичная резекция печени. Оставшаяся часть органа пи этом продолжает функционировать.
При раке внепеченочных желчных протоков показано удаление очагов поражения, лимфоузлов, а также желчного пузыря, части печени, 12-ти перстной кишки, поджелудочной железы. Это сложная операция, которая может привести к развитию тяжелых осложнений. Поэтому выполнять ее должен хирург с большим практическим опытом проведения подобных хирургических вмешательств. Если диагностирован один узел небольшого размера, но при этом сильно нарушена работа печени (например, из-за цирроза), то проводится трансплантация.
Паллиативные операции
Проводятся, если радикальное вмешательство невозможно. Это может быть установка в желчные протоки стентов, наружно-внутренне и наружное дренирование. Специалисты нашей клиники имеют большой практический опыт проведения подобных операций.
Лучевая терапия
Может быть назначена до или после операции с целью уменьшения размеров рака желчных протоков печени и профилактики рецидивов заболевания. При запущенной онкологии радиотерапия может использоваться в качестве самостоятельного метода при проведении паллиативного лечения, направленного на облегчение самочувствия больного и повышение качества его жизни. Чаще всего используют внешние источники облучения. В ряде случаев применяют внутрибилиарную брахитерапию (пациенту в желчные пути на короткое время вводят специальный зонд, который является источником излучения).
Химиотерапия
Также может быть назначена до или после операции либо самостоятельно, на последних стадиях холангиоцеллюлярного рака для облегчения страданий пациента. Химиотерапия может быть системной или внутриартериальной, когда растворы препаратов вводятся непосредственно в печеночную артерию. В результате в кровь попадает небольшое количество препарата, благодаря чему дозировку можно увеличить без риска развития побочных эффектов.
Химиолучевая терапия
Сочетание двух вышеперечисленных методик. Это позволяет более эффективно уничтожать клетки опухоли. Но при таком лечении велик риск развития серьезных побочных эффектов.
Строение печени
Печень и желчный пузырь
Выполнение многочисленных функций связано с особенностями внутреннего строения печени. Плотная оболочка, покрывающая печень под брюшиной, уходит вглубь органа и разделяет его на дольки призматической формы диаметром около 1,5 мм. Количество таких печеночных долек у человека достигает 500 тыс., они являются структурно-функциональной единицей печени (рис. 2). В дольке клетки печени (гепатоциты) группируются в виде радиальных пластинок, между которыми располагаются широкие кровеносные капилляры (синусоидные), сходящиеся к печени). Внутри радиальных пластинок между двумя соседними рядами гепатоцитов образуются щели, называемые желчными проточками: в них поступает желчь, продуцируемая гепатоцитами.
Каждая печеночная клетка одной своей стороной соприкасается со стенкой кровеносного капилляра, а другой – с просветом желчного проточка. Такое строение позволяет гепатоцитам работать в двух направлениях: выделять желчь в желчные проточки и направлять глюкозу, белки, жиры, витамины, мочевину и пр. в кровь. Сырье для производства желчи и многочисленных веществ также поступает по капиллярам с артериальной и венозной кровью. Как уже говорилось, артериальная кровь прибывает в печень по ветвям печеночной артерии, а венозная – по разветвлениям воротной вены. В широких капиллярах печеночных долек артериальная кровь смешивается с венозной и течет очень медленно, что способствует обмену веществ между кровью и гепатоцитами. В стенке капилляров располагаются также особые клетки – звездчатые макрофаги, которые выполняют защитную функцию. Они могут захватывать из крови и уничтожать различные чужеродные частицы, микроорганизмы, поврежденные клетки. Насыщенная продуктами жизнедеятельности гепатоцитов кровь поступает из капилляров в центральную вену дольки, а оттуда – в более крупные вены, по которым выносится из печени и попадает в нижнюю полую вену, т.е. возвращается в общий кровоток.
Профилактика
Специфической профилактики заболевания не существует. Снизить риск развития онкологического поражения желчных протоков можно, выполняя следующие рекомендации:
- правильное питание;
- контроль веса;
- соблюдение режима труда и отдыха;
- избегание стрессовых ситуаций;
- отказ от малоподвижного образа жизни, регулярные прогулки на свежем воздухе;
- отказ от вредных привычек;
- соблюдение техники безопасности при работе на вредном производстве;
- вакцинация от вирусного гепатита;
- регулярное, не реже раза в год, прохождение профилактических осмотров, это поможет выявить возможные патологические изменения в желчных протоках на ранней стадии, что существенно облегчит лечение и улучшит прогноз.
Информация проверена экспертом
Михайлов Алексей Геннадьевич оперирующий онколог, врач высшей квалификационной категории, к.м.н. стаж: 21 год
Информация в статье предоставлена в справочных целях и не заменяет консультации квалифицированного специалиста. Не занимайтесь самолечением! При первых признаках заболевания необходимо обратиться к врачу.